
【题目】钼是一种过渡金属元素,通常用作合金及不锈钢的添加剂,这种元素可增强合金的强度、硬度、可焊性及韧性,还可增强其耐高温及耐腐蚀性能。如图是化工生产中制备金属钼的主要流程图。
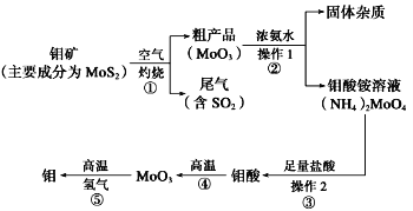
(1)写出在高温下发生反应①的化学方程_____
(2)生产中用足量的浓氨水吸收反应①的尾气合成肥料,写出该反应的离子方程式:___
(3)如果在实验室模拟操作1和操作2,则需要使用的主要玻璃仪器有_____
(4)某同学利用如图所示装置来制备氢气,利用氢气还原三氧化钼,根据要求回答问题:

①步骤⑤的化学反应方程式为___。请设计一个实验方案验证H2的还原性并检验其氧化产物,其装置连接顺序是____。
②在烧瓶A中加入少量硫酸铜的目的是__
③两次使用D装置,其中所盛的药品依次是_____、____。
【答案】2MoS2+7O2![]() 2MoO3+4SO2 SO2+2NH3·H2O=2NH4++SO32-+ H2O 烧杯、漏斗、玻璃棒 MoO3 +3H2
2MoO3+4SO2 SO2+2NH3·H2O=2NH4++SO32-+ H2O 烧杯、漏斗、玻璃棒 MoO3 +3H2![]() Mo +3H2O ACBDD 可形成原电池,加快生成氢气的速率 无水硫酸铜 碱石灰
Mo +3H2O ACBDD 可形成原电池,加快生成氢气的速率 无水硫酸铜 碱石灰
【解析】
根据流程图分析主要反应和主要操作,完成化学方程式、选择所需仪器。根据实验目的,设计相关实验,并防止空气的影响。
(1)据流程图找出反应①的反应物、生成物,并用化合价升降法配平,得2MoS2+7O2![]() 2MoO3+4SO2;
2MoO3+4SO2;
(2)足量的浓氨水吸收SO2生成正盐,离子方程式为SO2+2NH3·H2O=2NH4++SO32-+ H2O;
(3)步骤②得固体和溶液,操作1为过滤。步骤③复分解反应能进行,则钼酸难溶于水,操作2为过滤。需要使用的主要玻璃仪器有烧杯、漏斗、玻璃棒;
(4)①步骤⑤的化学反应方程式为MoO3 +3H2![]() Mo +3H2O;制备H2并还原MoO3可证明其还原性,用无水硫酸铜检验氧化产物水,必须对氢气干燥,并防止空气中水汽干扰。故装置连接顺序是ACBDD,故答案为:MoO3 +3H2
Mo +3H2O;制备H2并还原MoO3可证明其还原性,用无水硫酸铜检验氧化产物水,必须对氢气干燥,并防止空气中水汽干扰。故装置连接顺序是ACBDD,故答案为:MoO3 +3H2![]() Mo +3H2O;ACBDD;
Mo +3H2O;ACBDD;
②在烧瓶A中加入少量硫酸铜,锌置换出铜,从而形成原电池,加快生成氢气的速率;
③第一次使用D装置,所盛药品为无水硫酸铜,用于检验氧化产物水。第二次使用D装置,所盛药品为碱石灰等,防止空气中的水汽使无水硫酸铜变蓝,故答案为:无水硫酸铜;碱石灰。


科目:高中化学 来源: 题型:
【题目】某待测液中可能含有Cu2+、Mg2+、Fe3+、K+、NH![]() 、Cl-等离子,现通过如下实验对其中的阳离子进行检验:
、Cl-等离子,现通过如下实验对其中的阳离子进行检验:
(1)取少量待测液,仔细观察,呈无色。
(2)向上述待测液中滴加NaOH溶液,有白色沉淀生成;实验过程中还有刺激性气味的气体产生,该气体能使湿润的红色石蕊试纸变蓝。
据此可以判断该待测液中一定含有的阳离子是___,一定没有的阳离子是___。还有一种阳离子没有检验,检验这种离子的实验方法是(填写实验名称)___,现象是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究小组拟合成染料X和医药中间体Y。
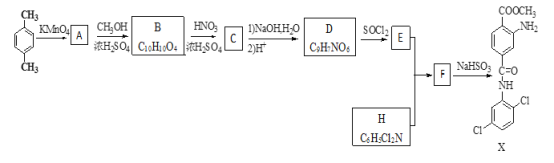
已知:①![]() ②
②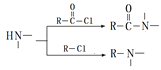 ③
③![]() ④
④![]() 。
。
(1)下列说法正确的是_________。
A.化合物A能与能与NaHCO3反应产生气体 B.X的分子式是C15H14Cl2O3N2
C.化合物C能发生取代、还原、加成反应 D.A→B,B→C的反应类型均为取代反应
(2)化合物D的结构简式是_________。
(3)写出E+H→F 的化学反应方程式__________________。
(4)写出化合物B(C10H10O4)同时符合下列条件的两种同分异构体的结构简式______________。
①与NaHCO3溶液反应,0.1mol该同分异构体能产生4.48L(标准状况下)CO2气体;②苯环上的一氯代物只有两种且苯环上的取代基不超过三个;③核磁共振氢谱有五种不同化学环境的氢,且峰面积比为1:2:2:2:3。
(5)设计以乙烯为原料合成制备Y(![]() )的合成路线________________(用流程图表示,无机试剂任选)。
)的合成路线________________(用流程图表示,无机试剂任选)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列各组离子在指定溶液中能大量共存的是( )
A.pH=l的溶液中:Fe2+、NO3-、SO42-、Na+
B.由水电离的c(H+)=1×10-14mo1·L-1的溶液中:Ca2+、K+、Cl-、HCO3-
C.![]() =1013的溶液中:NH4+、Al3+、NO3-、Cl-
=1013的溶液中:NH4+、Al3+、NO3-、Cl-
D.c(Fe3+)=0.1mol·L-1的溶液中:K+、ClO-、SO42-、SCN-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)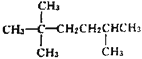 ,请用系统命名法对该物质进行命名:___。若该烃为一单烯烃的加成产物,则单烯烃可能有___种结构。
,请用系统命名法对该物质进行命名:___。若该烃为一单烯烃的加成产物,则单烯烃可能有___种结构。
(2)某含苯环的化合物A,其相对分子质量为104,碳的质量分数为92.3%,A的分子式为___。
(3)若25℃时CH3COOH的电离平衡常数Ka=1.8×10-5mol·L-1,向aLCH3COOH溶液中加入bmol CH3COONa,混合液恢复至25℃时呈中性,则原 CH3COOH溶液的物质的量浓度为____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三个密闭容器中分别充入N2、H2、O2三种气体,以下各种情况下排序正确的是( )
A.当它们的体积和温度、压强均相同时,三种气体的密度:ρ(H2)>ρ(N2)>ρ(O2)
B.当它们的温度和密度都相同时,三种气体的压强:P(H2)>P(N2)>P(O2)
C.当它们的质量和温度、压强均相同时,三种气体的体积:V(O2)>V(N2)>V(H2)
D.当它们的压强和体积、温度均相同时,三种气体的质量:m(H2)>m(N2)>m(O2)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】五种短周期元素X、Y、Z、M、N,其原子半径与原子序数的关系如图,下列说法错误的是( )

A. 非金属性:X>Z
B. 气态氢化物的稳定性:M<N
C. X和Y形成的化合物只可能含离子键
D. M最高价氧化物对应的水化物是一种弱酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】除去粗盐中的杂质 CaCl2、MgCl2 和 Na2SO4,过程如下:
![]()
下列有关说法中,不正确的是( )
A. 除去 Mg2+的主要反应: Mg2++ 2OH-=Mg(OH)2↓
B. 试剂①一定不是Na2CO3溶液
C. 检验 SO42-是否除净:取少量滤液,加稀盐酸酸化,再加 BaCl2 溶液
D. 滤液加稀盐酸时只发生反应:H+ +OH- =H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中学化学中几种常见物质的转化关系如图所示,且已知将F的饱和溶液滴入沸水中,煮沸可得到以H为分散质的红褐色胶体。
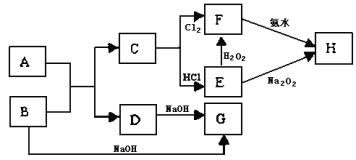
请回答下列问题:
(1)红褐色胶体中H粒子的直径大小范围____;
(2)写出H2O2的电子式:____;
(3)写出B→G的离子方程式____;
(4)若A、B恰好完全反应,将产物C与足量盐酸反应得到amol气体,另取等质量B与足量盐酸反应得到b mol气体,a:b=5:7,则A的化学式为___。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com