
����Ŀ�������ü�������NO2��Ⱦ�����о���CH4+2NO2![]() N2+CO2+2H2O����1 L�ܱ������У����Ʋ�ͬ�¶ȣ��ֱ����0.50 mol CH4��1.2 mol NO2�����n(CH4)��ʱ��仯���й�ʵ�����ݼ��±���
N2+CO2+2H2O����1 L�ܱ������У����Ʋ�ͬ�¶ȣ��ֱ����0.50 mol CH4��1.2 mol NO2�����n(CH4)��ʱ��仯���й�ʵ�����ݼ��±���

����˵����ȷ����
A. ��ʵ�����ݿ�֪ʵ����Ƶ��¶�T1��T2
B. 020 min�ڣ�CH4�Ľ������ʣ��ڣ���
C. 40 minʱ��������T1��Ӧ������Ϊ0.18
D. �����У�010 min�ڣ�NO2�Ľ�������Ϊ0.0300 mol��L-1min-1
 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ҵ��ұ�����ĵ�һ����Ӧԭ��Ϊ2SnO2 + 3C![]() 2Sn + aM��+ CO2��,������˵���д������(����)
2Sn + aM��+ CO2��,������˵���д������(����)
A. ��Ӧ��SnO2����ԭ B. a��ֵΪ3
C. ��Ӧ���������������� D. ÿ����1 mol CO2ת�Ƶ���8 mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ӱ�컯ѧ��Ӧ���ʵ����غܶ࣬ijУ��ѧС����ʵ��ķ�������̽����ʵ��ҩƷ��ͭ������þ��0.5 mol L-1H2SO4��Һ��2 mol L-1 H2SO4��Һ����ͬѧ�о���ʵ�鱨�����±���
ʵ�鲽�� | ���� | ���� |
���ֱ�ȡ�������2 mol L-1 ��������Һ����֧�Թ��� | ��Ӧ������ þ>����ͭ����Ӧ | ����������Խ���ã���Ӧ����Խ�� |
��1�� ��ͬѧ����ʵ�鲽����Ϊ______________________��
��2�� ��ͬѧ��ʵ��Ŀ����__________________________��
Ҫ�ó���ȷ��ʵ����ۣ�����Ҫ���Ƶ�ʵ��������_____________��
��ͬѧΪ�˸���ȷ���о�Ũ�ȶԷ�Ӧ���ʵ�Ӱ�죬������ͼ��ʾװ�ý���ʵ����

��3����ͬѧ��ʵ����Ӧ�òⶨ��������_________________��
��4����ͬѧ��ɸ�ʵ��Ӧѡ�õ�ʵ��ҩƷ��________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijС��Ϊ�о��绯ѧԭ���������ͼװ�á�����������ȷ����

A. a��b������ʱ����Ƭ�ϲ����н���ͭ����
B. ����a��b�Ƿ����ӣ���Ƭ�����ܽ⣬��Һ����ɫ���dz��ɫ
C. a��b�õ�������ʱ�����������b��a
D. a��b�õ�������ʱ��FeƬ�Ϸ���������Ӧ����Һ��SO42-��ͭ�缫�ƶ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������㶹����һ��Ǣ������Ѫ�ܼ�����ҩ����谭Ѫ˨��չ�������㶹�ؿ���ͨ�����·����ϳ�(���ַ�Ӧ������ʡ��)��
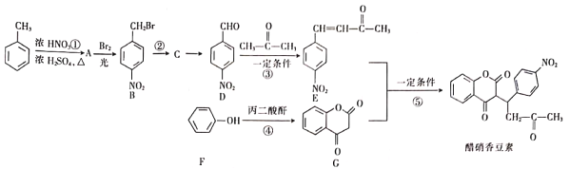
��ش��������⣺
(1)A��������___________�������㶹�������������ŵ�����Ϊ___________��
(2)��Ӧ�ٵķ�Ӧ������___________����Ӧ�ݵķ�Ӧ����Ϊ___________��
(3)C�Ľṹ��ʽΪ___________����Ӧ�ܵĻ�ѧ����ʽΪ______________________��
(4)����E��������˵����ȷ����___________(����ĸ)
a.���������Ը��������Һ����D��E
b.�ں˴Ź������������������շ�
c����˳���칹
d���Է����ӳɷ�Ӧ���ۺϷ�Ӧ��������Ӧ����ȥ��Ӧ
(5)���ӽṹ��ֻ����һ��������ͬʱ��������������G��ͬ���칹�干��___________��
�ٿ����Ȼ�����Һ������ɫ��Ӧ���ڿ���̼��������Һ��Ӧ���ɶ�����̼���塣
���У������ϵ�һ�ȴ���ֻ�����ֵĽṹ��ʽΪ___________����������G�ĸ���ͬ���칹���ѡ�õ�������___________(����ĸ)
a.Ԫ�ط����� b.��������� c.�˴Ź�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ʰ��ᡢ��η�������������ȷ���ǣ� ����
A.���ᡢ���ʳ��
B.���ᡢ��ʯ�ҡ�������
C.���ᡢ�ռ����ͭ
D.���ᡢʯ��ʯ��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������Ȼ�ѧ����ʽ��ȷ������������
A. �����ȼ������H����890.3 kJ��mol��1�������ȼ�յ��Ȼ�ѧ����ʽ�ɱ�ʾΪCH4��g����2O2��g��=CO2��g����2H2O��g������H����890.3 kJ��mol��1
B. 500 ����30 MPa�£���0.5 mol N2��g����1.5 mol H2��g�������ܱ������г�ַ�Ӧ����NH3��g��������19.3 kJ�����Ȼ�ѧ����ʽΪN2��g����3H2��g�� ![]() 2NH3��g������H����38.6 kJ��mol��1
2NH3��g������H����38.6 kJ��mol��1
C. HCl��NaOH��Ӧ���к�����H��-57.3 kJ��mol��1����H2SO4��Ca��OH��2��Ӧ���к�����H��2x��-57.3��kJ��mol��1
D. ��֪2C��s����2O2��g��=2CO2��g������H��a��2C��s����O2��g��=2CO��g������H��b����a<b
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ҵ�Ʊ�������ķ�ӦΪ��3SiCl4(g)+2N2(g)+6H2(g)![]() Si3N4(s)+12HCl(g) ��H<0����0.3 molSiCl4 ��һ���� N2��H2 Ͷ��2 L��Ӧ������ֻ�ı��¶��������Si3N4�������仯���±���
Si3N4(s)+12HCl(g) ��H<0����0.3 molSiCl4 ��һ���� N2��H2 Ͷ��2 L��Ӧ������ֻ�ı��¶��������Si3N4�������仯���±���
ʱ��/min ����/g �� ��/�� | 0 | 1 | 2 | 3 | 4 | 5 | 6 |
250 | 0.00 | 1.52 | 2.80 | 3.71 | 4.73 | 5.60 | 5.60 |
300 | 0.00 | 2.13 | 3.45 | 4.48 | 4.48 | 4.48 | 4.48 |
����˵����ȷ����
A. 250��,ǰ 2min�� Si3N4 ��ƽ����Ӧ����Ϊ 0.02 mol��L��1��min��1
B. ��Ӧ�ﵽƽ��ʱ�� �����¶��� N2 �� H2 ��ת����֮����ͬ
C. �ﵽƽ��ǰ�� 300�������ķ�Ӧ���ʱ� 250��죻 ƽ��� 300��� 250����
D. ��Ӧ�ﵽƽ��ʱ�� ���������·�Ӧ�ų�������һ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��SO2ͨ�����й������̿��ƻ���ҵԭ��H2SO4�������ԴH2��
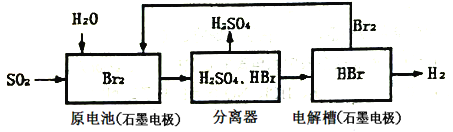
����˵���д������
A. �����в��������缫����ʯī��Ϊ����
B. ԭ����и����ĵ缫��ӦΪ��SO2+2H2O��2e��=SO42��+4H+
C. �ù����������ܷ�Ӧ�Ļ�ѧ����ʽ��ʾΪ��SO2+Br2+2H2O=2HBr+H2SO4
D. ���������յ��ŵ�Br2��ѭ�����ã�ԭ��ز����ĵ��ܿɳ�����ã����ܻ�������Դ
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com