
【题目】某同学利用如图装置探究SO2的性质. 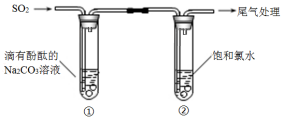
下列有关反应的方程式,不正确的是( )
A.①中溶液显红色的原因:CO32﹣+H2OHCO3﹣+OH﹣
B.①中溶液红色褪去的原因:2SO2+CO32﹣+H2O═CO2+2HSO3﹣
C.②中溶液显黄绿色的原因:Cl2+H2O═HCl+HClO
D.②中溶液黄绿色褪去的原因:SO2+Cl2+2H2O═H2SO4+2HCl
科目:高中化学 来源: 题型:
【题目】实验室用锌与稀硫酸反应制取氢气,欲使产生的速率加快,下列措施可行的是( )
A. 加水稀释B. 加少量NaOH溶液
C. 改用的浓硫酸D. 加入适量CuSO4溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸、硝酸和盐酸既是重要的化工原料也是化学实验室里必备的试剂.
(1)常温下,可用铝槽车装运浓硫酸,这是因为浓硫酸具有性;硝酸应保存在棕色试剂瓶中,这是因为硝酸具有性;敞口放置的浓盐酸浓度会减小,这是因为盐酸具有性.
(2)①在100mL 18molL﹣1的浓硫酸中加入过量的铜片,加热使之充分反应,产生的气体在标准状况下的体积为13.44L,则参加反应的铜片的质量为(选填序号);
a.115.2g b.76.8g c.57.6g d.38.4g
②若使上述①中反应剩余的铜片继续溶解,可向其中加入硝酸钠,写出反应的离子方程式: .
(3)工业制盐酸是以电解饱和氯化钠溶液为基础进行的,该电解过程中阳极的电极反应式为: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验过程如图所示,则图③试管中的现象是( ) 
A.铜片溶解,产生无色气体,该气体遇空气变为红棕色
B.铜片溶解,产生无色气体,该气体遇到空气不变色
C.铜片溶解,放出红棕色有刺激性气味的气体
D.无明显现象,因稀硫酸不与铜反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】砒霜的主要成分是As2O3,有剧毒,致死量为0.1 g。As2O3是两性偏酸性氧化物,微溶于水,生成H3AsO3;该酸及其对应的盐也均有毒性,其中碱金属对应的盐溶于水,其他金属对应的盐均几乎不溶于水。下列关于处理一瓶含有砒霜废液的方案正确的是( )
A.直接倒入下水道
B.经过滤后倒入下水道
C.加入足量生石灰后,倒入指定地点
D.加入足量氢氧化钠后,倒入指定地点
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有BaCl2和NaCl混合溶液aL,将它均分成两份。一份滴加硫酸,使Ba2+完全沉淀;另一份滴加AgNO3溶液,使Cl-完全沉淀.反应中消耗xmolH2SO4、ymolAgNO3 . 据此得知原混合溶液中的c(Na+)为( )
A.(2y-4x) /amol·L-1
B.(y-2x) /amol·L-1
C.(2y-2x) /amol·L-1
D.(y-x) /amol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将2.56g Cu和一定量的浓HNO3反应,随着Cu的不断减少,反应生成气体的颜色逐渐变浅,当Cu反应完毕时,共收集到气体1.12L(标准状况),则反应中消耗HNO3的物质的量为( )
A.0.05 mol
B.1 mol
C.1.05 mol
D.0.13 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某无色溶液里,只含有下列八种离子中的某几种:Mg2+、Na+、H+、Ag+、Cl﹣、 ![]() .已知该溶液能跟金属铝反应,且放出的气体只有氢气,试回答:
.已知该溶液能跟金属铝反应,且放出的气体只有氢气,试回答:
(1)若溶液跟Al反应后有[Al(OH)4]﹣生成,则原溶液一定含有大量的离子,还可能含有大量的离子.
(2)若溶液跟Al反应后有Al3+生成,则原溶液中一定不含有大量离子.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com