


 。请回答下列问题:
。请回答下列问题:


 字词句篇与同步作文达标系列答案
字词句篇与同步作文达标系列答案科目:高中化学 来源:不详 题型:单选题
| A.使用催化剂有利于加快合成氨反应的反应速率 |
| B.硫酸工业中,将黄铁矿粉碎后加入沸腾炉中 |
| C.500℃左右比在室温时更有利于提高合成氨的转化率 |
| D.配制氯化铁溶液时,将氯化铁加入盐酸中,然后加水稀释 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
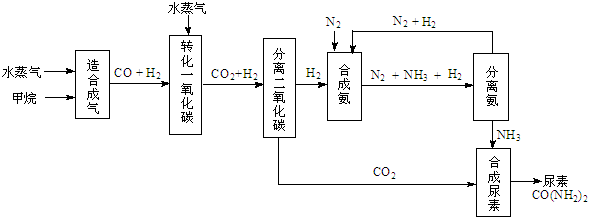
 CO(g)+3H2(g);△H>0
CO(g)+3H2(g);△H>0| 温度/℃ | 400 | 500 | 800 |
| 平衡常数K | 9.94 | 9 | 1 |
 H2(g)+CO2(g),该反应平衡常数随温度的变化如下:
H2(g)+CO2(g),该反应平衡常数随温度的变化如下:查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| 项目 | H2 | N2 | NH3 |
| 起始时 | 5 mol·L-1 | 3 mol·L-1 | 0 |
| 2 s末 | 2 mol·L-1 | | |

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.原电池负极被氧化 |
| B.任何化学反应都能设计成原电池 |
| C.化学反应的速率和限度均可通过改变化学反应条件而改变 |
| D.化学反应达到平衡状态时,只要条件不改变,各物质的浓度就不再改变 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 2NH3(g) ΔH=Q kJ·mol-1,能量变化如下图,回答下列问题:
2NH3(g) ΔH=Q kJ·mol-1,能量变化如下图,回答下列问题:
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 4NO(g)+6H2O(g) ΔH=-905.5 kJ·mol-1
4NO(g)+6H2O(g) ΔH=-905.5 kJ·mol-1 2N2(g)+6H2O(g) ΔH=-1267 kJ·mol-1
2N2(g)+6H2O(g) ΔH=-1267 kJ·mol-1
| A.升高温度,反应(ⅰ)和(ⅱ)的平衡常数均减小 |
| B.840 ℃后升高温度,反应(ⅰ)的正反应速率减小,反应(ⅱ)的正反应速率增大 |
| C.900 ℃后,NO产率下降的主要原因是反应(ⅰ)平衡逆向移动 |
| D.800 ℃左右时,氨的催化氧化主要按照(ⅰ)进行 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 2C(g)+ D(s) ,5 min后达到平衡。平衡时A为1.6mol,放出的热量为Q。在t0时刻,若从平衡体系中分离出四分之一的混合气体,新平衡体系中c(A)为0.6mol/L。
2C(g)+ D(s) ,5 min后达到平衡。平衡时A为1.6mol,放出的热量为Q。在t0时刻,若从平衡体系中分离出四分之一的混合气体,新平衡体系中c(A)为0.6mol/L。| 起始 n(A)/mol | 起始 n(B)/mol | 起始 n(C)/mol | 起始 n(D)/mol | 达到平衡时放出(或吸收)的热量 |
| 0 | 1.6 | 8 | 足量 | |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com