
【题目】新型冠状病毒对紫外线和热敏感,有些方法还是可以有效灭活病毒的,下列做法错误的是( )
A.56℃以上加热30min
B.95%的酒精
C.含氯消毒剂(如84消毒液)
D.过氧乙酸和氯仿等脂溶剂
科目:高中化学 来源: 题型:
【题目】将过氧化钠投入到氯化亚铁溶液中,可观察到的现象是( )
A. 最终生成白色沉淀 B. 最终生成红褐色沉淀
C. 最终出现灰绿色沉淀 D. 无变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题: 
(1)若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,则①电解池中X极上的电极反应式为 . 在X极附近观察到的实验现象是 . ②Y电极上的电极反应式为 .
③要使电解后溶液恢复到电解前的状态,则需加入(或通入) .
(2)如果要用电解方法精炼粗铜,电解液a选用CuSO4溶液,则: ①X电极的材料是 , 电极反应式为 .
②Y电极的材料是 , 电极反应式为 . (说明:杂质发生的电极反应不必写出)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】黄铜矿(CuFeS2)是重要的矿藏,以黄铜矿为原料生产碱式氯化铜和铁红(氧化铁)颜料的工艺流程如图所示。

(1)反应Ⅰ的离子方程式为_____________,该反应的氧化剂是________________。
(2)反应Ⅱ的离子方程式为_________________________。
(3)反应Ⅵ是在45~50℃的条件下进行的,写出该反应的化学方程式:__________________。
(4)碱式氯化铜有多种组成,可表示为Cua(OH)bClc·xH2O,为测定某碱式氯化铜的组成,某实验小组进行下列实验:
①称取样品9.30g,用少量稀HNO3溶解后配成100.00mL溶液A;
②取25.00mL溶液A,加入足量AgNO3溶液,得到AgCl固体1.435g;
③另取25.00mL溶液A,调节pH为4~5,用浓度为0.40mol·L-1的EDTA(Na2H2Y·2H2O)标准溶液滴定Cu2+(离子方程式为Cu2++H2Y2-=CuY2-+2H+),滴定至终点,消耗标准溶液50.00mL。通过计算确定该样品的化学式为___________(填化学式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列每组中各物质内既有离子键又有共价键的一组是( )
A.NaOH、H2SO4、(NH4)2SO4B.MgO、Na2SO4、NH4HCO3
C.Na2O2、KOH、Na2SO4D.HCl、Al2O3、MgCl2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室中常用氧化浓盐酸的方法制取氯气,实验装置如图所示:
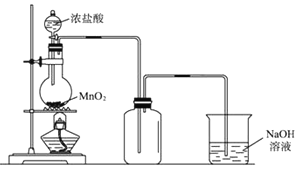
(1)写出制备氯气的离子方程式: ______ ;
(2)为了得到纯净、干燥的氯气,此装置还需增加净化装置,请根据气体的流动方向,依次按顺序选择所用的装置,正确的选项是 ______ ;
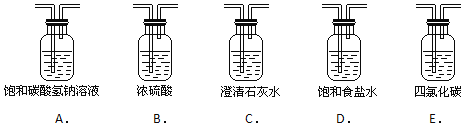
(3)如果将过量二氧化锰与20mL12mol/L的盐酸混合加热,充分反应后生成的氯气明显少于0.06mol,其主要原因有:① ______ ;② ______ .
(4)多余的氯气可以通过下列装置暂时储存后再利用,请选择可以用作氯气的储气的装置 ______ ;
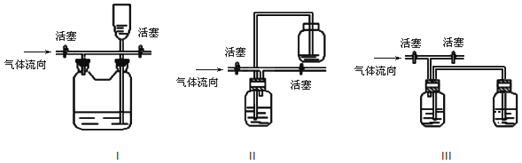
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是( )
A. 氯化钠可用于配制生理盐水 B. 二氧化硅可用于制造玻璃
C. 海水中的钠元素以单质存在 D. 氧化镁(熔点2 800 ℃)是优良的耐高温材料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[化学-选修3:物质结构与性质]铁氰化钾,化学式为K3[Fe(CN)6],主要应用于制药、电镀、造纸、钢铁生产等工业。其煅烧分解生成KCN、FeC2、N2、(CN)2等物质。
(1)基态K原子核外电子排布简写式为___________。 K3[Fe(CN)6]中所涉及的元素的基态原子核外未成对电子数最多的是_________,各元素的第一电离能由大到小的顺序为_________。
(2)(CN)2分子中存在碳碳键,则分子中σ键与π键数目之比为_______。KCN与盐酸作用可生成HCN,HCN的中心原子的杂化轨道类型为_________。
(3)CO能与金属Fe形成Fe(CO)5,该化合物熔点为253 K,沸点为为376 K,其固体属于_____晶体。
(4)下图是金属单质常见的两种堆积方式的晶胞模型。

①铁采纳的是a堆积方式.铁原子的配位数为_____,该晶体中原子总体积占晶体体积的比值为____(用含π的最简代数式表示)。
②常见的金属铝采纳的是b堆积方式,铝原子的半径为r pm,则其晶体密度为_____g·cm-3(用含有r、NA的最简代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】漂白液、漂白粉和漂粉精既可作棉、麻、纸张的漂白剂,又可用作游泳池及环境的消毒剂.它们在生产、生活中有广泛应用.某实验小组同学看到一则报道:某造纸厂误将槽车中漂白液(NaCl和NaClO的混合液,其中有效成分为NaClO)倒入盛放饱和KAl(SO4)2溶液的池中,造成中毒事件.该小组同学为探究中毒原因进行了如下实验.
(1)小组成员甲同学依据漂白液具有漂白消毒的性质推测,漂白液中ClO﹣具有氧化性.进行如下实验: Ⅰ.取10mL漂白液,依次加入Na2SO3溶液和BaCl2溶液,观察到有白色沉淀生成,经检验白色沉淀不溶于盐酸.
Ⅱ.另取10mL漂白液,加入品红溶液,发现溶液红色逐渐变浅,一段时间后褪为无色.
Ⅲ.再取10mL漂白液,加入品红溶液,加入少量稀硫酸酸化后,观察溶液红色立即变为无色.
①由实验Ⅰ得出ClO﹣具有氧化性,写出相关反应的离子方程式 .
②对比实验Ⅱ和Ⅲ说明ClO﹣氧化性与溶液酸碱性的关系是 .
(2)小组成员乙同学依据(1)中的实验提出:漂白液在酸性溶液中有Cl2生成,为此进行如下实验: 首先,他利用pH计分别测得漂白液pH>7,饱和KAl(SO4)2溶液pH<7.然后用下图1所示的装置继续实验,探究漂白液在酸性溶液中是否能反应生成Cl2 . 
①在测定漂白液pH的实验中,乙同学没有选择pH试纸的理由可能是;
②若打开分液漏斗活塞向烧瓶中加入硫酸,不久烧瓶中有黄绿色气体产生.A中反应的离子方程式 .
③若打开分液漏斗活塞向烧瓶中加入饱和KAl(SO4)2溶液,预计只有观察到以下现象 , 才能说明漂白液与酸性溶液混合会产生Cl2 .
(3)为了进一步了解漂白液生产和保存的实际意义,小组其他成员还研究漂白液的稳定性,他们查阅资料,下图是30℃时,pH=11的漂白液中NaClO的质量百分含量随时间变化图2: 
①分析分解速率v(Ⅰ)与v(Ⅱ)的大小关系,原因是
②4d~8d,Ⅰ中v(NaClO)=mol/(Ld)(常温下漂白液的密度约为1g/cm3 , 且溶液体积变化忽略不计,结果保留2位有效数字.)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com