
【题目】设NA表示阿伏加德罗常数的值,下列说法不正确的是
A. 4.0g氦气中含有的最外层电子数为4NA
B. 3.9g2H37Cl中含有的中子数为2.1NA
C. 标准状况下,11.2L丙烷中含有的非极性键数目为NA
D. 100mL1mol·L-1CH3COOH溶液中含有的分子数目大于0.1NA
科目:高中化学 来源: 题型:
【题目】滴定分数是指滴定过程中标准溶液与待测溶液中溶质的物质的量之比。用0.10mol·L-1NaOH溶液滴定0.10mol·L-1H2C2O4(草酸)溶液的滴定曲线如图所示。下列说法不正确的是( )
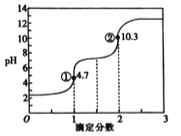
A. H2C2O4属于二元弱酸
B. 若用NaOH标准溶液滴定NaHC2O4溶液,可用酚酞作指示剂
C. 图中①处: c(Na+)+c(H+)=c(HC2O4-)+c(C2O42-)+c(OH-)
D. 图中②处:c(Na+)>c(C2O42-)>c(OH-)>c(HC2O4-)>c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将用导线连接的电极X、Y插入装有硫酸铜溶液的烧杯中(外电路中电子流向如图所示)。据此判断下列说法正确的是( )。
A.外电路中电流方向为X→Y
B.若电极材料分别为锌片和铜片,则Y为锌片
C.X极上发生还原反应
D.若电极材料都是金属,则金属活动性:X>Y
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示X、Y、Z、W均为短周期元素,它们在周期表中的相对位置如图所示。若X原子的最外层电子数是内层电子数的2倍,下列说法中正确的是 ( )
![]()
A. X 、Y对应的氧化物都是酸性氧化物
B. X的氧化物不能与Mg发生化学反应
C. Z比Y更容易与氢气化合
D. W与X形成的化合物中化学键类型为共价键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海洋中有丰富的食品、矿产、能源、药物和水产资源等(如下图所示),下列有关说法错误的是 ( )

A. 第①步除去粗盐S![]() 、Ca2+、Mg2+、Fe3+等杂质离子,加入的药品顺序为: BaCl2溶液→NaOH溶液→Na2CO3溶液→过滤后加盐酸
、Ca2+、Mg2+、Fe3+等杂质离子,加入的药品顺序为: BaCl2溶液→NaOH溶液→Na2CO3溶液→过滤后加盐酸
B. ②中海水淡化的方法主要有蒸馏法、电渗析法、离子交换法等
C. 在第③④⑤步中溴元素均被氧化
D. 第⑤步涉及的分离操作有萃取、蒸馏
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】溶液、胶体和浊液这三种分散系的根本区别是( )
A.是否是大量分子或离子的集合体 B.分散质粒子直径的大小
C.能否透过滤纸或半透膜 D.是否均一、稳定、透明
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:①2H2(g)+O2(g)=2H2O(l);△H=-572kJ/mol
②2H2(g)+O2(g)=2H2O(g);△H=-484kJ/mol
③CH4(g)+2O2(g)=2H2O(l)+CO2(g);△H=-890kJ/mol
(1)已知H-H的键能436kJ/molO=O的键能496kJ/molH-O的键能463kJ/mol,根据上述数据计算①②哪一个反应可以通过键能直接计算得出 。并计算写出反应 H2O ( l ) = H2O ( g )的焓变△H= 。
(2)请根据题干计算CO2(g)+4H2( g ) =CH4( g ) +2H2O( g )的焓变△H= 。
(3)在①②③三个方程式中哪一个是燃烧热的热化学方程式 。(填反应方程式的序号)标准状况下,取甲烷和氢气的混合气体11.2 L完全燃烧后恢复到常温,则放出的热量为263.8kJ,试求混合气体中甲烷和氢气体积比 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】升高温度时,化学反应速率加快,主要是由于
A. 分子运动速率加快,使反应物分子间的碰撞机会增多
B. 反应物分子的能量增加,活化分子百分数增大,有效碰撞次数增多,化学反应速率加快
C. 该化学反应的过程是放热的
D. 该化学反应的过程是吸热的
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com