
����Ŀ��ij��Ȼ�л�������A����C��H��OԪ�أ���A��صı仯���£����ַ�Ӧ��������ȥ����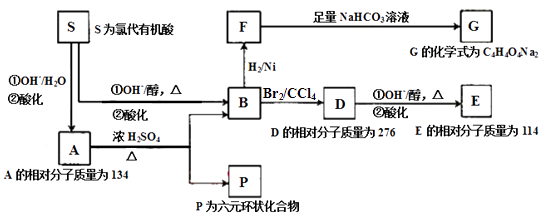
��1��������B�Ĺ����������� �� B��F�ķ�Ӧ����Ϊ ��
��2��д�����з�Ӧ�Ļ�ѧ����ʽ�����ӷ���ʽ��S��B�ĵڢٲ��� ��
A��P�� ��
D��E�ĵڢٲ��� ��
��3��nmol A�������۷�Ӧ���ɣ�n��1��molH2Oʱ��������״�����Ľṹ��ʽΪ
��4��д����D������ͬ�����ŵ�D������ͬ���칹��Ľṹ��ʽ�� ��
���𰸡�
��1��̼̼˫�����Ȼ����ӳɷ�Ӧ��ԭ��Ӧ
��2��HOOCCHClCH2COOH+3OH����OOCCH=CHCOO��+Cl��+3H2O��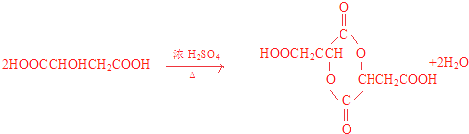 ��HOOCCHBrCHBrCOOH+4OH����OOCC��CCOO��+2Br��+4H2O
��HOOCCHBrCHBrCOOH+4OH����OOCC��CCOO��+2Br��+4H2O
��3��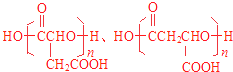
��4��![]()
���������⣺��A����C��H��O����Ԫ�أ�SΪ�ȴ��л��ᣬˮ����Եõ�A��˵��S�����к���C��H��O��Cl����Ԫ�أ����ݷ�Ӧ������֪����S��B������ȥ��B��F�����ӳɣ��õ���������F����F��NaHCO3��Ӧ���õ��εĻ�ѧʽΪ��C4H4O4Na2 �� ˵��F�Ƕ�Ԫ���ᣬ�Ӷ�˵��S�����к���������COOH��S�е�Clԭ�Ӽ��������±���OHȡ�������ɺ��Щ�COOH�ͩ�OH���л���A������A������Ũ���������£�����������Ԫ��״�������ʩ�OH�ڦ�̼ԭ���ϣ��ٽ��A����Է���������Ϊ134��������֪AΪHOOCCHOHCH2COOH��SΪ ![]() ��BΪHOOCCH=CHCOOH��FΪHOOCCH2CH2COOH��DΪ
��BΪHOOCCH=CHCOOH��FΪHOOCCH2CH2COOH��DΪ ![]() ��D��NaOH����Һ�з�����ȥ������E��HOOCC��CCOOH��PΪ��Ԫ�������ṹ��ʽΪ
��D��NaOH����Һ�з�����ȥ������E��HOOCC��CCOOH��PΪ��Ԫ�������ṹ��ʽΪ ![]() ����1��BΪHOOCCH=CHCOOH�������к���̼̼˫�����Ȼ����ֹ����ţ�B�����ӳɷ�Ӧ��ԭ��Ӧ����F�����Դ��ǣ�̼̼˫�����Ȼ����ӳɣ���ԭ����Ӧ����2��S��B�ĵڢٲ���HOOCCHClCH2COOH+3OH����OOCCH=CHCOO��+Cl��+3H2O��
����1��BΪHOOCCH=CHCOOH�������к���̼̼˫�����Ȼ����ֹ����ţ�B�����ӳɷ�Ӧ��ԭ��Ӧ����F�����Դ��ǣ�̼̼˫�����Ȼ����ӳɣ���ԭ����Ӧ����2��S��B�ĵڢٲ���HOOCCHClCH2COOH+3OH����OOCCH=CHCOO��+Cl��+3H2O��
A��P�� 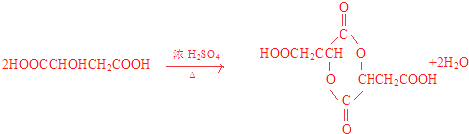 ��
��
D��E�ĵڢٲ���HOOCCHBrCHBrCOOH+4OH����OOCC��CCOO��+2Br��+4H2O��
���Դ��ǣ�HOOCCHClCH2COOH+3OH����OOCCH=CHCOO��+Cl��+3H2O�� ��
��
HOOCCHBrCHBrCOOH+4OH����OOCC��CCOO��+2Br��+4H2O����3��n mol A�������۷�Ӧ���ɣ�n��1��mol H2Oʱ��������״�����Ľṹ��ʽΪ 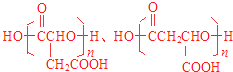 �����Դ��ǣ�
�����Դ��ǣ� 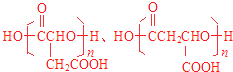 ����4����D������ͬ�����ŵ�D������ͬ���칹��Ľṹ��ʽΪ
����4����D������ͬ�����ŵ�D������ͬ���칹��Ľṹ��ʽΪ ![]() �����Դ��ǣ�
�����Դ��ǣ� ![]() ��
��


 ���Ž�������С״Ԫϵ�д�
���Ž�������С״Ԫϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ӷ���ʽ������ǣ� ��
A.�ù����������ᷴӦ�Ʊ��轺��SiO ![]() +2H+�TH2SiO3�����壩
+2H+�TH2SiO3�����壩
B.FeI2��Һ��ͨ������Cl2��2Fe2++Cl2�T2Fe3++2Cl��
C.����NaHSO4 ��Һ��Ba��OH��2 ��Һ��Ӧ��H++OH��+SO ![]() +Ba2+�TH2O+BaSO4��
+Ba2+�TH2O+BaSO4��
D.FeCl3��Һ��ͨ��SO2 �� ��Һ��ɫ��ȥ��2Fe3++SO2+2H2O�T2Fe2++SO ![]() +4H+
+4H+
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����500mLϡ�����м���һ�����������ۣ�������ȫ�ܽ�ų�NO����5.6L����״������ͬʱ��Һ��������9.3g�������ж���ȷ���ǣ� ��
A.ԭ��Һ��Ͷ���������ʵ�����0.25mol
B.ԭ��Һ�е�HNO3Ũ����2.0mol/L
C.��Ӧ�����Һ�л������ܽ�9.6gͭ
D.��Ӧ�����Һ��c��Fe2+����c��Fe3+��=1��2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʵ�鷽���п��е��ǣ� ��
A. �ó���ʯ��ˮ����CO���Ƿ���CO2
B. ��BaCl2��ȥNaOH��Һ�л��е�����Na2SO4
C. �þƾ��ѵ�ˮ�еĵ���ȡ����
D. ���ܽ⡢���˵ķ�������CaCl2��NaCl��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ������ ��
A. ��״���£�O2�����ԼΪ22.4 L
B. ��״���£�CO2������Ħ�����Ϊ22.4 L
C. ��״���£�0.5 mol��H2O�����ԼΪ11.2 L
D. 0��,101kPaʱ��1 mol O2��N2�Ļ������������ԼΪ22.4 L
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������Ա���š������ש�顱ʱ���й��Ա�Ѿ���̫���ݲ���,ÿ����װ�����ư�װ���У�עˮ���ü��������м��ȾͿ��Ժ��ˣ���Ҫ���������Է�ֹˮ��Ʈ����������˵����ȷ���ǣ� ��
���� | ����þ | �Ȼ�þ |
�۵�/�� | 2 852 | 714 |
A. �Ա�Ȳ�ʱע���H2O��Ħ��������18��
B. H2O+Cl2![]() HCl+HClO�ⷴӦ����������ԭ��Ӧ
HCl+HClO�ⷴӦ����������ԭ��Ӧ
C. �������ͬλ��1H��2D��3T��16Oֻ���γ�����ˮ����
D. �ڱ�״���£�1molˮ�����Լ��22��4L
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������װ���У�A��ʵ�����Ʊ�Cl2�ķ���װ�ã�Բ����ƿ��ʢ�ŵ��Ƕ������̣�C��DΪ���徻��װ�ã�EӲ�ʲ�������װ��ϸ��˿����FΪ����Ŀչ��ƿ���ձ�GΪβ������װ�á��Իش�
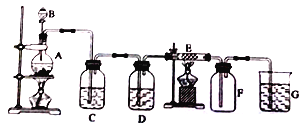
��1��Cװ�����Լ�Ϊ______��
��2��E�е�����Ϊ______��
��3��д����A��G�з�����Ӧ�����ӷ���ʽ��A�� ___________��G�� ________________��
��4��KMnO4�������Ա�MnO2ǿ�ö࣬ʵ����Ҳ������KMnO4�����Ũ���ᷴӦ��ȡ��������Ӧ����ʽ���£�2 KMnO4+16HCl(Ũ)=2KCl+2MnCl2+5Cl2��+8H2O��
�ٿ����á������š��������ת�Ƶķ������Ŀ: __________��
�ڸ÷�Ӧ�б�������δ��������HCl�����ʵ���֮����________�������20mL��12mol/L��Ũ����������KMnO4��ַ�Ӧ��ʵ�����ռ��������ڱ�״���µ����Ϊ_______��
A.��1.68L B.>1.68L C.��1.68L D.<1.68L
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ᣨD����һ����Ҫ��ҽҩ�м��壬��ͨ�����з����ϳɣ� 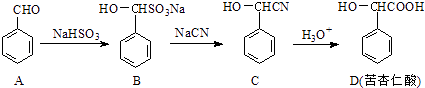
��A��B�ķ�Ӧ����Ϊ
��D������Ϊ�����������Ľṹ��ʽΪ
��E��D��ͬ���칹�壬E�к��б�������E�ܷ�������ˮ�ⷴӦ��E+H2O ![]() CH3OH+F����������F�Ľṹ�֣����к˴Ź���������4����������Ϊ1��2��2��1�Ľṹ��ʽΪ ��
CH3OH+F����������F�Ľṹ�֣����к˴Ź���������4����������Ϊ1��2��2��1�Ľṹ��ʽΪ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijС����ij�¶��²ⶨ��Һ��pHʱ���֣�0.01mol/L��NaOH��Һ�У�c��H+��c��OH����=10��12��mol/L��2 �� ���С���ڸ��¶��²��0.1mol/LNaOH��Һ��0.1mol/LHCl��ҺpHӦΪ�� ��
A.13��1
B.13��2
C.11��1
D.10��2
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com