
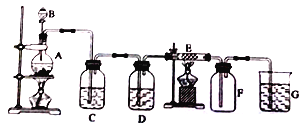
【题目】在下面的装置中,A是实验室制备Cl2的发生装置,圆底烧瓶中盛放的是二氧化锰,C、D为气体净化装置;E硬质玻璃管中装有细铁丝网;F为干燥的空广口瓶:烧杯G为尾气吸收装置。试回答:
(1)C装置中试剂为______。
(2)E中的现象为______。
(3)写出在A、G中发生反应的离子方程式:A: ___________。G: ________________。
(4)KMnO4的氧化性比MnO2强得多,实验室也可以用KMnO4固体和浓盐酸反应制取氯气,反应方程式如下:2 KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O。
①考试用“单线桥”标出电子转移的方向和数目: __________。
②该反应中被氧化和未被氧化的HCl的物质的量之比是________,如果将20mL、12mol/L的浓盐酸与足量KMnO4充分反应,实际能收集到氯气在标准状况下的体积为_______。
A.≥1.68L B.>1.68L C.≤1.68L D.<1.68L
【答案】 饱和食盐水 棕黄色的烟 Mn02+4H++2Cl-(浓) ![]() Mn2++Cl2↑+2H2O Cl2+2OH-=Cl-+ClO-+H2O
Mn2++Cl2↑+2H2O Cl2+2OH-=Cl-+ClO-+H2O  5:3 D
5:3 D
【解析】本题考查实验方案设计的评价,(1)装置A制取氯气,氯气中混有水蒸气和HCl,应先除去HCl,后除去水蒸气,除去氯气中的HCl,通过饱和食盐水,即装置C中盛放的是饱和食盐水;(2)装置E中发生铁和氯气的反应,产生棕黄色的烟;(3)装置A中制取氯气,离子反应方程式为MnO2+4H++2Cl-![]() Mn2++Cl2↑+2H2O,装置G的作用是吸收未反应的氯气,离子方程式为Cl2+2OH-=Cl-+ClO-+H2O;(4)①根据反应方程式,KMnO4中Mn的化合价降低,HCl中Cl的化合价升高,消耗2molKMnO4转移电子10e-,应从HCl中Cl出来,箭头指向KMnO4中Mn,即为
Mn2++Cl2↑+2H2O,装置G的作用是吸收未反应的氯气,离子方程式为Cl2+2OH-=Cl-+ClO-+H2O;(4)①根据反应方程式,KMnO4中Mn的化合价降低,HCl中Cl的化合价升高,消耗2molKMnO4转移电子10e-,应从HCl中Cl出来,箭头指向KMnO4中Mn,即为 ;②被氧化HCl的物质的量,看Cl2中Cl的物质的量,即被氧化的HCl物质的量为10mol,未被氧化HCl,看生成物中Cl-的物质的量,即未被氧化HCl的物质的量为6mol,因此两者的比值为10:6=5:3;假设HCl全部参加反应,根据反应方程式,生成氯气的体积为20×10-3×12×5×22.4/16L=1.68L,因为高锰酸钾溶液与浓盐酸反应,随着反应的进行,盐酸浓度变稀,到达某一浓度反应停止,产生Cl2的体积小于1.68L。
;②被氧化HCl的物质的量,看Cl2中Cl的物质的量,即被氧化的HCl物质的量为10mol,未被氧化HCl,看生成物中Cl-的物质的量,即未被氧化HCl的物质的量为6mol,因此两者的比值为10:6=5:3;假设HCl全部参加反应,根据反应方程式,生成氯气的体积为20×10-3×12×5×22.4/16L=1.68L,因为高锰酸钾溶液与浓盐酸反应,随着反应的进行,盐酸浓度变稀,到达某一浓度反应停止,产生Cl2的体积小于1.68L。


科目:高中化学 来源: 题型:
【题目】下表是某食品包装袋上的说明,从表中的配料中分别选出一种物质填在相应的横线上。

①富含蛋白质的物质是______________;
②富含糖类的物质是________________;
③富含油脂的物质是________________;
④富含维生素的物质是______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】保持洁净安全的生存环境已成为全人类的共识。
(1)某日空气中各种污染物的污染指数分别为:二氧化硫66,二氧化氮50,可吸入颗粒120。该地区的当日首要污染物是 。
(2)汽车尾气(含有烃类、CO、SO2与NO等物质)是城市的污染源。治理的方法之一是在汽车的排气管上装一个“催化转换器”(用铂、钯合金作催化剂)。它的特点是使CO与NO反应,生成无毒气体,并促使烃类充分燃烧及SO2的转化。写出CO与NO反应的化学方程式: 。
(3)pH< 的雨水称为酸雨;向煤中加入适量的 ,可以大大减少燃物产物中SO2的量。
(4)1998年我国长江流域发生百年一遇的洪水,洪水泛滥期间为解决灾民的饮用水问题,防疫人员向灾民发放明矾来净化河水。明矾的净水原理是 (用有关反应的离子方程式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知温度T时水的离子积常数为KW,该温度下,将浓度为a mol·L-1的一元酸HA与b mol·L-1的一元碱BOH等体积混合,可判定该溶液呈中性的依据是( )
A.a=b
B.混合溶液中,c(H+)= ![]() mol·L-1
mol·L-1
C.混合溶液中,c(H+)+c(B+)=c(OH-)+c(A-)
D.混合溶液的pH=7
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于电解质的说法正确的是( )
A.石墨、水银均能导电,所以它们是电解质
B.SO2溶于水能导电,所以SO2是电解质
C.BaSO4在水溶液中难导电,但熔融状态下能导电,所以BaSO4是电解质
D.导电能力强的是强电解质溶液,导电能力弱的是弱电解质溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用括号中的试剂及相应操作除去下列各组中的少量杂质,合理的一组是
A. 溴苯中的苯(NaOH溶液,分液) B. 乙醇中的水(新制的氧化钙,蒸馏)
C. 乙酸中的乙醇(金属钠,蒸馏) D. 苯中的甲苯(酸性高锰酸钾溶液,分液)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com