
【题目】已知X、Y、Z、W为短周期主族元素,在周期表中的相对位置如图,有下列说法:

①若HmXOn为强酸,则X的氢化物溶于水一定显酸性(m、n均为正整数)
②若四种元素均为金属,则Z的最高价氧化物对应的水化物一定为强碱
③若四种元素均为非金属,则W的最高价氧化物对应的水化物一定为强酸
④若四种元素只有一种为金属,则Z与Y的最高价氧化物对应的水化物一定为强酸。
其中正确的说法有几项( )
A. 1项 B. 2项 C. 3项 D. 4项
【答案】A
【解析】
X、Y、Z、W为短周期主族元素,由元素在周期表中的相对位置,可知X、Y处于第二周期,Z、W处于第三周期。
①若HmXOn为强酸,则X可为氮元素,其氢化物为氨气,水溶液呈碱性,故①错误;
②若四种元素均为金属,则X为![]() 、Z为Na、Y为Be、W为Mg,Z的最高价氧化物对应水化物为NaOH,属于强碱,故②正确;
、Z为Na、Y为Be、W为Mg,Z的最高价氧化物对应水化物为NaOH,属于强碱,故②正确;
③若四种元素均为非金属,X、Z至少处于ⅣA族,W可能为P、S或Cl,最高价氧化物对应的水化物中硫酸、高氯酸为强酸,而磷酸属于中强酸,故③错误;
④若四种元素只有一种为金属,则X为B、Z为Al、Y为C、W为Si,Z、Y二者的最高价氧化物对应的水化物分别为氢氧化铝、碳酸,二者都不是强酸,故④错误。
故正确的只有②,故选A。
综上所述,本题正确答案为A。


科目:高中化学 来源: 题型:
【题目】实验室制取乙烯的反应原理为:CH3CH2OH![]() CH2=CH2↑+H2O,选用下图A进行反应。但常因温度过高而使乙醇和浓硫酸生成少量的二氧化硫。有人设计下列实验以确认上述混合气体中存在乙烯和二氧化硫,试回答下列问题。
CH2=CH2↑+H2O,选用下图A进行反应。但常因温度过高而使乙醇和浓硫酸生成少量的二氧化硫。有人设计下列实验以确认上述混合气体中存在乙烯和二氧化硫,试回答下列问题。
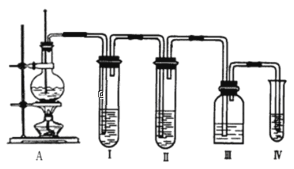
(1)将下列所给的试剂中选出所必需的试剂,按气流方向从左到右依次是:______(可重复,填字母)。
A.品红溶液 B.NaOH溶液 C.浓H2SO4 D.溴水
(2)能说明二氧化硫气体存在的现象是______。
(3)使用装置Ⅲ的目的是______。
(4)确定含有乙烯的现象是______。
(5)写出IV中发生的化学反应方程式______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属镍与铁,钴相似,在常温下对水和空气都较稳定,能抗碱性腐蚀。常温下,镍即可与一氧化碳反应,形成剧毒的四羰基镍(Ni(CO)4),加热后它又会分解成金属镍和—氧化碳。工业上用含废镍废料(含有铝、铁和有机物)为原料制备兰尼镍的工艺流程如图所示:
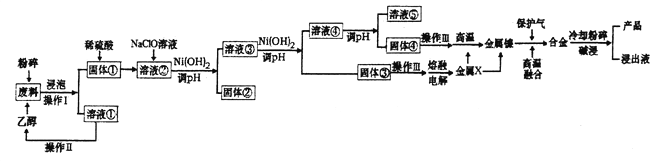
已知:25℃时Ni(OH)2的Ksp=5.4×10-16;Al(OH)3的Ksp=3.0×10-34.
(1)若将NaOH固体进行高温熔融,可选择的坩埚为_________。
a.铁坩埚 b.氧化铝坩埚 c.石英坩埚 d.镍坩埚
(2)操作Ⅱ的名称为__________;实验室中在进行操作III时,仪器除酒精灯、坩埚、三脚架外还缺______________。
(3)加入NaC1O溶液时发生反应的离子反应方程式______________________________。
(4)固体④经操作III得到NiO。合金中铝和镍的物质的量之比为2:3,则前后两份金属铝用量的最佳配比为________________。
(5)25℃时,若测得溶液⑤pH=9,该溶液中c(Ni2+)/c(A13+)=__________。
(6)将金属X与金属镍进行高温融合时,可否用CO做保护气,请说明原因_________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于NO和NO2的叙述正确的是( )
A.NO是一种红棕色气体
B.常温常压下,NO不能与空气中的氧气直接化合
C.含等质量的氧元素的NO和CO的物质的量相等
D.NO2可用排水法收集
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求回答问题:
(1)除去下列表格物质中的杂质(括号中是杂质),从所给试剂及操作方法中选出合适的药品及方法(填序号):
除杂试剂:A.溴水 B.饱和碳酸钠溶液 C.氢氧化钠溶液 D.乙醇
操作方法:E.蒸馏 F.分液 G.洗气 H.萃取
物质(括号中是杂质) | 除杂试剂 | 操作方法 |
①硝基苯(硝酸) | _____ | _____ |
②乙酸乙酯(乙酸) | _____ | _____ |
③甲烷(乙烯) | _____ | _____ |
(2)①乙酸中官能团的名称是__________________。
②工业上用乙烯水化法制备乙醇,反应的化学方程式是______________。
③红热的铜丝插入乙醇中反复几次发生反应,反应的化学方程式是______________,该反应类型为___________反应。
④丁烷有___________种同分异构体,其中___________(写名称)熔、沸点较低。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属(M)–空气电池(如图)具有原料易得、能量密度高等优点,有望成为新能源汽车和移动设备的电源。该类电池放电的总反应方程式为:4M+nO2+2nH2O=4M(OH) n。已知:电池的“理论比能量”指单位质量的电极材料理论上能释放出的最大电能。下列说法不正确的是

A. 采用多孔电极的目的是提高电极与电解质溶液的接触面积,并有利于氧气扩散至电极表面
B. 比较Mg、Al、Zn三种金属–空气电池,Al–空气电池的理论比能量最高
C. M–空气电池放电过程的正极反应式:4Mn++nO2+2nH2O+4ne–=4M(OH)n
D. 在Mg–空气电池中,为防止负极区沉积Mg(OH)2,宜采用中性电解质及阳离子交换膜
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列6种符号回答问题:①1H ②2H ③3H ④14C ⑤14N ⑥16O
(1)共有_______种核素,属于_______种元素。
(2)互为同位素的是____________。(填序号,下同)
(3)质量数相等的是______________,中子数相等的是_________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com