
【题目】下列关于NO和NO2的叙述正确的是( )
A.NO是一种红棕色气体
B.常温常压下,NO不能与空气中的氧气直接化合
C.含等质量的氧元素的NO和CO的物质的量相等
D.NO2可用排水法收集
 开心练习课课练与单元检测系列答案
开心练习课课练与单元检测系列答案 开心试卷期末冲刺100分系列答案
开心试卷期末冲刺100分系列答案 双基同步导航训练系列答案
双基同步导航训练系列答案科目:高中化学 来源: 题型:
【题目】正盐A、B均含三种元素,且所含元素种类相同。A在加热条件下发生如下变化。已知,气体D能使带火星的木条复燃。透过蓝色钴玻璃,A、B、C的焰色反应均为紫色。往C的溶液中加入AgNO3溶液,出现白色沉淀,再加入稀硝酸,沉淀不溶解,且沉淀质量为14.35 克。请回答:
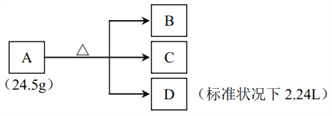
(1)C 的化学式为___________。
(2)写出 A 分解的化学方程式___________。
(3)将A与C混合,再加入稀硫酸,有气体产生,用离子方程式表示发生的反应___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CO2的大量排放不仅会造成温室效应还会引起海水中富含二氧化碳后酸度增加,可能会杀死一些海洋生物,甚至会溶解掉部分海床,从而造成灾难性的后果。所以二氧化碳的吸收和利用成为当前研究的重要课题。
(1)工业上以CO2与H2为原料合成甲醇,再以甲醇为原料来合成甲醚。
已知:CO2(g)+3H2(g)CH3OH(g)+H2O(g) △H1
2CH3OH(g)CH3OCH3(g)+H2O(g) △H2=-24.5 kJmol﹣1
2CO2(g)+6H2(g) CH3OCH3(g)+3H2O(g) △H3=-122.5 kJmol﹣1
甲醇的电子式为________________;△H1=________kJ·mol-1
(2)某科研小组探究用活性炭处理汽车尾气的可行性,在T1℃体积为2L的恒温密闭容器中进行了实验,并根据实验数据绘制了如下图像,其中X代表NO浓度变化,Y代表N2和CO2浓度变化:
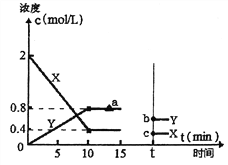
①若15min,后升高到一定温度,达到新平衡后容器中N2、CO2、NO的浓度之比为1:1:3,到达到新平衡时CO2的反应速率与图中a点相比较,速率_____(填“增大”、“减小”或“不变”),此时平衡常数K与T1℃相比_______(填“增大”、“减小”或“不变”)。②T1℃时该反应的平衡常数为_________________。
③如上图所示,若15min后改变了一个条件,t时刻建立新的平衡,b点坐标(0.6,t),c点坐标(0.3,t)。则改变的条件可能是_______(填序号)。
a.扩大容器体积 b.升高温度 c.使用合适催化剂 d.移走部分NO
(3)已知:H2CO3的电离常数Ka1=4.4×10-7,Ka2=5×10-11。25℃时若用1L 1mol· L-1的NaOH溶液吸收CO2,当溶液中c(CO32-):c(H2CO3)=2200,此时该溶液的pH值为________________。
(4)以熔融K2CO3为电解质的甲醚燃料电池,具有能量转化率高,储电量大等特点,则该电池的负极电极反应式为______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列指定反应的离子方程式正确的是
A. 向MgCl2溶液中滴加过量氨水:Mg2++2OH-=Mg(OH)2↓
B. 用稀硝酸洗涤试管内壁的银镜:Ag+4H++NO![]() =Ag++NO↑+2H2O
=Ag++NO↑+2H2O
C. 将Cu粉加入到Fe2(SO4)3溶液中:2Fe3++3Cu=2Fe+3Cu2+
D. 向NaAlO2溶液中通入过量CO2:AlO![]() +CO2+2H2O=Al(OH)3↓+HCO
+CO2+2H2O=Al(OH)3↓+HCO![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某科学家利用二氧化铈(CeO2)在太阳能作用下将H2O、CO2转变成H2、CO。其过程如下:
mCeO2![]() (m-x)CeO2·xCe+xO2(m-x)CeO2·xCe+xH2O+ xCO2
(m-x)CeO2·xCe+xO2(m-x)CeO2·xCe+xH2O+ xCO2![]() mCeO2+ xH2+ xCO
mCeO2+ xH2+ xCO
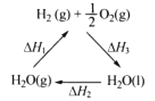
下列说法不正确的是
A. 该过程中CeO2没有消耗
B. 该过程实现了太阳能向化学能的转化
C. 右图中△H1=△H2+△H3
D. 以CO和O2构成的碱性燃料电池的负极反应式为CO+4OH——2e—=CO32-+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知X、Y、Z、W为短周期主族元素,在周期表中的相对位置如图,有下列说法:

①若HmXOn为强酸,则X的氢化物溶于水一定显酸性(m、n均为正整数)
②若四种元素均为金属,则Z的最高价氧化物对应的水化物一定为强碱
③若四种元素均为非金属,则W的最高价氧化物对应的水化物一定为强酸
④若四种元素只有一种为金属,则Z与Y的最高价氧化物对应的水化物一定为强酸。
其中正确的说法有几项( )
A. 1项 B. 2项 C. 3项 D. 4项
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】阅读下面的短文,回答问题。
聚碳酸酯(PC)是一类碳酸的聚酯,是一种强韧的热塑性树脂,耐弱酸,耐弱碱,耐中性油,不耐强碱,有阻燃性。其光学性能接近有机玻璃(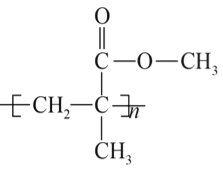 ),在透明建筑板材、电子电器、光盘媒介、汽车工业等领域有广泛应用。碳酸本身并不稳定,但其衍生物,如碳酸二苯酚酯、光气等有一定稳定性。工业上以碳酸的衍生物和双酚A为原料合成聚碳酸酯(PC),反应如下:
),在透明建筑板材、电子电器、光盘媒介、汽车工业等领域有广泛应用。碳酸本身并不稳定,但其衍生物,如碳酸二苯酚酯、光气等有一定稳定性。工业上以碳酸的衍生物和双酚A为原料合成聚碳酸酯(PC),反应如下:
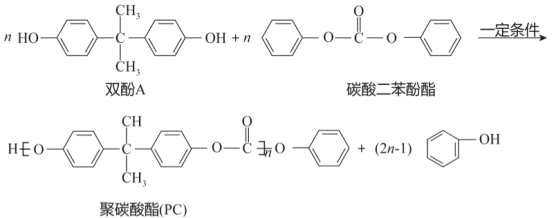
(1)下列说法正确的是_______(填序号)。
a.光气比碳酸稳定
b.聚碳酸酯能和强碱发生反应
c.聚碳酸酯易燃
d.聚碳酸酯是一种强韧的热塑性树脂
(2)双酚A和光气(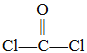 )也可发生类似的缩聚反应,生成一种聚碳酸酯。该反应的化学方程式是___________________________________________________。
)也可发生类似的缩聚反应,生成一种聚碳酸酯。该反应的化学方程式是___________________________________________________。
(3)有机玻璃的单体的结构简式是___________________________________________。在一定条件下,有机玻璃和NaOH溶液能发生反应,该反应的化学方程式是_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关物质用途的说法合理的是( )
A. Si可用于制造太阳能电池
B. 液氨可用作制冷剂
C. 聚氯乙烯可用于制食品包装袋
D. 漂白粉可用于杀菌消毒
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,有甲、乙两份体积均为1L、浓度均为0.1mol·L-1的醋酸溶液,其pH为3,①甲用蒸馏水稀释到100L时,溶液的pH变为x;②乙与等体积、浓度为0.2mol·L-1的NaOH溶液混合,在混合液中:n(CH3COO-)+n(OH-)-(H+)=y mol。x、y的正确答案组合为
A. 3<x<5、0.2 B. 3<x<5、0.1 C. 3、0.1 D. 5、0.2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com