
【题目】化学电源在日常生活和高科技领域中都有广泛应用。
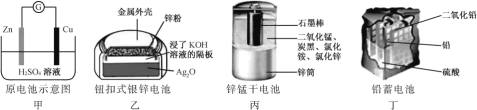
下列说法不正确的是( )
A. 甲:Zn2+向Cu电极方向移动,Cu电极附近溶液中H+浓度增加
B. 乙:正极的电极反应式为Ag2O+2e+H2O2Ag+2OH
C. 丙:锌筒作负极,发生氧化反应,锌筒会变薄
D. 丁:电池放电过程中,硫酸浓度不断减少。
科目:高中化学 来源: 题型:
【题目】25℃时,在1L的密闭容器中充入NO2发生如下反应:2NO2(g)![]() N2O4(g)△H=-57 kJ·mol-1(N2O4在25℃时为无色气体)。
N2O4(g)△H=-57 kJ·mol-1(N2O4在25℃时为无色气体)。
(1)该反应的ΔS__________0(填“>”、“<”或“=”)。
(2)当开始充入0.03mol的NO2时,25℃时,实验测得NO2的平衡浓度为0.01 mol·L-1,则NO2的平衡转化率(α)是_____________。25℃时上述反应的平衡常数K =_________。
(3)25℃时,实验测得该反应的活化能Ea=92.4 kJ·mol-1。下列能量关系图合理的是_____。
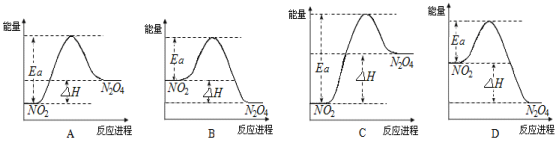
(4)如把该密闭容器放入80℃的热水中,则气体的颜色___________(填“不变”、“加深”或“变浅”),NO2的转化率___________(填“增大”、“不变”或“减小”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】肼(N2H4)分子中所有原子均达到稀有气体原子的稳定结构,它的沸点高达113℃,已知肼的球棍模型如图所示,下列有关说法不正确的是
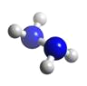
A. 肼是由极性键和非极性键构成的非极性分子
B. 肼沸点高达113℃,可推测肼分子间能形成氢键
C. 肼分子中N原子采用sp2杂化方式
D. 32g肼分子中含有5NA个σ键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】石墨烯(如图a)是一种由单层碳原子构成的平面结构新型碳材料,石墨烯中部分碳原子被氧化后,其平面结构会发生改变,转化为氧化石墨烯(如图b)。
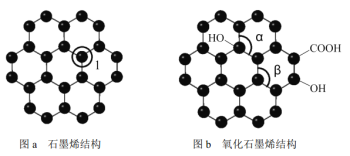
(1)图a中,1号C与相邻C形成σ键的个数为___________,该C原子杂化方式是______;图b中键角α_________键角β。(填“>” 、 “<” 或“=” )
(2)若将图乙所示的氧化石墨烯分散在H2O中,则氧化石墨烯中可与H2O形成氢键的原子有_______(填元素符号)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】醇脱水是合成烯烃的常用方法,实验室合成环己烯的反应和实验装置如下:
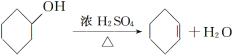

可能用到的有关数据如下:
相对分子质量 | 密度/(g·cm-3) | 沸点/℃ | 溶解性 | |
环己醇 | 100 | 0.961 8 | 161 | 微溶于水 |
环己烯 | 82 | 0.810 2 | 83 | 难溶于水 |
合成反应:在a中加入20 g环己醇和2小片碎瓷片,冷却搅动下慢慢加入1 mL浓H2SO4,b中通入冷却水后,开始缓慢加热a,控制馏出物的温度不超过90 ℃。
分离提纯:反应粗产物倒入分液漏斗中分别用少量5%碳酸钠溶液和水洗涤,分离后加入无水氯化钙颗粒,静置一段时间后弃去氯化钙,最终通过蒸馏得到纯净环己烯10 g。
回答下列问题:
(1)装置b的名称是__________。
(2)本实验中最容易产生的副产物的结构简式为_______。
(3)在本实验分离过程中,产物应该从分液漏斗的_______(填“上口倒出”或“下口放出”)。
(4)分离提纯过程中加入无水氯化钙的目的是______。
(5)在环己烯粗产物蒸馏过程中,不可能用到的仪器有____(填正确答案标号)。
A 圆底烧瓶 B 温度计 C 吸滤瓶 D 球形冷凝管 E 接收器
(6)以下区分环己烯精品和粗品的方法,合理的是______。
a.用酸性高锰酸钾溶液 b.用金属钠 c.测定沸点
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮、硫、碳的氧化物都会引起环境问题,越来越引起人们的重视。如图是氮、硫元素的各种价态与物质类别的对应关系:
(1)根据A对应的化合价和物质类别,A为___________(写分子式),从氮元素的化合价能否发生变化的角度判断,图中既有氧化性又有还原性的化合物有____________。
(2)浓、稀硝酸的性质既相似又有差别,若要除去铁制品表面的铜镀层应选择________,反应的离子方程式为______________。
(3)某同学设计了如图所示的套管实验装置(部分装置未画出)来制备SO2并利用实验现象来检验其还原性,制备SO2时选用的试剂为Cu和浓H2SO4。回答下列问题:

①写出制取SO2的化学方程式:_______________。
②该同学利用实验现象来检验SO2的还原性,则选用的试剂为_____。
A. 品红溶液 B. 酸性高锰酸钾溶液 C. 双氧水(H2O2)
(4)工厂里常采用NaOH溶液吸收NO、NO2的混合气体,使其转化为化工产品NaNO2,试写出其化学反应方程式_______。
(5)工业上把海水先进行氧化,再吸收溴,达到富集溴的目的。吸收工艺常用的方法是先用热空气吹出Br2,再用SO2吸收Br2。取吸收后的溶液,向其中加入氯化钡溶液有白色沉淀析出。写出SO2吸收Br2反应的化学方程式为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,取一定量的PbI2固体配成饱和溶液 ,T时刻改变某一条件,离子的浓度变化如图所示,(注:第一次平衡时c(I-)=2x10-3mol/L, c(Pb2+)=1x10-3mol/L)下列有关说法正确的是

A.常温下,Ksp=2x10-6
B.温度不变,向PbI2饱和溶液中加入少量硝酸铅浓溶液,PbI2的溶解度不变,c(Pb2+)不变
C.T时刻改变的条件是升高温度,PbI2的,Ksp 增大
D.常温下Ksp[PbS]=8x10-28,向PbI2的悬浊液中加入Na2S溶液,PbI2(s)+S2-(aq)![]() PbS(s)+2I-(aq)反应的化学平衡常数为5x1018
PbS(s)+2I-(aq)反应的化学平衡常数为5x1018
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于有机物的说法正确的是
A.分子式为C5H10O2,且属于酯的同分异构体共有9种(不考虑立体异构)
B.环己烯(![]() )分子中的所有碳原子共面
)分子中的所有碳原子共面
C.乙醇和丙三醇互为同系物
D.二环己烷( ![]() )的一氯代物有3种结构(不考虑立体异构)
)的一氯代物有3种结构(不考虑立体异构)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com