
【题目】材料的不断发展可以促进社会进步:
(1)玻璃是常见的硅酸盐产品,制玻璃发生的主要反应为_________,__________。
(2)钢化玻璃是一种常见的玻璃产品,其主要成分为_______________。
我们看到的玻璃,一般都呈淡绿色,只是因为原料中混有____________。
(3)插座也是一种塑料,它有绝缘性好,耐热,抗水等优点。它属于热____性塑料。
科目:高中化学 来源: 题型:
【题目】用惰性电极电解200mL KCl和CuSO4的混合溶液,经过一段时间后两极分别得到11.2L(标准状况下)气体。原混合溶液中KCl的物质的量浓度不可能为
A. 5mol/L B. 4mol/L C. 2.5mol/L D. 1mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:H2(g)+Cl2(g)![]() 2HCl(g)的反应能量变化示意图如下。下列说法不正确的是
2HCl(g)的反应能量变化示意图如下。下列说法不正确的是

A. 键的断裂过程是吸热过程,键的形成过程是放热过程
B. “假想的中间物质”的总能量高于起始态H2和Cl2的总能量
C. 反应的△H=[(a+b)-2c]kJ/mol
D. 点燃条件和光照条件下,反应的△H不同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数,下列叙述正确的是( )
A. 64 g SO2含有氧原子数为1NA
B. 物质的量浓度为0.5 mol·L-1的MgCl2溶液,含有Cl-数为1 NA
C. 标准状况下,22.4 L H2O的分子数为1NA
D. 常温常压下,14 g N2含有分子数为0.5 NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有金属单质A、B和气体甲、乙(黄绿色气体)、丙及物质C 、D、E、F、G,它们之间能发生如下反应(图中有些反应的产物和反应的条件没有全部标出)。
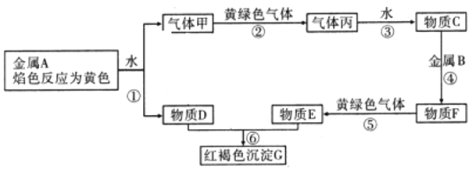
请根据以上信息回答下列问题:
(1)写出下列物质的化学式:A_______、B_______、G ________
(2)写出反应①的化学方程式__________________________________;反应⑤的离子方程式 ____________________________________;
(3)检验物质E的阳离子可以滴加KSCN,现象为_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】阿司匹林的结构简式如右图: 
根据这一信息,回答下列问题:。
(1) 写出阿司匹林的分子式:______________________________________
(2) 根据结构,推测阿司匹林的性质,下列试剂中,不能与阿司匹林反应的是 (_______)
A、氢氧化钠溶液 B、硫酸钠溶液 C、碳酸钠溶液 D、稀硫酸
(3) 阿司匹林是一种人工合成药物,化学上用水杨酸与乙酸酐(CH3CO)2O反应来制取阿司匹林。请用化学反应方程式表示这个过程:__________________________________________________________
(4)阿司匹林与NaOH反应可以得到可溶性钠盐,有比阿司匹林更好的疗效。请写出此反应的方程式:__________________________________________________________
(5) 有四种常见药物 ①阿司匹林 ②青霉素 ③胃舒平 ④麻黄碱。请回答:
①某同学胃酸过多,应选用的药物是________(填序号)。
抗酸药是治疗胃酸过多的一类药品,请写出一种抗酸药与胃酸反应的化学方程式:_________________________________________________________
②由于具有兴奋作用,国际奥委会严禁运动员服用的药物是________(填序号)。
③从用药安全角度考虑,使用前要进行皮肤敏感性测试的药物是________(填序号)。
④滥用药物会导致不良后果,如过量服用________(填序号)会出现水杨酸中毒,应立即停药,并静脉注射NaHCO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于Fe(OH)3胶体的叙述中,正确的是( )
A. 制备Fe(OH)3胶体的化学方程式是FeCl3+3H2O![]() Fe(OH)3↓+3HCl
Fe(OH)3↓+3HCl
B. 在制备Fe(OH)3胶体的实验中,加热煮沸时间越长,越有利于胶体的生成
C. Fe(OH)3胶体微粒能吸附阳离子,从而使Fe(OH)3胶体带有一定电荷
D. Fe(OH)3胶体能够吸附水中悬浮的固体颗粒并沉降,达到净水目的
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】标准状况下,将a L H2和Cl2的混合气体点燃,充分反应后,将混合气体通入含b mol NaOH的热溶液中,气体恰好被完全吸收,NaOH无剩余,测得反应后溶液中含Cl-、ClO-、![]() ,且三者物质的量之比为8∶1∶1,则原混合气体中H2的物质的量为( )
,且三者物质的量之比为8∶1∶1,则原混合气体中H2的物质的量为( )
A. ![]() mol B.
mol B. ![]() mol C.
mol C. ![]() mol D.
mol D. ![]() mol
mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有前四周期A,B,C,D,E、X六种元素,已知B,C,D,E、A五种非金属元素原子半径依次减小,其中B的s能级上电子总数等于p能级上电子总数的2倍.X原子的M能层上有4个未成对电子.请回答下列问题:
(1)写出C,D,E三种原子第一电离能由大到小的顺序为__。
(2)A原子与B,C,D原子形成最简单化合物的稳定性由强到弱的顺序为__,根据价层电子对互斥理论预测BA2D的分子构型为__。
(3)某蓝色晶体,其结构特点是X2+、X3+离子分别占据立方体互不相邻的顶点,而立方体的每条棱上均有一个BC﹣.与A同族且相差两个周期的元素R的离子位于立方体的恰当位置上,根据其结构特点可知该晶体的化学式为____(用最简正整数表示)。
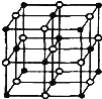
(4)科学家通过X射线探明,KCl、MgO、CaO、TiN的晶体结构与NaCl的晶体结构相似(如右图所示),其中3种离子晶体的晶格能数据如下表:

根据表格中的数据:判断KCl、MgO、TiN 三种离子晶体熔点从高到低的顺序是__,MgO晶体中一个Mg2+周围和它最邻近且等距离的O2﹣有__个。
(5)研究物质磁性表明:金属阳离子含未成对电子越多,则磁性越大,磁记录性能越好,离子型氧化物V2O5和Cr2O3中,适合作录音带磁粉原料的是__。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com