
| A.③④⑤⑦⑧⑨ | B.③⑥⑦⑧ | C.③⑥⑦⑧⑨ | D.①②③④⑤⑥⑦⑧⑨ |


 应用题天天练四川大学出版社系列答案
应用题天天练四川大学出版社系列答案科目:高中化学 来源:不详 题型:填空题
| 元素代号 | L | M | Q | R | T |
| 原子半径/nm | 0.160 | 0.143 | 0.112 | 0.104 | 0.066 |
| 主要化合价 | +2 | +3[ | +2 | +6、-2 | -2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.元素周期表中有8个主族 | B.稀有气体元素原子的最外层电子数均为8个 |
| C.碳元素位于第二周期ⅣA族 | D.ⅠA族全是金属元素 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

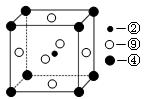


查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.Z是酸酐,但它不和水反应 | B.Z是一种碱性氧化物 |
| C.Z的化学式可能为X2Y5 | D.Z熔化时破坏化学键 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
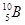 和
和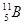 两种同位素构成的。已知5.4克晶体硼(B)全部氢化生成B2H6 (硼烷)气体时,可得标准状况下5.6L硼烷,则晶体硼中
两种同位素构成的。已知5.4克晶体硼(B)全部氢化生成B2H6 (硼烷)气体时,可得标准状况下5.6L硼烷,则晶体硼中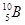 和
和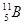 两种核素的原子个数比是
两种核素的原子个数比是查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.H2SeO3 | B.HMnO4 | C.H3BO3 | D.H3PO4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com