
【题目】根据乙烯的性质回答下列问题:
(1)在空气中点燃乙烯,观察到现象是____________________________________________。
(2)乙烯燃烧的化学方程式是____________________________________________________。
(3)与甲烷相比较,乙烯燃烧有较浓的黑烟的原因是_____________________________。
【答案】火焰明亮,伴有黑烟,同时放出大量热 C2H4+3O2![]() 2CO2+2H2O 乙烯的含碳量(85.7%)大于甲烷的含碳量(75%),易不完全燃烧,产生碳的黑色小颗粒
2CO2+2H2O 乙烯的含碳量(85.7%)大于甲烷的含碳量(75%),易不完全燃烧,产生碳的黑色小颗粒
【解析】
(1)乙烯具有可燃性,在空气中燃烧火焰明亮,伴有黑烟。
(2)乙烯燃烧生成二氧化碳和水;
(3). 乙烯的含碳量(85.7%)大于甲烷的含碳量(75%);
(1)乙烯具有可燃性,在空气中燃烧的现象是火焰明亮,伴有黑烟,同时放出大量热。
(2)乙烯燃烧生成二氧化碳和水,反应的方程式是C2H4+3O2![]() 2CO2+2H2O;
2CO2+2H2O;
(3). 乙烯的含碳量(85.7%)大于甲烷的含碳量(75%),不完全燃烧,产生碳的黑色小颗粒。


 作业辅导系列答案
作业辅导系列答案 同步学典一课多练系列答案
同步学典一课多练系列答案 经典密卷系列答案
经典密卷系列答案 金牌课堂练系列答案
金牌课堂练系列答案科目:高中化学 来源: 题型:
【题目】常温下,分别取浓度不同、体积均为20.00 mL的3种HCl溶液,分别滴入浓度为1.0001mol/L、0.1000 mol/L和0.01000 mol/L的NaOH溶液,测得3个反应体系的pH随V(NaOH)变化的曲线如图。在V(NaOH)=20.00 mL前后pH出现突跃。下列说法不正确的是
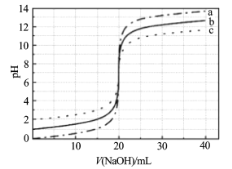
A.曲线a、b、c对应的c(HCl):a=100c
B.曲线a、b、c对应的c(NaOH):a>b>c
C.当V(NaOH)=20.00 mL时,3个体系中均满足:c(Na+)=c(Cl-)
D.当V(NaOH)相同时,pH突跃最大的体系中的c(H+)最大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氧化碳的捕集、利用是我国能源领域的一个重要战略方向。
(1)科学家提出由CO2制取C的太阳能工艺如图所示。

①若“重整系统”发生的反应中n(FeO)/n(CO2)=6,则FexOy的化学式为____________。
②“热分解系统”中每分解1mol FexOy,转移电子的物质的量为________。
(2)工业上用CO2和H2反应合成二甲醚。已知:CO2(g)+ 3H2(g)═CH3OH(g)+ H2O(g) △H1=-53.7kJ/mol,CH3OCH3(g)+H2O(g) ═ 2CH3OH(g) △H2=+23.4kJ/mol,则2CO2(g)+ 6H2(g)![]() CH3OCH3(g)+3H2O(g) △H3=______kJ/mol。
CH3OCH3(g)+3H2O(g) △H3=______kJ/mol。
①一定条件下,上述合成甲醚的反应达到平衡状态后,若改变反应的某一个条件,下列变化能说明平衡一定向正反应方向移动的是_____(填代号)。
a.逆反应速率先增大后减小 b.H2的转化率增大
c.反应物的体积百分含量减小 d.容器中的nCO2/nH2值变小
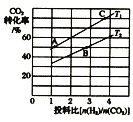
②在某压强下,合成甲醚的反应在不同温度、不同投料比时,CO2的转化率如图所示。T1温度下,将6 mol CO2和12molH2充入2L的密闭容器中,5 min后反应达到平衡状态,则0~5min内的平均反应速率v(CH3OCH3) =___;KA、KB、KC三者之间的大小关系为_____。
(3)常温下,用氨水吸收CO2可得到NH4HCO3溶液,在NH4HCO3溶液中:c (NH4+)_____c(HCO3-)(填“>”、“<”或“=”);反应NH4++HCO3-+H2O![]() NH3·H2O+H2CO3的平衡常数K=__________________。(已知常温下NH3·H2O的电离平衡常数Kb=2×10-5,H2CO3的电离平衡常数K1=4×10-7mol·L-1,K2=4×10-11mol·L-1)
NH3·H2O+H2CO3的平衡常数K=__________________。(已知常温下NH3·H2O的电离平衡常数Kb=2×10-5,H2CO3的电离平衡常数K1=4×10-7mol·L-1,K2=4×10-11mol·L-1)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙酸分子的结构式为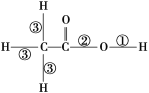 ,下列反应及断键部位正确的是
,下列反应及断键部位正确的是
①乙酸的电离,是①键断裂
②乙酸与乙醇发生酯化反应,是②键断裂
③在红磷存在时,Br2与CH3COOH的反应:CH3COOH+Br2![]() CH2Br—COOH+HBr,是③键断裂
CH2Br—COOH+HBr,是③键断裂
④乙酸变成乙酸酐的反应:2CH3COOH→![]() ,是①②键断裂
,是①②键断裂
A. ①②③ B. ①②③④ C. ②③④ D. ①③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】取0.92 g由C、H、O三种元素组成的有机物A,在足量氧气中完全燃烧,若将燃烧产物通过碱石灰,碱石灰质量增加2.84 g;若将燃烧产物通过浓硫酸,浓硫酸质量增加1.08 g;已知:A的蒸气对氢气的相对密度为23。
(1)A的分子式是_____;
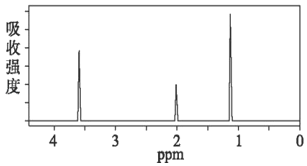
(2)A的1H核磁共振谱图如图所示,写出其结构简式:_____;它的一种同分异构体的结构简式为_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物A~F的转化关系如下图所示。已知A在标准状况下的密度为1.25gL—1,D能发生银镜反应,F是难溶于水且有芳香气味的油状液体。
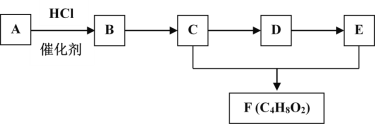
请回答:
(1)A中官能团名称为________。
(2)C→D的反应类型是_________。
(3)A和E一定条件下也可生成F的化学方程式是_______。
(4)下列说法正确的是______。
A.A和B都能使酸性KMnO4褪色
B.D和E能用新制氢氧化铜悬浊液检验
C.可以用饱和碳酸钠溶液除去C、E和F混合物中的C、E
D.推测有机物F可能易溶于乙醇
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图示与对应的叙述不相符的是
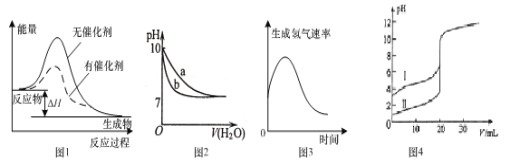
A.图1表示某放热反应分别在有、无催化剂的情况下反应过程中的能量变化
B.图2表示相同温度下,向pH=10的氢氧化钠溶液和氨水中分别加水稀释时pH变化曲线,其中b表示氨水稀释时pH的变化曲线
C.图3表示镁条放入盐酸中生成氢气速率随时间的变化,起初反应速率加快的原因能是该反应为放热反应
D.图4表示室温下,用0.l00mol ·L-1NaOH溶液分别滴定20.00 mL 0.100 mol ·L-1的盐酸和醋酸,其中I表示的是滴定盐酸的曲线
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图,在注射器中加入少量Na2SO3晶体,并吸入少量浓硫酸(以不接触纸条为准)。则下列有关说法正确的是( )
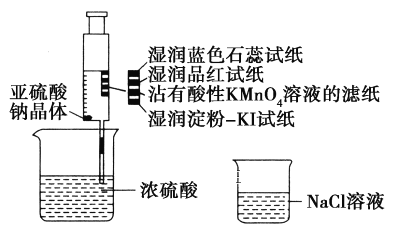
A. 蓝色石蕊试纸先变红后褪色
B. 品红试纸、沾有酸性KMnO4溶液的滤纸均褪色,证明SO2具有漂白性
C. 湿润淀粉-KI试纸未变蓝说明SO2的氧化性弱于I2
D. NaCl溶液可用于除去实验中多余的SO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某混合气体由一种气态烷烃和一种气态烯烃(含一个双键)组成,在同温同压下,混合气体对氢气的相对密度13,在标准状况下,将56L混合气体通入足量的溴水中,溴水的质量增重35g。
(1)计算确定混合气体中烃的化学式_____。
(2)混合气体中两种烃的物质的量之比_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com