
【题目】某混合气体由一种气态烷烃和一种气态烯烃(含一个双键)组成,在同温同压下,混合气体对氢气的相对密度13,在标准状况下,将56L混合气体通入足量的溴水中,溴水的质量增重35g。
(1)计算确定混合气体中烃的化学式_____。
(2)混合气体中两种烃的物质的量之比_____。
【答案】CH4、C4H8 3∶1
【解析】
(1)根据相对密度得出混合气体的平均相对分子质量,混合气体中必定有甲烷,利用混合气体的总体积得出混合气体的物质的量,算出混合气体的总质量,加入溴水后,溴水的质量增加的的是烯烃的质量,即烯烃的质量是35g,甲烷的质量为65g-35g=31g,甲烷的总物质的量为![]() =1.875mol,设烯烃的分子式为CnH2n,利用烯烃的质量关系,(2.5mol-1.875mol)×14ng·mol-1=35g,可以算出n的值;
=1.875mol,设烯烃的分子式为CnH2n,利用烯烃的质量关系,(2.5mol-1.875mol)×14ng·mol-1=35g,可以算出n的值;
(2)根据分析可以得到甲烷与丁烯的物质的量之比。
(1)混合气体的平均相对分子质量为13×2=26,必有甲烷,混合气体的物质的量为![]() =2.5mol,混合气体的质量为2.5 mol×26 g·mol-1=65g,甲烷的物质的量为
=2.5mol,混合气体的质量为2.5 mol×26 g·mol-1=65g,甲烷的物质的量为![]() =1.875mol;设烯烃的分子式为CnH2n,(2.5mol-1.875mol)×14ng·mol-1=35g,解得n=4,化学式为C4H8;
=1.875mol;设烯烃的分子式为CnH2n,(2.5mol-1.875mol)×14ng·mol-1=35g,解得n=4,化学式为C4H8;
故答案为:CH4、C4H8;
(2)甲烷与丁烯的物质的量之比=1.875mol∶(2.5mol-1.875mol)=3∶1;
故答案为3∶1


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】一定温度下,向3个初始体积均为1.0 L的密闭容器中按下表所示投料,发生反应N2(g)+3H2(g)![]() 2NH3(g) △H<0达到平衡,下列说法错误的是
2NH3(g) △H<0达到平衡,下列说法错误的是
容器编号 | 容器类型 | 起始物质的量/mol | 反应物的转化率 | 平衡时NH3的物质的量/mol | ||
N2 | H2 | NH3 | ||||
Ⅰ | 恒温恒容 | 1 | 3 | 0 | α1 | 1.2 |
Ⅱ | 绝热恒容 | 1 | 3 | 0 | α2 | a |
Ⅲ | 恒温恒压 | 2 | 6 | 0 | α3 | b |
A. 达到平衡时,α1>α2
B. 平衡时NH3的物质的量b<2.4
C. 达到平衡时,容器Ⅱ中的反应速率比容器Ⅰ中的大
D. 保持温度不变,向容器Ⅰ中再充入0.1mol N2、0.2mol H2、0.2 mol NH3,平衡向正反应方向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知CrO42-和Cr2O72-在溶液中可相互转化。室温下,初始浓度为1.0 mol·L-1的Na2CrO4溶液中c(Cr2O72-)随c(H+)的变化如图所示。

(1)用离子方程式表示Na2CrO4溶液中的转化反应______。
(2)由图可知,溶液酸性增大,CrO42-的平衡转化率____(填“增大”“减小”或“不变”)。根据A点数据,计算出该转化反应的平衡常数为________。
(3)升高温度,溶液中CrO42-的平衡转化率减小,则该反应的ΔH________0(填“大于”“小于”或“等于”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】据预测,到2040年我国煤炭消费仍将占能源结构的三分之一左右。H2S在催化活性碳(AC)表面的迁移,对煤的清洁和综合应用起了很大的促进作用,其机理如图所示,其中ad表示物种的吸附状态。下列有关叙述错误的是

A.图中阴影部分表示H2S分子的吸附与离解
B.AC表面作用的温度不同,H2S的去除率不同
C.H2S在AC表面作用生成的产物有H2O、H2、S、SO2、CS2等
D.图中反应过程中只有H—S键的断裂,没有H—S键的形成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】生产医用防护口罩的原料聚丙烯纤维属于有机高分子材料,其单体为丙烯。丙烯除了合成聚丙烯外,还广泛用于制备1,2—二氯丙烷、丙烯醛、丙烯酸等。请回答下列问题:
Ⅰ.工业上用丙烯加成法制备1,2—二氯丙烷,主要副产物为3—氯丙烯,反应原理为:
①![]()
![]()
②![]()
![]()
(1)已知![]() 的活化能
的活化能![]() (逆)为
(逆)为![]() ,则该反应的
,则该反应的![]() (正)活化能为_____
(正)活化能为_____![]() 。
。
(2)一定温度下,向恒容密闭容器中充入等物质的量的![]() 和
和![]() ,在催化剂作用下发生反应①②,容器内气体的压强随时间的变化如下表所示。
,在催化剂作用下发生反应①②,容器内气体的压强随时间的变化如下表所示。
时间/min | 0 | 60 | 120 | 180 | 240 | 300 | 360 |
压强/kPa | 80 | 74.2 | 69.4 | 65.2 | 61.6 | 57.6 | 57.6 |
用单位时间内气体分压的变化来表示反应速率,即![]() ,则反应①前180min内平均反应速率
,则反应①前180min内平均反应速率![]() ____
____![]() (保留小数点后2位)。
(保留小数点后2位)。
Ⅱ.丙烯的制备方法
方法一:丙烷无氧脱氢法制备丙烯反应如下:
![]()
![]()
(3)①某温度下,在刚性容器中充入![]() ,起始压强为10kPa,平衡时总压为14kPa,
,起始压强为10kPa,平衡时总压为14kPa,![]() 的平衡转化率为______。该反应的平衡常数
的平衡转化率为______。该反应的平衡常数![]() ______kPa(保留小数点后2位)。
______kPa(保留小数点后2位)。
②总压分别为100kPa、10kPa时发生该反应,平衡体系中![]() 和
和![]() 的物质的量分数随温度变化关系如图所示:
的物质的量分数随温度变化关系如图所示:
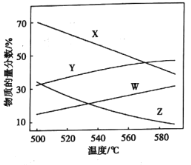
10kPa时,![]() 和
和![]() 的物质的量分数随温度变化关系的曲线分别是_____、______。
的物质的量分数随温度变化关系的曲线分别是_____、______。
方法二:丙烷氧化脱氢法制备丙烯还生成![]() 、
、![]() 等副产物,制备丙烯的反应如下:
等副产物,制备丙烯的反应如下:
![]()
![]() 。在催化剂作用下
。在催化剂作用下![]() 的转化率和
的转化率和![]() 的产率随温度变化关系如图所示。
的产率随温度变化关系如图所示。
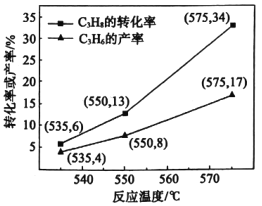
(4)①图中![]() 的转化率随温度升高而上升的原因是_________。
的转化率随温度升高而上升的原因是_________。
②575℃时,![]() 的选择性为___。(
的选择性为___。(![]() 的选择性=
的选择性=![]() )
)
③基于上述研究结果,能提高![]() 选择性的措施是______。
选择性的措施是______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列三个化学反应的平衡常数(K1、K2、K3)与温度的关系分别如表所示:
化学反应 | 平衡常数 | 温度 | |
973K | 1173K | ||
①Fe(s)+CO2(g) | K1 | 1.47 | 2.15 |
②Fe(s)+H2O(g) | K2 | 2.38 | 1.67 |
③CO(g)+H2O(g) | K3 | ? | ? |
下列说法正确的是
A.ΔH1<0,ΔH2>0
B.反应①②③的反应热满足关系:ΔH1-ΔH2=ΔH3
C.反应①②③的平衡常数满足关系:K1·K2=K3
D.要使反应③在一定条件下建立的平衡向正反应方向移动,可采取降温措施
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定量的X加入某密闭容器中,发生反应:2X(g)![]() 3Y(g)+Z(g),混合气体中X的物质的量分数与温度关系如图所示:下列推断正确的是()。
3Y(g)+Z(g),混合气体中X的物质的量分数与温度关系如图所示:下列推断正确的是()。
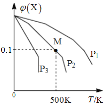
A. 升高温度,该反应平衡常数K减小
B. 压强大小有P3>P2>P1
C. 平衡后加入高效催化剂使平均摩尔质量增大
D. 在该条件下M点X平衡转化率为9/11
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:![]() 。室温下,向浓度为0.1mol·L-1的氨水中缓缓通入HCl,
。室温下,向浓度为0.1mol·L-1的氨水中缓缓通入HCl,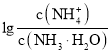 随pOH的变化曲线如下图所示。假设溶液体积没有变化,下列推断正确的是( )
随pOH的变化曲线如下图所示。假设溶液体积没有变化,下列推断正确的是( )
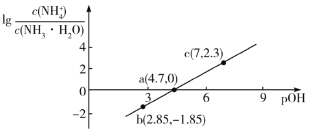
A.NH3·H2O的电离常数的数量级为10-4
B.b点溶液中:![]()
C.c点溶液中:![]()
D.pOH=8的溶液中:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以氯酸钠(NaClO3)等为原料制备亚氯酸钠(NaClO2)的工艺流程如下,下列说法中,不正确的是
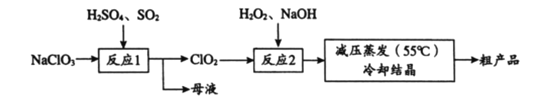
A. 反应1中,每生成1 mol ClO2有0.5 mol SO2被氧化
B. 从母液中可以提取Na2SO4
C. 反应2中,H2O2做氧化剂
D. 采用减压蒸发可能是为了防止NaClO2受热分解
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com