
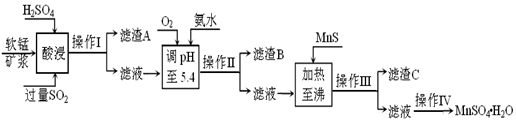
| 沉淀物 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Mn(OH)2 | Cu(OH)2 | Zn(OH)2 | CuS | ZnS | MnS | FeS |
| pH | 5.2 | 3.2 | 9.7 | 10.4 | 6.7 | 8.0 | ≥-0.42 | ≥2.5 | ≥7 | ≥7 |
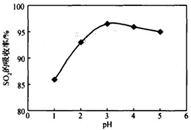
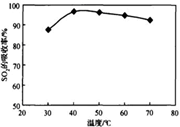
 Zn2++2OH-,由于表中氢氧化锌完全沉淀时溶液pH=8.0,25℃时Kw=1.0×10-14,则该溶液中c(H+)=1.0×10-8mol/L,c(OH-)=Kw/ c(H+)=10-6mol/L,由于此时溶液c(Zn2+)=1.0×10-5mol/L,则Ksp[Zn(OH)2(s)]= c(Zn2+)? c2(OH-)= 1.0×10-17,注意保留两位有效数字。
Zn2++2OH-,由于表中氢氧化锌完全沉淀时溶液pH=8.0,25℃时Kw=1.0×10-14,则该溶液中c(H+)=1.0×10-8mol/L,c(OH-)=Kw/ c(H+)=10-6mol/L,由于此时溶液c(Zn2+)=1.0×10-5mol/L,则Ksp[Zn(OH)2(s)]= c(Zn2+)? c2(OH-)= 1.0×10-17,注意保留两位有效数字。

 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案 本土教辅赢在暑假高效假期总复习云南科技出版社系列答案
本土教辅赢在暑假高效假期总复习云南科技出版社系列答案 暑假作业北京艺术与科学电子出版社系列答案
暑假作业北京艺术与科学电子出版社系列答案科目:高中化学 来源:不详 题型:单选题
| A.pH=3的溶液:Ca2+、CH3COOH、Br-、Na+ |
| B.水电离的c(H+)=1×10-13mo1·L-1的溶液:Na+、K+、SO42-、CO32- |
| C.含有大量Fe3+的溶液:Na+、Mg2+、NO3-、SCN- |
| D.含有大量NO3-的溶液:NH4+、H+、SO42-、I- |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.H2S溶液中: Br-、Na+ 、SO42-、Hg2+ |
| B.c(H+)=l×l0-13mol/L的溶液中:K+ 、Cl-、SO42-、 C6H5O- |
| C.与铝反应产生大量氢气的溶液中: NO3-、I- 、Al3+、Na+ |
| D.含有0.1mol/L Fe3+的溶液中: CO32-、NH4+、 NO3-、 Na+ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.NH4+、Ca2+、OHˉ、CO32ˉ |
| B.Ag+、H+、SO32ˉ、ClOˉ |
| C.NH4+、Brˉ、Na+、SO42ˉ |
| D.H+、Clˉ、Fe2+、NO3ˉ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.稀氨水吸收足量SO2:NH3·H2O + SO2= NH4++ HSO3- |
| B.向Ca(ClO)2溶液中通入过量二氧化碳:ClO-+ H2O + CO2=" HClO" + HCO3- |
| C.稀硝酸中加入铁粉:2Fe + 6H+= 2Fe3++ 3H2↑ |
| D.过氧化钠与冷水反应:2Na2O2+ 2H2O = 4Na++ 4OH-+ O2↑ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.使甲醛呈红色的溶液:NH4+、Ba2+、HCO3-、Cl- |
| B.c(H+)=10-12mol/L的溶液:K+、Ba2+、Br-、Cl- |
| C.1.0mol/L的KNO3溶液:H+、Fe2+、SO42-、Cl- |
| D.与Al反应能产生H2的溶液:NH4+、SO32-、AlO2-、I- |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.Na2S溶液中 SO42-、 K+、Br-、Cu2+ |
| B.在c(H+)=1.0×10-13mol·L-1的溶液中 Na+、S2-、AlO2-、SO32- |
| C.能使甲基橙显红色的溶液: K+、MnO4-、H2C2O4、SO42- |
| D.在 NH3·H2O 的溶液中Ba2+、NO3-、Cl-、Ag+ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.在含大量Fe3+的溶液中:NH4+、Na+、Cl-、SCN- |
| B.在强碱性溶液中:Na+、K+、AlO2-、CO32- |
| C.在c(H+)=10-13 mol/L的溶液中:NH4+、Al3+、SO42-、NO3- |
| D.在pH=1的溶液中:K+、Fe2+、Cl-、NO3- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com