
【题目】用惰性电极电解一定量的硫酸铜溶液,电解一段时间后,向电解液加入0.1mol碱式碳酸铜晶体(不含结晶水),恰好使溶液恢复到电解前的浓度和pH.下列有关叙述不正确的是( )
A.电解过程产生的气体体积(在标准状况下)为5.6 L
B.电解过程只发生了2CuSO4+2H2O ![]() 2Cu+O2↑+2H2SO4
2Cu+O2↑+2H2SO4
C.电解过程转移的电子数为3.612×1023个
D.加入的碱式碳酸铜的反应是:Cu2(OH)2CO3+2H2SO4═2CuSO4+CO2↑+3H2O
【答案】B
【解析】解:电解硫酸铜溶液后溶液呈酸性,向电解后的溶液中加入碱式碳酸铜能恢复原溶液,碱式碳酸铜和硫酸反应生成硫酸铜、水和二氧化碳,溶液质量增加的量是铜、氢氧根离子,所以实际上电解硫酸铜溶液分两个阶段:第一阶段2CuSO4+2H2O ![]() 2Cu↓+O2↑+2H2SO4 ,
2Cu↓+O2↑+2H2SO4 ,
第二阶段:2H2O ![]() 2H2↑+O2↑,
2H2↑+O2↑,
将碱式碳酸铜化学式改变为2CuOH2OCO2 , 所以加入0.1molCu2(OH)2CO3 就相当于加入0.2molCuO和0.1mol水,
第一阶段:根据铜原子守恒知,电解硫酸铜溶液析出n(Cu)=n(CuO)=0.2mol,转移电子的物质的量=0.2mol×2=0.4mol;
第二阶段:电解生成0.1mol水转移电子的物质的量=0.1mol×2=0.2mol,
所以解过程中共转移的电子数为0.4mol+0.2mol=0.6mol;
A、电解分为两步电解硫酸铜和水生成氧气0.1mol,电解0.1mol水生成0.1mol氢气和0.05mol氧气,共生成气体0.15mol+0.1mol=0.25mol,气体标准状况体积=0.25mol×22.4L/mol=5.6L,故A正确;
B、电解硫酸铜溶液分两个阶段:第一阶段2CuSO4+2H2O ![]() 2Cu↓+O2↑+2H2SO4 , 第二阶段:2H2O
2Cu↓+O2↑+2H2SO4 , 第二阶段:2H2O ![]() 2H2↑+O2↑,故B错误;
2H2↑+O2↑,故B错误;
C、上述分析计算可知电子转移总数为0.6mol,电解过程转移的电子数=0.6mol×6.02×1023=3.612×1023个,故C正确;
D、加入的碱式碳酸铜的反应是:Cu2(OH)2CO3+2H2SO4═2CuSO4+CO2↑+3H2O,故D正确;
故选B.


 黄冈小状元同步计算天天练系列答案
黄冈小状元同步计算天天练系列答案科目:高中化学 来源: 题型:
【题目】下列关于原子结构的说法正确的是( )
A. 所有原子都含有质子、中子和电子3种基本微粒
B. 质子数决定元素的种类,中子数决定原子的种类
C. 质子、中子和电子不可以进一步分成更小的微粒
D. 1H、2H、3H互称为同位素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】具有显著抗癌活性的10﹣羟基喜树碱的结构如图所示.下列关于10﹣羟基喜树碱的说法正确的是( ) 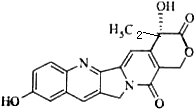
A.分子式为C20H16N2O5
B.不能与FeCl3溶液发生显色反应
C.不能发生酯化反应
D.一定条件下,1mol该物质最多可与1mol NaOH反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据所学知识,完成题目:
(1)请写出下列反应对应的离子方程式: ①用盐酸中和氢氧化钠溶液: .
②用稀硫酸清洗铁锈(Fe2O3):;
(2)写出离子反应方程式所对应的一个化学方程式.①Ba2++2OH﹣+SO ![]() +2H+=BaSO4↓+2H2O
+2H+=BaSO4↓+2H2O
②CO ![]() +2H+=H2O+CO2↑ .
+2H+=H2O+CO2↑ .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用 X 射线对 BaSO4 穿透能力较差的特性,医学上在进行消化系统的 X 射线透视时,常用 BaSO4 作内服造影剂,这种检查手段称为钡餐透视.
(1)医学上进行钡餐透视时为什么不用 BaCO3?(用离子方程式表示)________________________________
(2)某课外活动小组为了探究 BaSO4 的溶解度,分别将足量 BaSO4 放入a.5mL 水 ;b.40mL 0.2molL-1Ba(OH)2 溶 液 c.20mL 0.5molL-1Na2SO4 溶 液 d.40mL 0.1molL-1H2SO4溶液中,溶解至饱和。
①以上各溶液中,Ba2+的浓度由大到小的顺序为_______________________________
A.b>a>c>d B.b>a>d>c C.a>d>c>b D.a>b>d>c
②已知 25℃时,Kap=1.1×10-10,上述条件下,溶液 b 中的 SO42-浓度为_________________molL-1,溶解 c中 Ba2+的浓度为_________________molL-1
③某同学取同体积的溶液 b 和溶液 d④直接混合,则混合液的 pH 为_________________(设混合溶液的体积为混合前两溶液的体积之和)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】观察如下反应,总结规律,然后完成下列问题:①Al(OH)3+H2OAl(OH) ![]() +H+;
+H+;
②NH3+H2ONH ![]() +OH﹣
+OH﹣
(A)已知B(OH)3是一元弱酸,试写出其电离方程式________;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求填空:
(1)0.4mol氨气和0.2mol硫化氢的质量之比为 , 所含分子数之比为 .
(2)现有NH3、H2S、HCl三种气体,它们分别都含有1mol氢原子,则三种气体的物质的量之比为 .
(3)以下物质:①碳酸钾 ②空气 ③二氧化碳 ④铜 ⑤食盐 ⑥氢氧化钠 ⑦硫酸铜溶液 ⑧酒精 ⑨蔗糖(C12H22O11).其中属于电解质的是(填序号).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化学反应对应的离子方程式表示正确的是( )
A.FeCl3溶液与Cu的反应:Cu+Fe3+═Cu2++Fe2+
B.NH4HCO3溶于过量的NaOH溶液中:HCO ![]() +OH﹣═
+OH﹣═ ![]() +H2O
+H2O
C.少量SO2通入苯酚钠溶液中:C6H5O﹣+SO2+H2O═C6H5OH+HSO ![]()
D.FeBr2溶液与等物质的量的Cl2反应:2Fe2++2Br﹣+2Cl2═2Fe3++4Cl﹣+Br2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海洋是一个丰富的资源宝库,通过海水的综合利用可获得许多物质供人类使用.
(1)海水中盐的开发利用:Ⅰ.海水制盐目前以盐田法为主,建盐田必须选在远离江河入海口,多风少雨,潮汐落差大且又平坦空旷的海滩.所建盐田分为贮水池、蒸发池和池.
II.目前工业上采用比较先进的离子交换膜电解槽法进行氯碱工业生产,在电解槽中阳离子交换膜只允许阳离子通过,阻止阴离子和气体通过,请说明氯碱生产中阳离子交换膜的作用(写一点即可)
(2)电渗析法是近年来发展起来的一种较好的海水淡化技术,其原理如图所示.请回答后面的问题:
Ⅰ.海水不能直接通入到该装置中,理由是 .
Ⅱ.B口排出的是(填“淡水”或“浓水”).
(3)用苦卤(含Na+、K+、Mg2+、Cl﹣、Br﹣等离子)可提取溴,其生产流程如下:
Ⅰ.若吸收塔中的溶液含BrO3﹣ , 则吸收塔中反应的离子方程式为 .
Ⅱ.通过①氯化已获得含Br2的溶液,为何还需经过吹出、吸收、酸化来重新获得含Br2的溶液? .
Ⅲ.向蒸馏塔中通入水蒸气加热,控制温度在900C左右进行蒸馏的原因是 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com