
【题目】按要求完成下列问题:
(1)松油醇(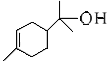 )的官能团的名称为________
)的官能团的名称为________
(2)戊烷有____种结构,请写出其中的核磁共振氢谱有1个吸收峰的结构简式__________
(3)分子式为![]() 且含两种官能团的链状有机物的结构简式为______________
且含两种官能团的链状有机物的结构简式为______________
(4)![]() 在一定条件下能生成高分子化合物的化学方程式为________________
在一定条件下能生成高分子化合物的化学方程式为________________
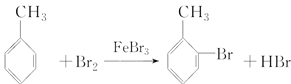
(5)写出甲苯生成 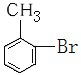 的反应方程式_____________
的反应方程式_____________
【答案】碳碳双键、羟基 3 (CH3)4C CH≡C-CH=CH2 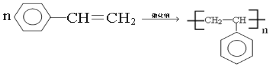
【解析】
(1)松油醇(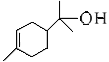 )含官能团有C=C、-OH,名称为碳碳双键、羟基,故答案为:碳碳双键;羟基。
)含官能团有C=C、-OH,名称为碳碳双键、羟基,故答案为:碳碳双键;羟基。
(2)戊烷有3种结构,①CH3CH2CH2CH2CH3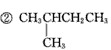
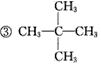 ,核磁共振氢谱有1个吸收峰,说明它的结构十分对称,其结构简式为(CH3)4C,故答案为:3,(CH3)4C。
,核磁共振氢谱有1个吸收峰,说明它的结构十分对称,其结构简式为(CH3)4C,故答案为:3,(CH3)4C。
(3)根据分子式为C4H4,得知其不饱和度为3,因为该有机物含两种官能团,故其结构中应含1个碳碳双键和1个碳碳三键,结构简式为CH≡C-CH=CH2,故答案为:CH≡C-CH=CH2。
(4)![]() 在一定条件下发生加聚反应生成高分子化合物的化学方程式为
在一定条件下发生加聚反应生成高分子化合物的化学方程式为![]() ,故答案为:
,故答案为:![]() 。
。
(5)甲苯和液溴在催化剂作用下生成 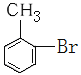 ,反应方程式为:
,反应方程式为:![]() ,故答案为:
,故答案为:![]() 。
。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】Ⅰ、锌和100 mL稀硫酸反应,小组同学根据实验过程绘制的标准状况下的气体体积V与时间 t的图像如下图所示。
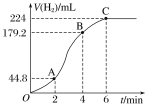
①在OA、AB、BC三段中反应速率最快的是_________,原因是__________________________。
②2~4 min内以硫酸的浓度变化表示的反应速率(假设溶液的体积不变)为________________。
③为了减缓反应速率而又不改变产生氢气的量,该同学在硫酸中分别加入等体积的下列溶液:
A.蒸馏水 B.NaCl溶液 C.0.5mol/L盐酸
其中,你认为可行的是(填序号)______________.
Ⅱ、在一个小烧杯里加入约20 g已研磨成粉末的氢氧化钡晶体[Ba(OH)2·8H2O],将小烧杯放在事先已滴有3~4滴水的玻璃片上,然后向烧杯内加入约10 g氯化铵晶体,并立即用玻璃棒迅速搅拌。试回答下列问题:
(1)实验中要立即用玻璃棒迅速搅拌的原因是______________________________。
(2)“结冰”现象说明该反应断开旧化学键________(填“吸收”或“放出”)的能量________(填“>”或“<”)形成新化学键________(填“吸收”或“放出”)的能量。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应Ⅰ:CaSO4(s)+ CO(g) ![]() CaO(s)+SO2(g)+CO2(g) ΔH=+218.4 kJ·mol-1反应Ⅱ:CaSO4(s)+4CO(g)
CaO(s)+SO2(g)+CO2(g) ΔH=+218.4 kJ·mol-1反应Ⅱ:CaSO4(s)+4CO(g) ![]() CaS(s)+4CO2(g) ΔH=-175.6 kJ·mol-1假设某温度下,反应Ⅰ的速率(v1)大于反应Ⅱ的速率(v2),则下列反应过程能量变化示意图正确的是
CaS(s)+4CO2(g) ΔH=-175.6 kJ·mol-1假设某温度下,反应Ⅰ的速率(v1)大于反应Ⅱ的速率(v2),则下列反应过程能量变化示意图正确的是
A.  B.
B. 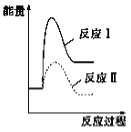 C.
C.  D.
D. 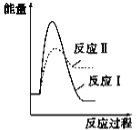
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】新型锌碘液流电池具有能量密度高、循环寿命长等优势,其工作原理如图所示。下列说法错误的是

A. 放电时电流从石墨电极流向锌电极
B. 充电时阳极反应式为:3I--2e-=I3-
C. 若将阳离子交换膜换成阴离子交换膜,放电时正负极也随之改变
D. 放电时左侧电解质储罐中的离子总浓度增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在25℃时,FeS的Ksp=6.3×10-18,CuS的Ksp=1.3×10-36,ZnS的Ksp=1.3×10-24。下列有关说法中正确的是
A. 饱和CuS溶液中Cu2+的浓度为1.3×10-36 mol·L-1
B. 25℃时,FeS的溶解度大于CuS的溶解度
C. 向物质的量浓度相同的FeCl2、ZnCl2的混合液中加入少量Na2S,只有FeS沉淀生成
D. 向饱和ZnS溶液中加入少量ZnCl2固体,ZnS的Ksp变大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分。
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
二 | ① | ② | ③ | ④ | ||||
三 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
回答下列问题:
(1)元素①的名称是____,元素⑧的符号是____。
(2)在这些元素中,___(用元素符号或化学式填写,下同)是最活泼的非金属元素,____是最不活泼的元素。
(3)这些元素的最高价氧化物对应的水化物中,____酸性最强,____碱性最强,具有两性的氢氧化物是____。
(4)比较⑤与⑥的化学性质,____更活泼,试用实验证明此结论(简述操作、现象和结论):________________________。
(5)⑦的最高价氧化物与⑤的最高价氧化物对应的水化物反应的离子方程式是______________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】冬季我国北方大部分地区出现雾霾天气,引起雾霾的微细粒子包含(NH4)2SO4、NH4NO3、有机颗粒物、扬尘、重金属铜等。
(1)N元素原子核外电子云的形状有___种;基态铜原子的价电子排布式为___。
(2)N和O中第一电离能较小的元素是__;SO42-的空间构型___。
(3)雾霾中含有少量的水,组成水的氢元素和氧元素也能形成化合物H2O2,其中心原子的杂化轨道类型为___,H2O2难溶于CC14,其原因为___。
(4)PM2.5富含NO,NO能被FeSO4溶液吸收生成配合物[Fe(NO)(H2O)5]SO4,该配合物中心离子的配位数为___。
(5)测定大气中PM2.5浓度的方法之一是β-射线吸收法,β-射线放射源可用85Kr。已知Kr晶体的晶胞结构如图所示,设NA为阿伏加德罗常数的值,晶胞边长为540pm,则该晶体的密__g/cm3(只列式不计算,Kr摩尔质量为84g·mol-1)。
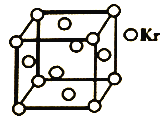
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Na、Al、Fe、Cu是中学化学中重要的金属元素。它们的单质及其化合物之间有很多转化关系。下表所列物质不能按如图(“→”表示一步完成)关系相互转化的是
选项 | A | B | C | D |
|
a | Na | Al | Fe | Cu | |
b | NaOH | Al2O3 | FeCl3 | CuO | |
c | NaCl | Al(OH)3 | FeCl2 | CuCl2 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业废水中仅含下表离子中的5种(不考虑水的电离及离子的水解),且各种离子的物质的量浓度均为0.1 molL-1 。
阳离子 | K+、Cu2+、Fe3+、Al3+、Fe2+ |
阴离子 | Cl-、CO32-、NO3-、SO42-、SiO32- |
某同学欲探究该废水的组成,进行了如下实验:
Ⅰ.用铂丝蘸取少量溶液,在火焰上灼烧,无紫色火焰(透过蓝色钴玻璃观察)。
Ⅱ.取少量溶液,加入KSCN溶液无明显变化。
Ⅲ.另取溶液加入少量盐酸,有无色气体生成,该无色气体遇空气变成红棕色,此时溶液依然澄清,且溶液中阴离子种类不变。
Ⅳ.向Ⅲ中所得溶液中加入BaCl2溶液,有白色沉淀生成。
请回答下列问题:
(1)甲同学最终确定原溶液中所含阳离子有 _____________,阴离子有__________。(写离子符号)
(2)Ⅲ中加入少量盐酸生成无色气体的离子方程式为___________________________。
(3)将Ⅲ中红棕色气体(标况下)收集一满试管然后倒扣入水中(假设溶质不扩散),所得溶液中溶质的物质的量浓度为___________ molL-1 (精确到小数点后第三位)。
(4)另取100mL原溶液,加入足量的NaOH溶液,充分反应后过滤,洗涤,灼烧至恒重,得到的固体的质量为______g。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com