
分析 (1)根据方程式知,2min内SO2的浓度由6mol/L下降为2mol/L,则△c(O2)=$\frac{1}{2}$△c(SO2)=$\frac{1}{2}$×(6-2)mol/L=2mol/L,v(O2)=$\frac{△c}{△t}$,△n(SO2)=△c(SO2)V;
(2)根据二氧化硫与反应热之间的关系式计算放出的热量;增大压强平衡向气体体积减小的方向移动;化学平衡常数只与温度有关;
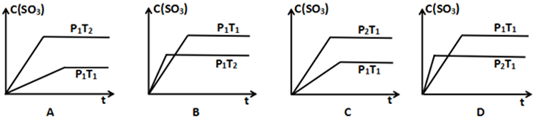
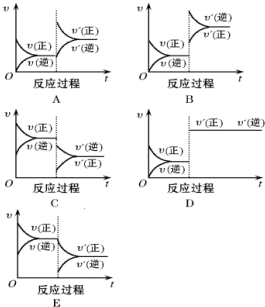
(3)增大压强化学反应速率增大,反应到达平衡的时间缩短,平衡正向移动,三氧化硫浓度增大;升高温度化学反应速率增大,反应到达平衡的时间缩短,平衡逆向移动,三氧化硫浓度减小;
(4)三氧化硫和水反应生成硫酸.
解答 解:(1)根据方程式知,2min内SO2的浓度由6mol/L下降为2mol/L,则△c(O2)=$\frac{1}{2}$△c(SO2)=$\frac{1}{2}$×(6-2)mol/L=2mol/L,v(O2)=$\frac{△c}{△t}$=$\frac{2mol/L}{2min}$=1mol/(L.min),△n(SO2)=△c(SO2)V=4mol/L×1L=4mol,
故答案为:1mol/(L.min);4mol;
(2)根据方程式知,2mol二氧化硫完全反应放出196.3kJ热量,则4mol二氧化硫完全反应放出392.6 kJ热量;增大压强平衡向气体体积减小的方向移动,即平衡向右移动;化学平衡常数只与温度有关,温度不变化学平衡常数不变,
故答案为:392.6 kJ;向右;不变;
(3)增大压强化学反应速率增大,反应到达平衡的时间缩短,平衡正向移动,三氧化硫浓度增大;升高温度化学反应速率增大,反应到达平衡的时间缩短,平衡逆向移动,三氧化硫浓度减小,所以符合的图象为BC,
故答案为:BC;
(4)三氧化硫和水反应生成硫酸,反应方程式为SO3+H2O=H2SO4,
故答案为:SO3+H2O=H2SO4.
点评 本题考查化学平衡移动影响因素、化学平衡计算,为高频考点,侧重考查学生获取信息、利用信息、化学反应原理解答问题能力,注意:化学平衡常数只与温度有关,与反应物浓度、反应物转化率、压强都无关,题目难度不大.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ③④ | C. | ②③ | D. | ②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
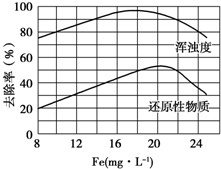 FeCl3具有净水作用,但腐蚀设备,而聚合氯化铁是一种新型的絮凝剂,处理污水比FeCl3高效,且腐蚀性小.请回答下列问题:
FeCl3具有净水作用,但腐蚀设备,而聚合氯化铁是一种新型的絮凝剂,处理污水比FeCl3高效,且腐蚀性小.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 方法1 | 用氨水将SO2转化为NH4HSO3,再氧化成(NH4)2SO4 |
| 方法2 | 用水煤气(主要成分为CO、H2等)将SO2在高温下还原成单质硫 |
| 方法3 | 用Na2SO3溶液吸收SO2转化为NaHSO3,再经电解转化为H2SO4 |
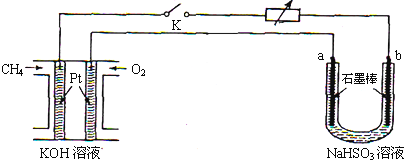
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 如表为元素周期表的一部分.
如表为元素周期表的一部分.| 碳 | 氮 | Y | |
| X | 硫 | Z |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
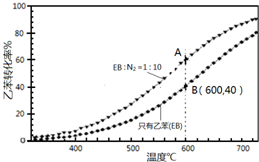 苯乙烯(
苯乙烯(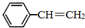 )是生产各种塑料的重要单体,可通过乙苯催化脱氢制得:
)是生产各种塑料的重要单体,可通过乙苯催化脱氢制得: CH2CH3(g)$\stackrel{催化剂}{?}$
CH2CH3(g)$\stackrel{催化剂}{?}$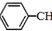 =CH2(g)+H2(g)△=+QkJ.mol-1
=CH2(g)+H2(g)△=+QkJ.mol-1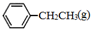 、
、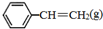 、H2(g)的燃烧热(△H)分别为-Q1 kJ•mol-1、-Q2kJ•mol-1、-Q3 kJ•mol-1,写出Q与Q1、Q2、Q3的关系式Q2+Q3-Q1.
、H2(g)的燃烧热(△H)分别为-Q1 kJ•mol-1、-Q2kJ•mol-1、-Q3 kJ•mol-1,写出Q与Q1、Q2、Q3的关系式Q2+Q3-Q1.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
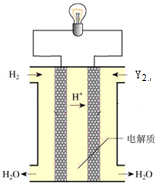
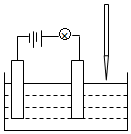 在电解质溶液的导电性实验(装置如图所示)中,若向某一电解质溶液中逐滴加入另一溶液时,则灯泡由亮变暗,至熄灭后又逐渐变亮的是( )
在电解质溶液的导电性实验(装置如图所示)中,若向某一电解质溶液中逐滴加入另一溶液时,则灯泡由亮变暗,至熄灭后又逐渐变亮的是( )| A. | 醋酸中逐滴加入氢氧化钠溶液 | B. | 硫酸钠中逐滴加入氢氧化钡溶液 | ||
| C. | 硫酸中逐滴加入氢氧化钡溶液 | D. | 盐酸中逐滴加入硝酸银溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 溶于水后能电离出H+的化合物都是酸 | |
| B. | BaSO4不溶于水,故BaSO4不是电解质 | |
| C. | CO2溶于水后溶液能导电,故CO2是电解质 | |
| D. | 尽管NaCl固体不导电,但NaCl是电解质 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com