
【题目】关于X、Y、Z三种元素,有以下五点信息
① X、Y、Z的单质在常温下均为气体;
② X单质可以在Z的单质中燃烧,生成物为XZ,火焰呈苍白色;
③ XZ极易溶于水,在水溶液中电离出X+和Z-,其水溶液能使蓝色石蕊试纸变红;
④ 每2个X2分子能与1个Y2分子化合成2个X2Y分子,X2Y常温下为液体;
⑤ Z单质溶于X2Y中,所得溶液具有漂白性。
(1)试写出Z的元素符号______;化合物XZ的电子式:_______,X2Y的结构式_________。
(2)用电子式表示XZ的形成过程_________________________________________________。
(3)写出信息⑤中的化学方程式__________________________________________________。
(4)X2、Y2和KOH溶液一起可以构成新型燃料电池,写出该电池的总反应方程式:
_______________________
已知拆开1mol X—X键、1mol Z—Z键、1mol X—Z键分别需要吸收的能量为436kJ、243kJ、432kJ,计算反应X2(g)+Z2(g)=2XZ(g)的ΔH=________kJ/mol .
【答案】 Cl ![]()
![]()
![]() Cl2+H2O=HCl+HclO(“
Cl2+H2O=HCl+HclO(“![]() ”也可) 2H2+O2=2H2O -185
”也可) 2H2+O2=2H2O -185
【解析】本题分析:本题主要考查氯的化合物的性质。
X的单质在Z的单质中燃烧,生成XZ,并且XZ极易溶于水,在水溶液中电离出X+和Z-。XZ的水溶液可使石蕊试液变红,说明X为H2,Z为Cl2,XZ为HCl;两分子X的单质可与一分子Y的单质化合生成两分子X2Y,X2Y常温下为液体,说明Y为O2,X2Y为H2O。Cl2溶于H2O中,反应生成HCl和HClO,HClO具有漂白作用。
(1)通过以上分析知,Z为Cl;XZ为HCl ,其电子式为![]() ;X2Y为H2O,其结构式为
;X2Y为H2O,其结构式为![]() 。
。
(2)用电子式表示XZ的形成过程:![]() 。
。
(3)信息⑤中氯气溶于水产生次氯酸,反应的化学方程式为Cl2+H2O=HCl+HclO(“![]() ”也可)。
”也可)。
(4)燃料电池的总化学方程式相当于燃烧反应的化学方程式为2H2+O2=2H2O。
ΔH=拆键吸收的能量-成键释放的能量=(436+243-2×432)kJ/mol =-185 kJ/mol。


科目:高中化学 来源: 题型:
【题目】在一定条件下,S8(s)和O2(g)发生反应依次转化为SO2(g)和SO3(g)(已知:2SO2+O2![]() 2SO3),反应过程中的能量关系可用右图简单表示(图中的ΔH 表示生成1 mol产物的数据)。 下列说法正确的是( )
2SO3),反应过程中的能量关系可用右图简单表示(图中的ΔH 表示生成1 mol产物的数据)。 下列说法正确的是( )
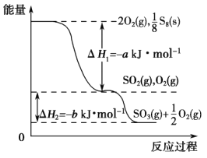
A.S8的燃烧热 ΔH=-a kJ·mol-1
B.1 mol SO2和过量 O2反应可释放出 b kJ 的热量
C.已知1个S8分子中有8个S-S,S=O的键能为d kJ·mol-1,O=O的键能为e kJ·mol-1,则S8分子中S-S的键能为(2d-a-e) kJ·mol-1
D.若使用V2O5作催化剂,当SO2(g)转化生成1mol SO3(g)时,释放的热量小于b kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】课外学习小组为检验溶液中是否含有常见的四种无机离子,进行了如图所示的实验操作。其中操作过程中产生的气体能使红色石蕊试纸变蓝,由该实验能得到的正确结论是( )
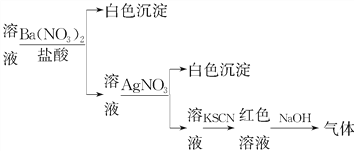
A. 溶液中一定含有SO![]()
B. 溶液中一定含有NH![]()
C. 溶液中一定含有Cl-
D. 溶液中一定含有Fe3+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是部分短周期元素原子半径与原子序数的关系图.则下列说法正确的是( )

A. 简单离子的半径:X<Z<M
B. 最高价氧化物对应水化物的酸性:R<N
C. Y、R两种元素的气态氢化物稳定性:Y>R
D. 由X与N两种元素组成的化合物不能与任何酸反应,但能与强碱反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是
A. 符合通式CnH2n+2且n不同的烃一定属于同系物
B. C60和纳米碳管互为同素异形体
C. 宇宙射线的作用下可使14N转化为14C,14N和14C互为同位素
D. C5H12的某种同分异构体只有一种一氯代物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于生物体内水和无机盐的叙述,错误的是
A. 是细胞中能源物质之一
B. 哺乳动物血液中钙离子含量过少会引起抽搐
C. 细胞内的自由水是生化反应的重要介质
D. 铁是合成血红蛋白的原料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究性学习小组设计了一组实验验证元素周期律。
(Ⅰ)甲同学在a、b、c三只烧杯里分别加入50 mL水,再分别滴加几滴酚酞溶液,依次加入大小相近的锂、钠、钾块,观察现象。
甲同学设计实验的目的是 , 烧杯 (填字母)中的反应最剧烈。
(Ⅱ)乙同学设计实验验证非金属元素的非金属性越强,对应的最高价含氧酸的酸性就越强。他设计了下图装置以验证氮、碳、硅元素的非金属性强弱。

乙同学设计的实验可直接证明三种酸的酸性强弱,已知A是强酸,常温下可与铜反应;B是块状固体;打开分液漏斗的活塞后,C中可观察到有白色沉淀生成。
(1)写出所选用物质的化学式:A: ;B: ; C: 。
(2)写出烧杯中发生反应的离子方程式:
(3)该装置存在着某个缺陷,改进的方法是
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是(设阿伏加德罗常数的数值为NA)( )
A. 在标准状况下,22.4L水所含分子数目为NA
B. 1mol·L-1K2SO4溶液所含K+数目为2NA
C. 1 mol钠与氧气反应生成Na2O或Na2O2时,失电子数目均为NA
D. O2的摩尔体积约为22.4 L·mol-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com