
【题目】下列事实不能说明Cl原子的得电子能力比S原子强的是( )
①HCl比H2S稳定
②HClO氧化性比H2SO4强
③HClO4酸性比H2SO4强
④Cl2能与H2S反应生成S
⑤Cl原子最外层有7个电子,S原子最外层有6个电子
⑥Cl2与Fe反应生成FeCl3,S与Fe反应生成FeS
A.②⑤B.①②C.①②④D.①③⑤
 挑战100单元检测试卷系列答案
挑战100单元检测试卷系列答案科目:高中化学 来源: 题型:
【题目】某兴趣小组用铝箔制备Al2O3、AlCl3·6H2O及明矾大晶体,具体流程如下

已知:(1) AlCl3·6H2O易溶于水、乙醇及乙醚;
(2) 明矾在水中的溶解度如下表:
温度/℃ | 0 | 10 | 20 | 30 | 40 | 60 | 80 | 90 |
溶解度/g | 3.00 | 3.99 | 5.90 | 8.39 | 11.7 | 24.8 | 71.0 | 109 |
(1)步骤Ⅱ中生成Al(OH)3的离子方程式为____________________________________________。
(2)步骤Ⅲ灼烧Al(OH)3所用实验室常用仪器为________,为了提高Al2O3纯度,需________(填操作步骤)。
(3)制备AlCl3·6H2O的工业生产中,胶状固体用酸浸取后,还需要通入HCl气体。通入HCl的作用主要有两点:____________和____________。
(4)已知:在不同温度条件下向一定量的氯化铝溶液中通入HCl气体,通入量对AlCl3·6H2O结晶量和结晶效率的影响如图,请补充完整由胶状固体制备AlCl3·6H2O晶体的实验方案:向胶状固体滴加一定浓度盐酸,直至恰好完全溶解,__________________________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化学用语正确的有
①乙酸的最简式:CH2O ②聚丙烯的结构简式:![]()
③羟基的电子式:![]() ④丙烷分子的比例模型:
④丙烷分子的比例模型:
⑤四氧化碳分子的电子式: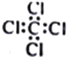 ⑥乙醇的分子式: CH3CH2OH
⑥乙醇的分子式: CH3CH2OH
⑦H2CO3的电离方程式:H2CO3![]() H++HCO3-⑧2-乙基-l,3-丁二烯分子的键线式:
H++HCO3-⑧2-乙基-l,3-丁二烯分子的键线式:
A. 1个 B. 2个 C. 3个 D. 4个
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液中含有较大量的Cl﹣、![]() 、OH﹣等3种阴离子,如果只取一次该溶液就能够分别将3种阴离子依次检验出来,下列实验操作顺序正确的是( )
、OH﹣等3种阴离子,如果只取一次该溶液就能够分别将3种阴离子依次检验出来,下列实验操作顺序正确的是( )
①滴加Mg(NO3)2溶液;②过滤;③滴加AgNO3溶液;④滴加Ba(NO3)2溶液
A.①②④②③B.④②①②③C.①②③②④D.④②③②①
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】摩尔质量是指单位物质的量的物质所具有的质量,已知NA为阿伏加德罗常数的值,请回答下列问题:
(1)已知NH3的相对分子质量为17,则NH3的摩尔质量为________。
(2)已知一个铁原子的质量为b g,则铁原子的摩尔质量为________。
(3)已知a g某气体中含分子数为b,则该气体的摩尔质量为________。
(4)有以下四种物质:①22 g二氧化碳 ②8 g氢气 ③1.204×1024个氮气分子 ④4 ℃时18 mL水,它们所含分子数最多的是__________,质量最大的是________,所含电子数最多的是________(填序号)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以电石渣[主要成分Ca(OH)2,含Fe2O3、MgO和SiO2等杂质]为原料制备纳米碳酸钙的一种工艺流程如下:


(1)“浸渍”时,NH4Cl和Ca(OH)2反应的化学方程式为________________________________________。
(2)“浸渍”时,一定时间内Ca2+浸取率随温度变化如图所示。Ca2+浸取率随温度升高而上升的两个原因是_________________________________________;__________________________________________。
(3) “碳化”时,一般采用低温工艺,对应的离子方程式为___________________________。
(4)滤液Ⅱ中,可循环利用的溶质的化学式为___________________________________。
(5)“洗涤”时,检验是否洗净的方法是________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列措施不能加快Zn与1mol/LH2SO4反应产生H2的速率的是( )
A.升高温度B.用Zn粉代替Zn粒
C.滴加少量的CuSO4溶液D.改用0.1mol·L-1H2SO4与Zn反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用铁泥(主要成分为Fe2O3、FeO和少量Fe)制备纳米Fe3O4,的流程示意图如下:

下列叙述错误的是
A. 为提高步骤①的反应速率,可采取搅拌、升温等措施
B. 步骤②中,主要反应的离子方程式是2Fe3++Fe=3Fe2+
C. 步骤④中,反应完成后剩余的H2O2无需除去
D. 步骤⑤中,“分离”包含的操作有过滤、洗涤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是( )
A. 温度升高,正逆反应速率都增大
B. 化学反应的速率和限度均可通过改变化学反应条件而改变
C. 可逆反应只是代表少数反应
D. 化学反应达到平衡状态时,正反应速率与逆反应速率相等
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com