
【题目】用铁泥(主要成分为Fe2O3、FeO和少量Fe)制备纳米Fe3O4,的流程示意图如下:

下列叙述错误的是
A. 为提高步骤①的反应速率,可采取搅拌、升温等措施
B. 步骤②中,主要反应的离子方程式是2Fe3++Fe=3Fe2+
C. 步骤④中,反应完成后剩余的H2O2无需除去
D. 步骤⑤中,“分离”包含的操作有过滤、洗涤
【答案】C
【解析】
铁泥(主要成分为Fe2O3、FeO和少量Fe)与稀盐酸反应得到的滤液A溶质为氯化铁、氯化亚铁、过量的稀盐酸,加入铁粉还原铁离子:2Fe3++Fe=3Fe2+,过滤过量的铁,滤液B的溶质为氯化亚铁,加入氢氧化钠溶液,生成Fe(OH)2浑浊液,向浑浊液中加入双氧水,双氧水将Fe(OH)2浊液氧化成浊液D,反应完成后需再加热一段时间除去剩余H2O2,浊液D与滤液B加热搅拌发生反应制得Fe3O4,经过滤、洗涤、干燥得产品Fe3O4,据此分析解答。
A.搅拌、适当升高温度可提高铁泥与盐酸的反应速率,A正确;
B.滤液A的溶质为氯化铁、氯化亚铁、过量的稀盐酸,加入铁粉还原Fe3+,即主要的离子反应为:2Fe3++Fe=3Fe2+,B正确;
C.步骤④中,浊液C中的氢氧化亚铁被过氧化氢氧化成浊液D,为了提高Fe3O4的产率需要控制浊液D与滤液B中Fe2+的比例,为防止滤液B中Fe2+在步骤⑤中被H2O2氧化,步骤④中反应完成后需再加热一段时间除去剩余H2O2,C错误;
D.步骤⑤为浊液D与滤液B加热搅拌发生反应制得Fe3O4,使Fe3O4分离出来需经过过滤、洗涤、干燥,D正确;
故答案选C。


 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案科目:高中化学 来源: 题型:
【题目】非金属单质A经如图所示的过程转化为含氧酸D,已知D为强酸,请回答下列问题。
![]()
![]()
![]()
![]()
![]()
![]()
![]()
(1)若A在常温下为固体,B是能使品红溶液褪色的有刺激性气味的无色气体:
①D的化学式是________;
②在工业生产中,B气体的大量排放被雨水吸收后形成了________而污染了环境。
(2)若A在常温下为气体,C是红棕色的气体:
①A、C的化学式分别是:A________;C________。
②D的浓溶液在常温下可与铜反应并生成C气体,请写出该反应的化学方程式_______________________________________________。该反应________(填“属于”或“不属于”)氧化还原反应。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列事实不能说明Cl原子的得电子能力比S原子强的是( )
①HCl比H2S稳定
②HClO氧化性比H2SO4强
③HClO4酸性比H2SO4强
④Cl2能与H2S反应生成S
⑤Cl原子最外层有7个电子,S原子最外层有6个电子
⑥Cl2与Fe反应生成FeCl3,S与Fe反应生成FeS
A.②⑤B.①②C.①②④D.①③⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据反应:①2Fe3++2I-=2Fe2++I2②Br2+2Fe2+=2Fe3++2Br-③Br2+2I-=I2+2Br-,判断离子的还原性由强到弱的顺序正确的是( )
A. Br-、Fe2+、I-B. I-、Fe2+、Br-
C. Br-、I-、Fe2+D. Fe2+、I-、Br-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在2L的体积不变的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示。
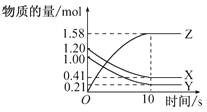
(1)写出该反应的化学方程式:________。
(2)从反应开始到10s,用Z表示的反应速率为________mol·L-1·s-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向10mL0.1 mol/L CuCl2溶液中滴加0.1 mol/L Na2S溶液滴加过程中-lgc(Cu2+)与Na2S溶液体积(V)的关系如图所示。下列说法错误的是

A. Ksp(CuS)的数量级为10-35
B. 曲线上各点的溶液均满足关系式c(S2-)·c(Cu2+)=Ksp(CuS)
C. a、b、c三点中,由水电离的c(H+)和c(OH-)的积最小的为b点
D. c点溶液中:c(Na+)>c(Cl-)>c(S2-)>c(OH-)>c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分,根据A~H在元素周期表中的位置,用元素符号或化学式回答下列问题:
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
1 | A | |||||||
2 | D | E | G | |||||
3 | B | C | F | H |
(1)上表中,元素金属性最强的是________(填元素符号)。
(2)写出D的原子结构示意图:__________
(3)B与C的原子半径比较: ________C (填“>”或“<”)。G与H的非金属性比较:G ________ H(填“>”或“<”)。
(4)A与H形成化合物的电子式:_______
(5)写出B的最高价氧化物对应水化物与H的气态氢化物的水溶液反应的离子方程式:______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25 ℃时,下列各组数据中比值为2:1的是( )
A. 0.2 mol/L的CH3COONa溶液与0.1 mol/L的CH3COONa溶液中c(CH3COO-)之比
B. pH=7的氨水与(NH4)2SO4的混合溶液中c(NH4+)与c(SO42-)之比
C. 等质量的Na2CO3固体和NaHCO3固体分别与足量盐酸反应,消耗盐酸的物质的量之比
D. pH均为2的H2SO4溶液与盐酸中c(H+)之比
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有四组分散系:①汽油和水形成的乳浊液;②含有泥沙的食盐水;③溶有碘(I2)的酒精溶液;④乙二醇和丙三醇的混合溶液(乙二醇和丙三醇的部分物理性质见下表)。
物质 | 熔点/℃ | 沸点/℃ | 密度/g·cm-3 | 溶解性 |
乙二醇 | -11.5 | 198 | 1.11 | 易溶于水和乙醇 |
丙三醇 | 17.9 | 290 | 1.26 | 能跟水、酒精以任意比互溶 |
请用下图所示的仪器分离以上各混合液,仪器和方法不能对应的是( )

A. ①―c―分液 B. ②―b―过滤 C. ③―d―蒸发结晶 D. ④―a―蒸馏
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com