
| A. | 大于50% | B. | 等于50% | C. | 小于50% | D. | 无法确定 |
分析 设质量分数分别为10%与90%的硫酸溶液的密度分别为xg/mL、yg/mL,硫酸溶液的密度随浓度增大而增大,所以x<y.假定体积为VmL,混合后溶质质量为混合前两溶液中溶质质量之和,混合后溶液质量为混合前溶液质量之和,根据质量分数定义用x、y表示出混合后的质量分数,结合密度关系判断.
解答 解:设质量分数分别为10%与90%的硫酸溶液的密度分别为xg/mL、yg/mL,硫酸溶液的密度随浓度增大而增大,所以x<y.
假定体积为VmL,则10%硫酸溶液的质量为VmL×xg/mL=Vxg,溶质硫酸的质量为:Vxg×10%=0.1Vxg;
90%的硫酸溶液的质量为VmL×yg/mL=Vyg,溶质硫酸的质量为:Vyg×90%=0.9Vyg;
则混合后硫酸的溶质质量分数为:$\frac{0.1Vxg+0.9Vyg}{Vxg+Vyg}$×100%=$\frac{0.1x+0.1y+0.8y}{x+y}$×100%=10%+$\frac{0.8y}{x+y}$×100%=10%+80%×$\frac{1}{1+\frac{x}{y}}$,
由于x<y,所以$\frac{x}{y}$<1,则1+$\frac{x}{y}$<2,80%×$\frac{1}{1+\frac{x}{y}}$>40%,
所以混合液中溶质质量分数:10%+80%×$\frac{1}{1+\frac{x}{y}}$>50%,
故选A.
点评 本题考查溶质质量分数的计算,题目难度中等,注意掌握溶质质量分数的概念及计算方法,明确硫酸的浓度越大、密度越大为解答关键,试题培养了学生的分析能力及化学计算能力.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
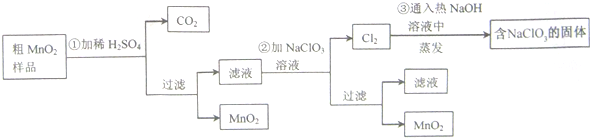
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 时间(s) | 0 | 20 | 40 | 60 | 80 | 100 |
| n(N2O4)/mol | 0.40 | a | 0.20 | c | d | e |
| n(NO2)/mol | 0.00 | 0.24 | b | 0.52 | 0.60 | 0.60 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ,氧化剂是氯酸钾,还原产物是Cl2.
,氧化剂是氯酸钾,还原产物是Cl2.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 儿童牙膏 | 防臭牙膏 | 透明牙膏 | |
| 摩擦剂 | 氢氧化铝 | 碳酸钙 | 氧化硅 |
| 物质类别 | 碱 | 盐 | 氧化物 |
 ,请写出氟化钠在水溶液中的电离方程式NaF=Na++F-.
,请写出氟化钠在水溶液中的电离方程式NaF=Na++F-.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2HI(g)?H2(g)+I2(g)△H<0 | B. | N2(g)+3H2(g)?2NH3(g)△H<0 | ||
| C. | C(s)+H2O(g)?CO(g)+H2(g)△H>0 | D. | CaCO3(s)?CO2(g)+CaCO3(s)△H>0 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
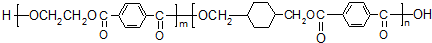
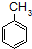 $\stackrel{KMnO_{4}/H+}{→}$
$\stackrel{KMnO_{4}/H+}{→}$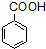
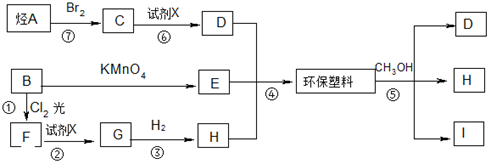
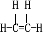 ;
;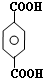 ;B的名称:对二甲苯,试剂X为NaOH水溶液.
;B的名称:对二甲苯,试剂X为NaOH水溶液.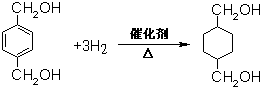 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 人造纤维、合成纤维和碳纤维都是有机高分子化合物 | |
| B. | 加热能杀死流感病毒是因为病毒的蛋白质受热变性 | |
| C. | 煤的干馏和石油的分馏均属于化学变化 | |
| D. | 油脂都不能使溴的四氯化碳溶液褪色 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com