
| A. | H3PO2中磷元素的化合价为+1 | |
| B. | H3PO2的电离方程式为H3PO2?H++H2 PO2- | |
| C. | H3PO2被AgNO3氧化成了H3PO4 | |
| D. | NaH2PO2、NaH2PO4、Na2HPO4均为酸式盐 |
分析 A.根据化合物中化合价的代数和为零计算;
B.一元弱酸部分电离出一个氢离子;
C.H3PO2和AgNO3溶液反应进行化学镀银,此反应中氧化剂与还原剂的物质的量之比为4:1,结合化合价判断产物;
D.H3PO2是一元酸,NaH2PO2是正盐.
解答 解:A.H3PO2中H为+1价,O为-2价,则磷元素的化合价为+1,故A正确;
B.次磷酸是一元弱酸,一元弱酸部分电离出一个氢离子,所以H3PO2的电离方程式为H3PO2?H++H2 PO2-,故B正确;
C.H3PO2中,氢元素为+1价,氧元素为-2价,依据化合价代数和为0,磷化合价为+1价,该反应中Ag+为氧化剂,H3PO2为还原剂,氧化剂与还原剂的物质的量之比为4:1,设反应产物中P的化合价为x,根据化合价升降相等可得,4×(1-0)=1×(x-1),解得x=5,所以氧化产物为+5价的H3PO4,故C正确;
D.H3PO2是一元酸,NaH2PO2是正盐,NaH2PO4、Na2HPO4均为酸式盐,故D错误.
故选D.
点评 本题考查了元素化合价的判断、弱电解质的电离、氧化还原反应、酸式盐的判断,题目涉及的知识点较多,侧重于考查学生对基础知识的应用能力,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 此时溶液中 Fe2+和 Fe3+的物质的量之比为 3:1 | |
| B. | 向溶液中滴入 KSCN 溶液,显血红色 | |
| C. | 无法计算原混合物的质量 | |
| D. | 原混合物中 n(Fe):n(Fe2O3)=2:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 日光灯管破碎,只需收集散落的汞即可 | |
| B. | 金属镁失火,应采用泡沫灭火器灭火 | |
| C. | 钡离子中毒,可以通过服用碳酸钠溶液解毒 | |
| D. | 烧碱溶液溅到皮肤上,应立即用大量的水冲洗 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
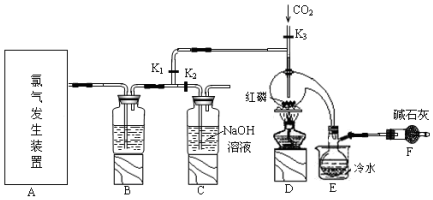
| 物质 | 熔点/℃ | 沸点/℃ |
| PCl3 | -112 | 75.5 |
| POCl3 | 2 | 105.3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 异丁烷的二氯代物 | |
| B. | 分子式为C6 H14的有机物 | |
| C. | 甲酸正丙酯属于酯的同分异构体 | |
| D. | 分子式为C5H10O2并能与饱和NaHCO3溶液反应放出气体的有机物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碘单质受热升华:紫色蒸气 | B. | 硫磺在氧气中燃烧:蓝紫色的火焰 | ||
| C. | 铁丝在氯气中燃烧:棕褐色的烟 | D. | 氢气在氯气中燃烧:淡蓝色火焰 |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
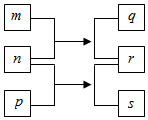 W、X、Y、Z是原子序数依次增大的短周期元素.m、n、p是由这些元素组成的二元化合物,r是元素Y的常见单质,能使带火星的木条复燃,q的水溶液呈碱性,0.01mol•L-1s溶液的pH为12,q、s的焰色反应均呈黄色.上述物质的转化关系如图所示.下列说法正确的是( )
W、X、Y、Z是原子序数依次增大的短周期元素.m、n、p是由这些元素组成的二元化合物,r是元素Y的常见单质,能使带火星的木条复燃,q的水溶液呈碱性,0.01mol•L-1s溶液的pH为12,q、s的焰色反应均呈黄色.上述物质的转化关系如图所示.下列说法正确的是( )| A. | 原子半径:W<X<Y<Z | |
| B. | Y的氢化物的沸点比Z的氢化物的沸点高 | |
| C. | 通常状况下,X的氢化物可能呈气态、液态或固态 | |
| D. | 由W、X、Y、Z四种元素只能组成一种化合物 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com