
����Ŀ��Ӣ������˹�ش�ѧ��ѧ�Ұ����ҡ���ķ�Ϳ�˹̹����ŵ��Ф���ͬ��������Ķ�����ͻ���Եء���˺�ѵķ�����ʯī�гɹ���ó�������ʯīϩ�����Ʊ�ʯīϩ������ʯī���뷨����ѧ����������ȡ�ʯīϩ�����ģ��ʾ��ͼ���£�
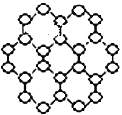
��1�������й�ʯīϩ��˵����ȷ����_________
A.12gʯīϩ����ѧ����ΪNA
B.ʯīϩ����������ԭ�ӿ��Դ���ͬһƽ��
C.��ʯī�����ʯīϩ��˷�ʯī�����֮��ķ��Ӽ�������
D.ʯīϩ��ÿ��Cԭ������3����Ԫ��,ÿ����Ԫ��ռ��6��Cԭ��
��2����ѧ����������ǻ�ô���ʯīϩ����Ч����֮һ,����Ϊ��ͭ���ܵȽ�����Ͻ�,��̼Դ�����Ǽ��顢��Ȳ�������Ҵ���̪ݼ���е�һ�ֻ�������ϡ�
�ٻ�̬ͭԭ��������ߵĵ���ռ�ݵ��ܼ�������_________����������Ԫ����,������������ͭԭ����ͬ��Ԫ�ػ���___________��
�����з������ڷǼ��Է��ӵ���__________��
a.����b.���ȼ��� c.��d.�Ҵ�
���Ҵ��ķе�Ҫ������Է���������������Ķ���,�����ԭ��____________________________��
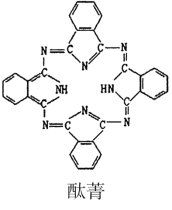
��̪ݼ��̪ݼͭȾ�Ϸ��ӽṹ����ͼ��,̪ݼ������̼ԭ�Ӳ��õ��ӻ���ʽ��____��
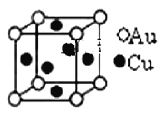
�ݽ���ͭ���γɵĽ���������Ͻ�(��ͼ),���Ļ�ѧʽ�ɱ�ʾΪ_________����Au��Χ�����������ȵ�Cu��_____��,��2��Cuԭ�Ӻ˵���С����Ϊd pm,�þ�����ܶȿ��Ա�ʾΪ__________g/cm3��(����٤��������NA��ʾ).
���𰸡�BC 3d K��Cr a��c �Ҵ����Ӽ���γ������������Ӽ䲻���γ���� sp2 Cu3Au��AuCu3 12 ![]()
��������
��1��A��ʯīϩ��һ��̼ԭ�Ӿ���1.5������������12gʯīϩ��������Ϊ1.5NA��ѡ��A����
B��̼̼˫��������ԭ�Ӷ�����ͬһƽ�棬���Ե���ʯīϩ����������ԭ�ӿ��Դ���ͬһƽ�棬ѡ��B��ȷ��
C��ʯī�ṹ�У�ʯī�����֮����ڷ��Ӽ������������Դ�ʯī�����ʯīϩ��˷�ʯī�����֮��ķ��Ӽ���������ѡ��C��ȷ��
D��ʯīϩ��������С�Ļ�Ϊ��Ԫ����ÿ��̼ԭ������3��C-C��ѧ������ÿ��Cԭ������3����Ԫ����ÿ����Ԫ��ռ�е�Cԭ����Ϊ6��![]() =2��ѡ��D����
=2��ѡ��D����
��ѡBC��
��2����ͭ��29��Ԫ�أ����̬ԭ�ӵĵ����Ų�ʽΪ��1s22s22p63s23p63d104s1����̬ͭԭ��������ߵĵ���ռ�ݵ��ܼ�������3d��
��������Ԫ����,������������ͭԭ����ͬ��Ԫ�ػ���K��Cr;
��a.����Ϊ��������ṹ���ṹ�Գƣ�������ɵ������غϣ����ڷǼ��Է��ӣ�ѡ��a��ȷ��
b.���ȼ���Ϊ��������ӣ��ṹ���Գƣ�������ɵ����IJ��غϣ����ڼ��Է��ӣ�ѡ��b����
c.��Ϊƽ���������Σ��ṹ�Գƣ�������ɵ������غϣ����ڷǼ��Է��ӣ�ѡ��c��ȷ��
d.�Ҵ��ṹ���Գƣ�������ɵ����IJ��غϣ����ڼ��Է��ӣ�ѡ��d����
��ѡac��
���Ҵ����Ӽ���������ʹ�����ۡ��е�����,��������Ӽ䲻���������
��̪ݼ������̼ԭ���γ�3��������1�����������Բ�ȡsp2�ӻ���̪ݼͭ���������ṩ�µ��ӶԵĵ�ԭ�Ӳ�����λԭ�ӣ�����̪ݼͭ��������ԭ�ӵ���λ��Ϊ2��
�ݸþ����к�ͭԭ�Ӹ���Ϊ6![]() =3�����н�ԭ����Ϊ8
=3�����н�ԭ����Ϊ8![]() =1,�����仯ѧʽΪCu3Au��AuCu3������ͼʾ��ͭԭ����Χ�����������ȵĽ�ԭ����4�������ݻ�ѧʽ����Au��Χ�����������ȵ�Cu��12������2��ͭԭ�Ӻ˵���С����Ϊd pm�������ⳤΪ
=1,�����仯ѧʽΪCu3Au��AuCu3������ͼʾ��ͭԭ����Χ�����������ȵĽ�ԭ����4�������ݻ�ѧʽ����Au��Χ�����������ȵ�Cu��12������2��ͭԭ�Ӻ˵���С����Ϊd pm�������ⳤΪ![]() d pm=
d pm=![]() d
d![]() 10-10 cm, �þ�����ܶ�=
10-10 cm, �þ�����ܶ�=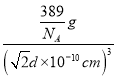 =
=![]() ��
��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����2.32g Na2CO3��NaOH�Ĺ���������ȫ�ܽ���ˮ���Ƴ���Һ��Ȼ�������Һ����μ���1 mol/L�����ᣬ�����������������CO2�����(��״��)��ϵ����ͼ��ʾ������˵���д������

A. OA�η�����Ӧ�����ӷ���ʽΪ:H����OH��===H2O CO32-��H��===HCO3-
B. ������35mL����ʱ������CO2�����Ϊ224mL
C. A����Һ�е�����ΪNaC1��NaHCO3
D. �������NaOH������0.60g
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��X(g)+2Y(g) ![]() 3Z(g)��H=-akJmol��1��a��0��������˵������ȷ����
3Z(g)��H=-akJmol��1��a��0��������˵������ȷ����
A.���߷�Ӧ�¶ȣ��淴Ӧ������������Ӧ���ʼ�С
B.�ﵽ��ѧƽ��״̬ʱ��X��Y��Z��Ũ�Ȳ��ٷ����仯
C.1molX��2molY��ȫ��Ӧ����3mol��Z���ų�akJ������
D.0.1molX��0.2molY��ַ�Ӧ����Z�����ʵ���һ��С��0.3mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����100 mLϡ�����ϡ����Ļ������Һƽ���ֳ����ݡ�������һ��������ͭ�ۣ�������ܽ�9.6 gͭ��(�����ʱ����ֻ����ԭΪNO����ͬ)������һ�����������ۣ�����������������������ı仯��ͼ��ʾ���������ж��д������
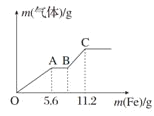
A.OA�����������NO��BC�����������H2
B.A���Ӧ����NO3-���ʵ���Ϊ0.2 mol
C.B���Ӧ�������۵�����Ϊ8.4 g
D.ԭ�������Һ��H2SO4��Ũ��Ϊ4.0 mol��L��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʱ�䣬ȫ����Χ�ڵ�������������Ӱ�������ǵ����彡������������Խ��Խ�ܵ����ǵ����ӡ�����β���к��н϶��NO��CO�������������ʹ�����ж������������е���Ⱦ��������������������ս�ǵ�ǰ����Ҫ����
��ش���������
(1)һ����̼������������Ҫ����Դ��Ҳ���Դ���ԭNO��������Ⱦ����������һ����������ȡCH3OH��
��֪����N2(g)+O2(g)===2NO(g) ��H=+180.5kJ��mol��1��
��2H2(g)+ O 2(g)===2H2O(1) ��H=��571.6kJ��mol��1��
��H2O(g)===H2O(1) ��H=��44kJ��mol��1��
д��H2��NO��Ӧ����N2��ˮ�������Ȼ�ѧ����ʽ��______________________��
(2)CO�����ںϳɼ״�����Ӧ����ʽΪCO(g)+2H2(g)![]() CH3OH(g)�����ܱ������г���10 mol CO��20molH2���ڴ��������·�����Ӧ���ɼ״����ı����������CO��ƽ��ת�������¶�(T)��ѹǿ(p)�Ĺ�ϵ��ͼ��ʾ����÷�Ӧ�ġ�H___________0(����>������<��)�����ﵽƽ��״̬Aʱ�����������Ϊ10L������ƽ��״̬Bʱƽ�ⳣ��K=___________����ʱ���������Ϊ___________L��
CH3OH(g)�����ܱ������г���10 mol CO��20molH2���ڴ��������·�����Ӧ���ɼ״����ı����������CO��ƽ��ת�������¶�(T)��ѹǿ(p)�Ĺ�ϵ��ͼ��ʾ����÷�Ӧ�ġ�H___________0(����>������<��)�����ﵽƽ��״̬Aʱ�����������Ϊ10L������ƽ��״̬Bʱƽ�ⳣ��K=___________����ʱ���������Ϊ___________L��

(3)��ҵ�ϲ��ü�ѹ�����£��ں���ȴװ�õ��������У���ȥ����ˮΪ���ռ�����NO���õ�40%�����ᡣԭ�����£�
2NO(g)+O2(g)![]() 2NO2(g) ��H=��114 kJ/mol
2NO2(g) ��H=��114 kJ/mol
3NO2(g)+H2O(��)![]() 2 HNO3(aq)+ NO(g) ��H=��69 92 kJ/molo
2 HNO3(aq)+ NO(g) ��H=��69 92 kJ/molo
���ý��²���������ԭ����_________________________________��
(4)���õ��ԭ��Ҳ���Դ���������������ͼΪ��ҵ����ģ��װ�á�����A��BΪ��缫(��ӵ�Դδ����)����AΪ___________��(����������������������������)���缫��ӦʽΪ______________________������Һ�����ʵijɷ�Ϊ___________(�ѧʽ)��

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������![]() ������־
������־![]() ����־
����־![]() ���������й��ڰ�ͭ�ļ��أ���������ͭ
���������й��ڰ�ͭ�ļ��أ���������ͭ![]() ͭ���Ͻ�
ͭ���Ͻ�![]() �������⣬����Ҫ������ң������������������Ʒ
�������⣬����Ҫ������ң������������������Ʒ![]() �ش��������⣺
�ش��������⣺
![]() ��Ԫ�ػ�̬ԭ�ӵĵ����Ų�ʽΪ______��3d�ܼ��ϵ�δ�ɶԵ�����Ϊ______��
��Ԫ�ػ�̬ԭ�ӵĵ����Ų�ʽΪ______��3d�ܼ��ϵ�δ�ɶԵ�����Ϊ______��
![]() ���������ڰ�ˮ�γ�
���������ڰ�ˮ�γ�![]() ��ɫ��Һ��
��ɫ��Һ��
![]() �������ӵ����幹����______��
�������ӵ����幹����______��
![]() ��
��![]() ��
��![]() ��
��![]() ֮���γɵĻ�ѧ����Ϊ___���ṩ�µ��ӶԵijɼ�ԭ����______��
֮���γɵĻ�ѧ����Ϊ___���ṩ�µ��ӶԵijɼ�ԭ����______��
![]() ����______����
����______����![]() ���������������Ǽ�����
���������������Ǽ�����![]() ������ԭ�ӵĹ���ӻ�����Ϊ______��
������ԭ�ӵĹ���ӻ�����Ϊ______��
![]() ����ͭ����������______���γɵľ��壻Ԫ��ͭ�����ĵڶ������ֱܷ�Ϊ��
����ͭ����������______���γɵľ��壻Ԫ��ͭ�����ĵڶ������ֱܷ�Ϊ��![]() ��
��![]() ��ԭ����______��
��ԭ����______��
![]() ij����ͭ�Ͻ�����������ṹ��ͼ��ʾ��
ij����ͭ�Ͻ�����������ṹ��ͼ��ʾ��
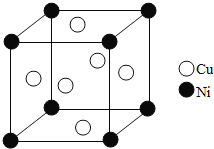
![]() ������ͭԭ������ԭ�ӵ�������Ϊ______��
������ͭԭ������ԭ�ӵ�������Ϊ______��
![]() ���Ͻ���ܶ�Ϊ
���Ͻ���ܶ�Ϊ![]() ����������
����������![]() ______nm��
______nm��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�о���ѧϰС�����ۼס��ҡ�����������ʵ��װ�õ��й��÷���������ȷ����
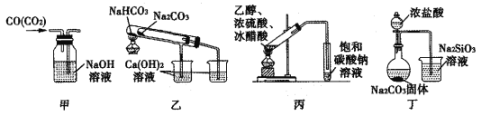
A.��װ�ã���������ȥCO�����е�CO2����
B.��װ�ã���������֤NaHCO3��Na2CO3�����ȶ���
C.��װ�ã�������ʵ�����Ʊ���������
D.��װ�ã��������Ƚ�HC1��H2CO3��H2SiO3������ǿ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������һЩԪ�ص���Ϣ��������һ��Ԫ�ز��ڶ����ڡ�
Ԫ��A | Ԫ��B | Ԫ��C | Ԫ��X | Ԫ��Y |
������һ�ֳ�����������Ԫ��X�γɺ�ɫ�ͺ���ɫ���ֳ��������� | ��̬ԭ��M��p�������5������ | �������н�������ǿ����X��Ӧ���������ֳ��������� | �������������ڲ��������3�������γ�˫ԭ�������� | ����Ϊ˫ԭ�ӷ��ӣ��ṹ������������Ŀ��Ϊ1:2 |
����������Ϣ�ش��������⣺
��1��д��X3�ĵȵ�����_____(дһ������)����̬Yԭ�Ӻ��������ռ�ݵ�����ܼ��ĵ�������״Ϊ______��
��2��AԪ����Ԫ�����ڱ��е�___������̬Aԭ�ӵ�δ�ɶԵ�����___����
��3��B��C��X�ļ����Ӱ뾶�ɴ�С��˳��Ϊ______�������ӷ��ţ���
��4��HX��HY���ֹ��ۼ��У����ļ��Խ�ǿ����____�������ϳ�����____��X��Y��Ԫ�ط��ű�ʾ����
��5��Y��̼Ԫ���γɵ�һ����������Y2�ǵȵ����壬��д���������ӵĵ���ʽ___��Y�ij����⻯��������ˮ����Ҫԭ����___��
��6����˿պȡ������CB�ھƾ��������գ������___ɫ����ɫԭ����___������ţ���
A��CB���Ȼӷ� B��CB���ȷֽ�
C��C�����е���ԾǨ D��B�����е���ԾǨ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��NA���������ӵ�������ֵ������˵����ȷ����
A.��0.1mol CO2����������ˮ����Һ��CO32-��HCO3-��H2CO3��������Ϊ0.1NA
B.��7.8gNa2O2��Na2S�Ļ�����У���������Ϊ0.3NA
C.ʹ0.5mol��ϩ��������Ȼ�̼��Һ��ȫ���գ����ѵĹ��ۼ�����Ϊ0.5NA
D.��״���£�2.24L Cl2��CH4��Ӧ��ȫ�������������������ĿС��0.1NA
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com