
 Cl2(g)��CO(g)����H����108 kJ��mol��1����Ӧ��ϵ�ﵽƽ������ʵ�Ũ���ڲ�ͬ�����µı仯״������ͼ��ʾ(��10 min��14 min��COCl2Ũ�ȱ仯����δʾ��)��
Cl2(g)��CO(g)����H����108 kJ��mol��1����Ӧ��ϵ�ﵽƽ������ʵ�Ũ���ڲ�ͬ�����µı仯״������ͼ��ʾ(��10 min��14 min��COCl2Ũ�ȱ仯����δʾ��)��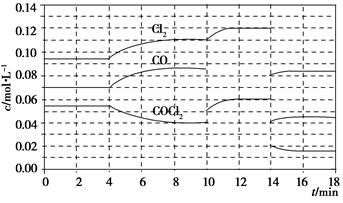
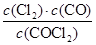 ��0.234��(2)��
��0.234��(2)��

 ���Ͱ�ͨ�������Сѧ��ʱͬ�����ϵ�д�
���Ͱ�ͨ�������Сѧ��ʱͬ�����ϵ�д� ���Ͱ�ͨ������ϵ�д�
���Ͱ�ͨ������ϵ�д� �ٷ�ѧ����ҵ��������ϵ�д�
�ٷ�ѧ����ҵ��������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 2C(g)+D(g),��2 min B��Ũ�ȼ���0.6 mol��L-1���Դ˷�Ӧ���ʵ���ȷ��ʾ��(����)
2C(g)+D(g),��2 min B��Ũ�ȼ���0.6 mol��L-1���Դ˷�Ӧ���ʵ���ȷ��ʾ��(����)�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
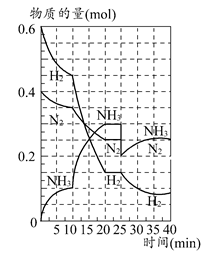
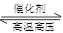 2NH3��ƽ�ⳣ��K����ֵΪ________�������¶Ȳ��䣬��Ӧ������25 minʱ����ȥ0.1 mol������ʱƽ�ⳣ��K��________(�������С�����䡱)������������䣬�ﵽ��ƽ��������Ӧ�Ļ�ѧ��Ӧ���ʱ�ԭƽ��״̬________(���С�����䡱)��
2NH3��ƽ�ⳣ��K����ֵΪ________�������¶Ȳ��䣬��Ӧ������25 minʱ����ȥ0.1 mol������ʱƽ�ⳣ��K��________(�������С�����䡱)������������䣬�ﵽ��ƽ��������Ӧ�Ļ�ѧ��Ӧ���ʱ�ԭƽ��״̬________(���С�����䡱)���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 cC(g)��5minʱ�����CΪxmol������˵����һ����ȷ����(����)
cC(g)��5minʱ�����CΪxmol������˵����һ����ȷ����(����)�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
| t/s | 0 | 50 | 150 | 250 | 350 |
| n(PCl3)/mol | 0 | 0.16 | 0.19 | 0.20 | 0.20 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
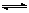 2C(g)��D(g) ���ֽ�5molA��10molB����һ���Ϊ2L���ܱ������У���Ӧ��10minʱ�ı�ijһ������C�����ʵ���Ũ����ʱ��仯��ϵ��ͼ��ʾ��
2C(g)��D(g) ���ֽ�5molA��10molB����һ���Ϊ2L���ܱ������У���Ӧ��10minʱ�ı�ijһ������C�����ʵ���Ũ����ʱ��仯��ϵ��ͼ��ʾ��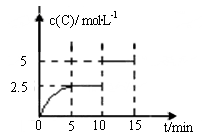
| A����0��5min�ڣ�����Ӧ���������� |
| B����Ӧ����ʼ��5minʱ��B��ת����Ϊ50% |
| C��5minʱ��ƽ�ⳣ����10minʱ��ƽ�ⳣ������ |
| D����15minʱ��B���������Ϊ25% |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 C��g����2D��g������5min���������B��Ũ�ȼ�����0.2mol��L��1����������������ȷ���ǣ� ��
C��g����2D��g������5min���������B��Ũ�ȼ�����0.2mol��L��1����������������ȷ���ǣ� ��| A����5min�ڸ÷�Ӧ��C��Ũ�ȱ仯��ʾ�ķ�Ӧ����Ϊ 0.02mol����L��min����1 |
| B����5minʱ��������D��Ũ��Ϊ0.2mol��L��1 |
| C���ÿ��淴Ӧ�淴Ӧ�Ľ��У�������ѹǿ������ |
| D��5minʱ�����������ܵ����ʵ���Ϊ3mol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 CH3OH(g)��H2O(g)����H����49.0 kJ��mol��1�����H2��CH3OH(g)��Ũ����ʱ��仯���±���ʾ������˵������ȷ����(����)
CH3OH(g)��H2O(g)����H����49.0 kJ��mol��1�����H2��CH3OH(g)��Ũ����ʱ��仯���±���ʾ������˵������ȷ����(����)| ʱ��/min | c(H2)/mol��L��1 | c(CH3OH)/mol��L��1 | v(��)��v(��)�Ƚ� |
| t0 | 6 | 0 | �� |
| t1 | 3 | 1 | v(��)��v(��) |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com