
����Ŀ���Ȼ�����Ʒ�к�������̼��ء�����غͲ�����ˮ�����ʡ�Ϊ���ᴿ�Ȼ��أ��Ƚ���Ʒ��������ˮ�У���ֽ������ˣ��ٽ���Һ������ͼ��ʾ������в������ش��������⣺

��1���Լ���Ļ�ѧʽΪ_______��
��2���Լ���Ļ�ѧʽΪ_______�����м����Լ����Ŀ���dz�ȥA�е�____������������Ѿ������ķ�����________________________________________________________��
��3�����з�����Ӧ�Ļ�ѧ����ʽΪ_________________________________________________��
��4����E�õ�KCl�����ʵ�������_______________��
���𰸡�BaCl2K2CO3Ba2+���ú�ȡ�����ϲ������Һ���Թ��У��μ�Na2SO4��Һ�����������֣�˵��Ba2+�ѳ���K2CO3+2HCl=CO2��+H2O+2KCl�����ᾧ
��������
�Ȼ�����Ʒ�к�������̼��ء�����غͲ�����ˮ�����ʣ���ȥ̼������Ӻ���������ӣ���Ҫ��������Ȼ�����Һ��Ϊ���ᴿ�Ȼ��أ��Ƚ���Ʒ��������ˮ�У���ֽ������ˣ���ʵ�����̿�֪����Һ�м��Լ�IΪ����BaCl2��Ȼ����˺�B��̼�ᱵ�����ᱵ��A�к��Ȼ������Ȼ��أ��ټ��Լ���Ϊ����K2CO3�����˺�C��Ϊ̼�ᱵ��Ȼ����ˣ�D�к�̼��ء�KCl���ټ����Լ���Ϊ�������ᣬ��ȥ������̼��أ����ͨ������Ũ���������ᾧ�õ�KCl���壬�Դ������
��1���������Ϸ�����֪�Լ������Ȼ�������ѧʽΪBaCl2��
��2���Լ�����̼��أ���ѧʽΪK2CO3��Ŀ���dz�ȥA�е�Ba2+�����鱵�����Ѿ������ķ����Ǿ��ú�ȡ�����ϲ������Һ���Թ��У��μ�Na2SO4��Һ�����������֣�˵��Ba2+�ѳ�����
��3�����м���������Ϊ�˳�ȥ������̼��أ�������Ӧ�Ļ�ѧ����ʽΪK2CO3+2HCl��CO2��+H2O+2KCl��
��4���Ȼ���������ˮ������E�õ�KCl�����ʵ������������ᾧ��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Ȼ��Ŀ����ʯ�ij���ͱ仯�ܶ���������Ӱ�졣�ؿ���ÿ����1![]() ,ѹǿ����Լ25000~30000KPa���¶�����25��30���϶ȡ��ڵؿ���SiO2��HF��������ƽ��: SiO2(s)+4HF(g)
,ѹǿ����Լ25000~30000KPa���¶�����25��30���϶ȡ��ڵؿ���SiO2��HF��������ƽ��: SiO2(s)+4HF(g) ![]() SiF4(g)+2H2O(g) + 148.9KJ
SiF4(g)+2H2O(g) + 148.9KJ
������������������:
��1���÷�Ӧ�ġ�H________0���ڵؿ��������____________�����ݳ�����֪�˴��¶Ƚϸߣ���÷�ӦΪ _____________��Ӧ����Է����������Է���������ȷ������
��2�����������Ӧ��ƽ�ⳣ��Kֵ��÷�Ӧ__________(����)��
A.һ��������Ӧ�����ƶ�
B.���淴Ӧ����һ���ӿ�
C.ƽ���ƶ�����Ϊ������Ӧ������������С
D.ƽ���ƶ�����Ϊ���淴Ӧ�����ȼ�С������
��3�����������Ӧ�����������ܱ������з���������Ӧ�Ѿ��ﵽƽ��ʱ�����г�������_______ (����)��
a.2 v��(HF) = v��(H2O) b. v (H2O) = 2v (SiF4)
c. SiO2���������ֲ��� d.��Ӧ�ﲻ��ת��Ϊ������
��4������Ӧ�����ݻ�Ϊ2.0L����Ӧʱ��8.0min��������������ܶ�������0.12g/L�������ʱ����HF��ƽ����Ӧ����Ϊ_____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���谢���ӵ�������ֵΪNA����֪�������������£������Ƿ�����ӦC6H12O6![]() 2CH3CH2OH��2CO2��������˵����ȷ���ǣ� ��
2CH3CH2OH��2CO2��������˵����ȷ���ǣ� ��
A. 0.1 mol������(C6H12O6)���ǻ�(��OH)��ĿΪ0.6NA
B. 10.0 g��������Ϊ46%�ľƾ����������Ʒ�Ӧ�����������Ϊ0.05NA
C. ���³�ѹ�£�4.48 L CO2��NO2�Ļ�����庬ԭ������Ϊ0.6NA
D. 4.8 g Mg��������CO2����ȫȼ�գ�ת�Ƶ�����ĿΪ0.4NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��±�ؼ��仯����㷺��������Ȼ���С��ش��������⣺
(1)����(COCl2)��һ����Ҫ���л��м��壬��ũҩ��ҽҩ���������ϡ��۰��������Լ������϶���������;�������ķ������幹��Ϊ______________��������Ԫ�صĵ縺����С�����˳��Ϊ______________����COCl2��Ϊ�ȵ�����ķ��Ӻ�����(��дһ��)__________��
(2)�ճ������У�����������ɼ��⣬����ƣ��Դ�ԭ�ӽṹ�ǶȽ�����һ����____________________________��
(3)���־�̬��������ͷǾ�̬����������ɿ��Ŀ�ѧ������_____________��
(4)һ��ͭ���廯�ᄃ���ṹ��ͼ��ʾ������ͼ�е�Cuȥ�����ٰ����е�Br����Cu���õ�����ͭ�ľ����ṹ������ͭ�Ķѻ���ʽΪ___________��ijͬѧ����̬ͭԭ�Ӽ۵��Ӵ����дΪ3d94s2��Υ���˺�������Ų������е�______��
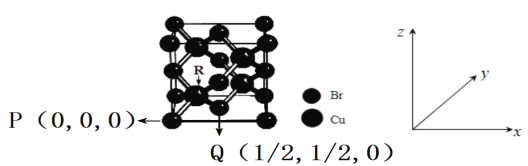
(5)���й�������ͭ���廯�ᄃ���ṹ˵����ȷ����_________(ѡ����ĸ���)��
A���û�����Ļ�ѧʽΪCuBr2
B��ͭ����λ��Ϊ8
C����ÿ��Br���ڵ�Br��12��
D����ͼ��P���Q���ԭ�����������ȷ��R���ԭ���������Ϊ(1/4,1/4,1/4)
(6)��ͼ��P���R���ԭ�Ӻ˼��Ϊa cm��NAΪ����٤��������ֵ����þ����ܶ�Ϊ______g/cm3��(�г�����ʽ����)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����з�Ӧͨ��ԭ���װ�ã���ʵ�ֻ�ѧ��ֱ��ת��Ϊ���ܵ���
A.Fe+H2SO4=FeSO4+H2��B.2NaOH+H2SO4=Na2SO4+2H2O
C.CaCO3+2HC1=CaCl2+H2O+CO2��D.BaCl2+Na2SO4=BaSO4��+2NaCl
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������з�Ӧ�У�ˮ�Ȳ�����������Ҳ���ǻ�ԭ������
A��2Na+2H20��2Na0H+H2�� B��C12+H20��HC1+HC10
C��2F2+2H20=4HF+02 D��2H20![]() 2H2��+02��
2H2��+02��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ���¶��£���һ���ݻ����ܱ������м���NH3��O2��1mol��������Ӧ��4NH3��g��+5O2��g��![]() 4NO��g��+6H2O��g��������˵���У������÷�Ӧ�ﵽ��ѧƽ��״̬����
4NO��g��+6H2O��g��������˵���У������÷�Ӧ�ﵽ��ѧƽ��״̬����
A. NO��H2OŨ�ȱȲ��ٱ仯 B. v(NH3)����v(NH3)��
C. ������ܶȲ��ٱ仯 D. v(NH3)����v(O2)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ӷ���ʽ��д������ǣ� ��
A.��������⣺![]()
B.����ͨ��NaOH��Һ�У�![]()
C.��KOH��Һ�м���![]() ��Һ��
��Һ��![]()
D.��![]() ��Һ�м������ϡ���
��Һ�м������ϡ���![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������Ԫ��W��X��Y��Z��R��ԭ��������������A��B��C��D��E��F����������Ԫ����ɵ���ѧ��ѧ�������ʣ�����A����Ԫ�����C����ʹʪ���ɫʯ����ֽ���������壬D����Ư���ԣ�E�ǵ��ʡ�������֮�������ͼת����ϵ(���ֲ���δ���)������˵������ȷ���ǣ� ��

A. �����Ӱ뾶��С��ϵ��Y��Z��RB. �������ӵĻ�ԭ�ԣ�W��Y��Z
C. �⻯��ķе㣺Z��Y��XD. C��E��Ӧ����F�ǹ�ҵ���������Ҫ��Ӧ֮һ
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com