
下列关于判断过程的方向的说法错误的是( )
|
| A. | NH4NO3溶于水吸热,说明其溶于水不是自发过程 |
|
| B. | 同一种物质气态时熵值最大,液态时次之,而固态时熵值最小 |
|
| C. | 不借助于外力能自发进行的过程,其体系的能量趋向于从高能状态转变为低能状态 |
|
| D. | 由焓判据和熵判据组合而成的复合判据,更适合于所有的过程 |
| 焓变和熵变. . | |
| 专题: | 化学反应中的能量变化. |
| 分析: | A、反应能否自发取决于焓变和熵变的复合判据; B、同一物质的固、液、气三种状态的熵值依次增大; C、物质的转化过程就是使物质趋向稳定的过程,物质的能量越低越稳定; D、根据△H﹣T△S是大于0还是小于0判断反应能否自发进行. |
| 解答: | 解:A、反应能否自发取决于焓变和熵变的复合判据,对于吸热过程,在一定温度下也能进行,故A错误; B、同一物质的固、液、气三种状态的熵值依次增大,故B正确; C、物质的转化过程就是使物质趋向稳定的过程,物质的能量越低越稳定,所以说不借助于外力能自发进行的过程,其体系的能量趋向于从高能状态转变为低能状态,故C正确; D、化学上就是根据△H﹣T△S是大于0还是小于0判断反应能否自发进行,故D正确. 故选:A. |
| 点评: | 本题考查反应热与焓变,题目难度不大,注意把握相关概念的理解. |


科目:高中化学 来源: 题型:
二甲醚是一种重要的清洁燃料,也可替代氟利昂作制冷剂等,对臭氧层无破坏作用。工业上可利用煤的气化产物(水煤气)合成二甲醚。请回答下列问题:
(1)煤的气化的主要化学反应方程式为: 。
(2)利用水煤气合成二甲醚的三步反应如下:
①2H2(g)+CO(g) 
 CH3OH(g) ΔH=-90.8kJ·mol-1
CH3OH(g) ΔH=-90.8kJ·mol-1
②2CH3OH(g) 
 CH3OCH3(g)+H2O(g) ΔH=-23.5kJ·mol-1
CH3OCH3(g)+H2O(g) ΔH=-23.5kJ·mol-1
③CO(g)+H2O(g) 
 CO2(g)+H2(g) ΔH=-41.3kJ·mol-1
CO2(g)+H2(g) ΔH=-41.3kJ·mol-1
写出水煤气直接合成二甲醚同时生成CO2的热化学反应方程式 。
(3)一定条件下的密闭容器中,该总反应达到平衡,要提高CO的转化率,可以采取的措施是 。
a.高温高压 b.低温低压 c.减少CO2的浓度
d.增加CO的浓度 e.分离出二甲醚 f.加入催化剂
(4)已知反应②2CH3OH(g) 
 CH3OCH3(g)+H2O(g)某温度下的平衡常数为400。此温度下,在密闭容器中加入CH3OH,反应到某时刻测得各组分的浓度如下:
CH3OCH3(g)+H2O(g)某温度下的平衡常数为400。此温度下,在密闭容器中加入CH3OH,反应到某时刻测得各组分的浓度如下:
| 物质 | CH3OH | CH3OCH3 | H2O |
| 浓度/(mol·L-1) | 0.44 | 0.6 | 0.6 |
比较此时正、逆反应速率的大小:v(正) v(逆)(填“>”、“<”或“=”),若上述情况达到平衡,此时c(CH3OH)= 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法合理的是 ( )
A.在稀硫酸中加入铜粉,铜粉不溶解;再加入K NO3 固体,铜粉仍不溶解
B.将等物质的量Cl2与SO2通入品红溶液,漂白性增强
C.浓H2SO4与Cu或C反应都需加热,浓硝酸与Cu或C反应都不需加热
D.铝、氧化铝、小苏打、醋酸铵都既能与盐酸又能与氢氧化钠溶液反应
查看答案和解析>>
科目:高中化学 来源: 题型:
 A、B、C、D、E、F是中学化学中常见的六种短周期元素,有关位置及信息如下:A的最高价氧化物对应的水化物与其氢化物反应生成离子化合物;C单质一般保存在煤油中;F的最高价氧化物对应的水化物既能与酸反应又能与碱反应,G单质是日常生活中用量最大的金属,易被腐蚀或损坏。请回答下列问题:
A、B、C、D、E、F是中学化学中常见的六种短周期元素,有关位置及信息如下:A的最高价氧化物对应的水化物与其氢化物反应生成离子化合物;C单质一般保存在煤油中;F的最高价氧化物对应的水化物既能与酸反应又能与碱反应,G单质是日常生活中用量最大的金属,易被腐蚀或损坏。请回答下列问题:
(1)A元素的氢化物水溶液能使酚酞变红的原因用电离方程式解释为 。
(2)同温同压下,将a L A氢化物的气体和b L D的氢化物气体通入水中,若所得溶液的pH=7,
则a b(填“>"或“<”或“=”)
(3)常温下,相同浓度F、G简单离子的溶液中滴加NaOH溶液,F、G两元素先后沉淀,F (OH)n完全沉淀的pH是4.7,G (OH)n完全沉淀的pH是2.8,则ksp较大的是: (填化学式)
(4)A与B可组成质量比为7:16的三原子分子,该分子释放在空气中其化学作用可能引发的后果有: 。
①酸雨 ②温室效应 ③光化学烟雾 ④臭氧层破坏
(5)A和C组成的一种离子化合物,能与水反应生成两种碱,该反应的化学方程式是 。
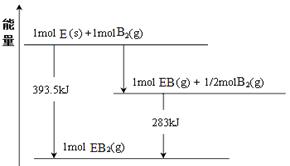
(6)已知一定量的E单质能在B2 (g)中燃烧,其可能的产物及能量关系如下左图所示:请写出一定条件下EB2(g) 与E(s)反应生成EB(g)的热化学方程式 。

(7)若在D与G组成的某种化合物的溶液甲中,加入铜片,溶液会慢慢变为蓝色,依据产生该现象的反应原理,所设计的原电池如上右图所示,其反应中正极反应式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
合成氨所需的氢气可由水煤气反应制得,其中的一步反应为:CO(g)+H2O(g)⇌CO2(g)+H2(g);△H=﹣43kJ•mol﹣1对于上述反应,下列措施中能提高CO转化率的是( )
|
| A. | 增大压强 | B. | 升高温度 |
|
| C. | 增大水蒸气的浓度 | D. | 增大CO的浓度 |
查看答案和解析>>
科目:高中化学 来源: 题型:
298K、10lkPa时,1molH2(g)与O2(g)完全反应生成H2O(g)时放出242kJ热量,而生成H2O(1)时放出286kJ热量,则下列表达不正确的是( )
|
| A. | 2H2(g)+O2(g)=2H2O(g);△H=﹣484kJ•mol﹣1 | B. | H2O(g)=H2(g)+O2(g);△H=242kJ•mol﹣1 |
|
| C. | H2(g)+O2(g)=H2O(1);△H=﹣286kJ•mol﹣1 | D. | H2O(1)=H2O(g);△H=﹣44kJ•mol﹣1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
在一定温度下,在定压容器a与定容容器b中,分别通入等量且体积比为1:3的N2和H2,开始时体积相同,达到平衡时,N2的转化率是( )
|
| A. | a大 | B. | b大 | C. | a、b一样大 | D. | 不一定 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列涉及离子方程式书写的评价合理的是 ( )
| 选项 | 化学反应及离子方程式 | 评价 |
| A | 次氯酸钙溶液中通入足量SO2:Ca2++ClO-+SO2+H2O===CaSO4↓+Cl-+2H+ | 正确 |
| B | 实验室用浓盐酸与MnO2反应制Cl2:MnO2+4H++2Cl- | 错误,H+、Cl-的化学计量数应相等 |
| C | 硝酸铁溶液中加过量氨水:Fe3++3NH3·H2O===Fe(OH)3(胶体)+3NH | 错误,Fe(OH)3应该是沉淀 |
| D | 铝溶于碳酸中:2Al+3H2CO3===2Al3++3H2↑+3CO | 正确 |
查看答案和解析>>
科目:高中化学 来源: 题型:
一定条件下,可逆反应X(g)+3Y(g) 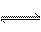 2Z(g),若X、Y、Z起始浓度分别为c1、c2、c3(均不为0),当达平衡时X、Y、Z的浓度分别为0.1mol /L,0.3mol/ L,0.08 mol/L,则下列判断不合理的是
2Z(g),若X、Y、Z起始浓度分别为c1、c2、c3(均不为0),当达平衡时X、Y、Z的浓度分别为0.1mol /L,0.3mol/ L,0.08 mol/L,则下列判断不合理的是
A.c1:c2=1:3 B.平衡时,Y和Z的生成速率之比为3:2
C.X、Y的转化率不相等 D.c1的取值范围为0< c1 <0.14 mo /L
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com