
【题目】钴元素是三元锂离子电池阳极材料的重要成分。请回答下列问题:
(1)钴元素在周期表中的位置是_______,其价电子排布式为______。
(2)第四电离能大小:I4(Fe)> I4(Co),从原子结构的角度分析可能的原因是____。
(3)取1mol配合物CoCl3·6NH3(黄色)溶于水,加入足量硝酸银溶液,产生3mol白色沉淀,沉淀不溶于稀硝酸。原配合物中络离子形状为正八面体。
①根据上述事实推测原配合物中络离子化学式为_______。
②该配合物在热NaOH溶液中发生反应,并释放出气体,该反应的化学方程式_____;生成气体分子的中心原子杂化方式为____。
(4)经X射线衍射测定发现,晶体钴在417℃以上堆积方式的剖面图如图所示,则该堆积方式属于_____,若该堆积方式下钴原子的半径为r,则该晶体的空间利用率为______(列出表达式并写出最终结果)。
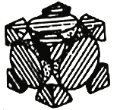
【答案】第四周期VIII族 3d74s2 Fe3+电子排布较稳定的3d5变为不稳定的3d4需要更多的能量 [Co(NH3)6]3+ [Co(NH3)6]Cl3+3NaOH=Co(OH)3↓+6NH3+3NaCl sp3 面心立方堆积 ![]()
【解析】
(1)钴的原子序数为27,依据元素周期表的结构及原子核外电子排布规律作答;
(2) 根据洪特规则易知,核外电子处于半充满或全充满状态比较稳定,结合电离能的定义作答;
(3)①依据题意判断出Cl-是外界离子,不是配位体;再结合络离子形状为正八面体进行推测;
②根据以上分析,该配合物为[Co(NH3)6]Cl3,与热NaOH溶液中发生反应,放出气体应为氨气;再根据价层电子对互斥理论与杂化轨道理论结合推测其杂化方式;
(4)依据金属原子常见的堆积模型判断;根据几何关系找出晶胞立方体面对角线长为4r,若该堆积方式下的晶胞参数为acm,则(4r)2=a2+a2,再根据空间利用率=![]() 计算作答。
计算作答。
(1)钴的原子序数为27,在周期表中位于第四周期VIII族,电子排布式为1s22s22p63s23p63d74s2,其外围电子排布式为3d74s2;
故答案为:第四周期VIII族;3d74s2;
(2) Fe3+外围电子排布式为3d5,Co3+外围电子排布式为3d6,由此可知Fe3+从电子排布较稳定的3d5变为不稳定的3d4需要更多的能量,所以第四电离能大小:I4(Fe)> I4 (Co);
故答案为:Fe3+电子排布较稳定的3d5变为不稳定的3d4需要更多的能量;
(3)①1mol配合物CoCl3·6NH3(黄色)溶于水,加入足量硝酸银溶液,产生3mol白色沉淀,沉淀不溶于稀硝酸,说明Cl-是外界离子,不是配位离子;络离子形状为正八面体,则说明Co3+与6个NH3形成配位络离子,则络离子化学式为[Co(NH3)6]3+,
故答案为:[Co(NH3)6]3+;
②根据以上分析,该配合物为[Co(NH3)6]Cl3,与热NaOH溶液中发生反应,放出气体应为氨气,则化学方程式[Co(NH3)6]Cl3+3NaOH=Co(OH)3↓+6NH3+3NaCl;NH3分子的中心原子的价电子对数为![]() =4,故杂化方式为sp3,
=4,故杂化方式为sp3,
故答案为:[Co(NH3)6]3+;[Co(NH3)6]Cl3+3NaOH=Co(OH)3↓+6NH3+3NaCl;sp3;
(4)由图可知,该堆积方式属于面心立方堆积;
钴原子在面心立方堆积中,钴原子处于顶点和面心,该堆积方式下的晶胞参数为acm,因钴原子的半径为r,则晶胞立方体面对角线长为4r,则依据几何关系可知(4r)2=a2+a2,解得r=![]() a cm,晶胞内钴原子数目=
a cm,晶胞内钴原子数目=![]() ,则其空间利用率=
,则其空间利用率=![]() ,
,
故答案为:面心立方堆积;![]() 。
。


科目:高中化学 来源: 题型:
【题目】双极膜(BP)是阴、阳复合膜,在直流电的作用下,阴、阳膜复合层间的H2O解离成H+和OH-,作为H+和OH-离子源。利用双极膜电渗析法电解食盐水可获得淡水、NaOH和HC1,其工作原理如下图所示,M、N为离子交换膜。

下列说法错误的是
A. 阴极室发生的反应为2H++2e-=H2↑
B. M为阳离子交换膜,N为阴离子交换膜
C. 若去掉双极膜(BP),阳极室会有C12生成
D. 电路中每转移1mol电子,两极共得到0.5 mol气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯气是一种重要的化工原料,自来水的消毒、农药的生产、药物的合成等都需要用氯气.
I.工业上通常采用电解法制氯气:观察下图,回答:
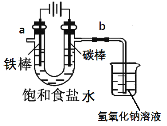
(1)电解反应的化学方程式为____________________。
(2)饱和食盐水通电后,b端产生的气体检验方法是____________。
II. 实验室用NaOH固体配制100 mL 1.0 mol·L-1的NaOH溶液,试回答下列各题:
(3)需要用托盘天平称量_______g NaOH固体;
(4)实验室有下列仪器:①漏斗 ②200mL容量瓶 ③烧杯 ④玻璃棒 ⑤药匙 ⑥托盘天平 ⑦冷凝。若要实施溶液配制,尚缺的玻璃仪器是___________、________;
(5)容量瓶在使用前必须先____________;
(6)配制过程有以下操作: ①称量 ②移液 ③冷却 ④洗涤 ⑤定容 ⑥溶解 ⑦摇匀 其正确的操作顺序应是:① →_________→________ →________ →________→________→ ⑦
(7)下列五项操作中会导致所得溶液浓度偏低的有____________(填序号);
①没有洗涤烧杯内壁和玻璃棒
②未冷却到室温就将溶液转移到容量瓶并定容
③在转移过程中有溶液撒在外面
④定容时观察液面时俯视
⑤定容后,把容量瓶反复摇匀后发现液面低于刻度线,便滴加几滴水至刻度处
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于晶体说法的正确组合是

①分子晶体中都存在共价键
②在晶体中只要有阳离子就一定有阴离子
③金刚石、SiC、NaF、NaCl、H2O、H2S晶体的熔点依次降低
④离子晶体中只有离子键没有共价键,分子晶体中肯定没有离子键
⑤CaTiO3晶体中(晶胞结构如上图所示)每个Ti4+和12个O2-紧邻
⑥SiO2晶体中每个硅原子与两个氧原子以共价键相结合
⑦晶体中分子间作用力越大,分子越稳定
⑧氯化钠熔化时离子键被破坏
A.①②③⑥ B.①②④
C.③⑤⑦ D.③⑤⑧
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在给定条件下,下列选项中所示的物质间转化能一步实现的是( )
A.Fe![]() Fe2O3
Fe2O3![]() Fe(OH)3B.Mg(OH)2
Fe(OH)3B.Mg(OH)2![]() MgCl2溶液
MgCl2溶液![]() Mg
Mg
C.NH3![]() NO
NO![]() NO2D.SO2
NO2D.SO2![]() (NH4)2SO4
(NH4)2SO4![]() BaSO4
BaSO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关物质的转化关系如下图所示,A为常见调味品,B为常见液体,C、E是金属。D、F为气态单质,其中D为黄绿色。J为红褐色固体,A、C、G、I、K的焰色反应均为黄色。K是一种含+6价元素的含氧酸盐,其摩尔质量为166 g·mol-1。
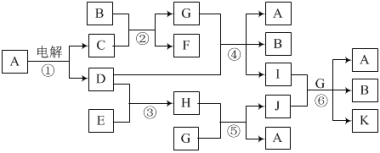
(1)物质B的电子式为___。物质D所含元素在周期表中的位置是___。
(2)写出反应②的化学方程式,并用单线桥表示电子转移的方向和数目:___。
(3)写出反应④的离子方程式:___。
(4)写出反应⑥的化学方程式:___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以粗硅(含硅、硼等)为原料制取四氯化硅(SiCl4)的装置示意图如下:
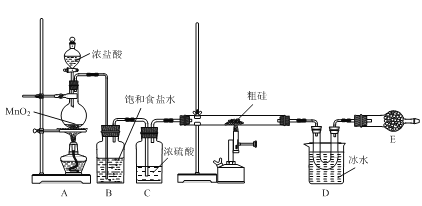
已知:①SiCl4遇水易反应;BCl3与SiCl4互溶。
②高温下硅、硼与氯气反应后所得物质的部分性质如表:
物质 | SiCl4 | BCl3 |
沸点/℃ | 57.7 | 12.8 |
熔点/℃ | -70.0 | -107.2 |
(1)装置A中盛装浓盐酸的仪器名称是___。
(2)用湿润的淀粉KI试纸可以检验Cl2,写出表示该反应原理的离子方程式:___。
(3)装置B中饱和食盐水的作用是___。
(4)装置D中收集到的物质,可用___方法分离出纯净的SiCl4。
(5)装置E中应装入的试剂名称是___,其作用有___、___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】300 mL Al2(SO4)3溶液中,含Al3+为1.62 g,在该溶液中加入0.1 mol·L-1Ba(OH)2溶液300 mL(忽略溶液体积变化),反应后溶液中SO42-的物质的量浓度为
A.0.4 mol·L-1B.0.1 mol·L-1C.0.2 mol·L-1D.0.3 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某烃结构式如图所示,有关其结构说法正确的是( )

A. 所有原子可能在同一平面上B. 最多有7个碳原子在同一条直线上
C. 所有碳原子可能在同一平面上D. 1 mol 该烃最多可与3 mol氢气反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com