
【题目】部分弱酸的电离平衡常数如下表所示:
弱酸 | HCOOH | HCN | H2CO3 |
电离平 衡常数(25 ℃) | K=1.77×10-4 | K=4.9×10-10 | K1=4.3×10-7 K2=5.6×10-11 |
下列选项正确的是( )
A.2CN-+H2O+CO2=2HCN+CO![]()
B.中和等体积、等pH的HCOOH和HCN消耗NaOH的量前者大于后者
C.物质的量浓度相等的HCOONa和KCN溶液中,c(Na+)-c(HCOO-)<c(K+)-c(CN-)
D.c(NH![]() )相等的HCOONH4溶液、NH4CN溶液、NH4HCO3溶液中:c(NH4HCO3)>c(NH4CN)>c(HCOONH4)
)相等的HCOONH4溶液、NH4CN溶液、NH4HCO3溶液中:c(NH4HCO3)>c(NH4CN)>c(HCOONH4)
科目:高中化学 来源: 题型:
【题目】下列有关化学与自然资源的开发利用描述中错误的是
A. 冶炼金属铁通常用热还原法
B. 要使海水淡化通常有蒸馏法和离子交换法
C. 用H2作为燃料的优点之一是燃烧后的产物不污染环境
D. 煤的干馏属于物理变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关丙烷的叙述中不正确的是( )
A. 光照下能够发生取代反应 B. 分子中所有碳原子一定在同一平面上
C. 是石油分馏的一种产品 D. 比丁烷更易液化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列事实能说明影响化学反应速率的决定性因素是反应物本身性质的是
A. Fe与浓盐酸反应比与稀盐酸反应快
B. Cu与浓硝酸反应比与稀硝酸反应快
C. N2与O2在常温、常压下不反应,放电时可反应
D. Cu能与浓硝酸反应,但不能与浓盐酸反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列框图所示的转化关系中,A、C均为常见的金属单质, E为固体非金属单质。B为棕红色固体氧化物,X为常见的无色液体。L焰色为黄色,且能使酚酞变红(反应过程中生成的水及其他产物已略去)

请回答以下问题:
(1)F的化学式为 ;
(2)I与氯水反应的离子方程式为 ;
(3)A与B生成C和D的反应是 (填“放出”或“吸收”)大量热量的反应;
(4)D与L反应的离子方程式为 。
(5)检验“黄色溶液”中金属阳离子的试剂是 (写化学式)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在给定温度和压强下的理想气体,影响其所占体积大小的主要因素是
A.分子直径的大小 B.分子间距离的大小
C.分子间引力的大小 D.分子数目的多少
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】容量瓶是用来配制物质的量浓度的溶液的定量仪器,其上标有:①温度 ②浓度 ③容量 ④压强⑤刻度线 ⑥酸式或碱式这六项中的( )
A.②④⑥
B.③⑤⑥
C.①②④
D.①③⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下面是甲、乙、丙三位同学制取乙酸乙酯的过程,请你参与并协助他们完成相关实验任务。
【实验目的】制取乙酸乙酯
【装置设计】甲、乙、丙三位同学分别设计了下列三套实验装置:

请从甲、乙两位同学设计的装置中选择一种作为实验室制取乙酸乙酯的装置,我选择的装置是 (选填 “甲”或 “乙”)。丙同学将甲装置中的玻璃管改成了球形干燥管除起冷凝作用外,它的另一重要作用是 。
【问题讨论】
a.根据试管②中观察到的现象,可知乙酸乙酯的物理性质有:
无色油状液体、 、 ;
b.试管②中饱和 Na2CO3 溶液的作用是 (填编号)。
A.溶解乙醇 B.降低乙酸乙酯的溶解度 C.中和乙酸
c.从试管②中分离出乙酸乙酯的实验操作是 。
d.生成乙酸乙酯的化学反应方程式 。
f.乙醇在铜或银作催化剂时,可以被氧化为一种有刺激性气味的物质,写出该反应的化学反应方程式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学设计如图装置,研究非金属元素性质变化规律。
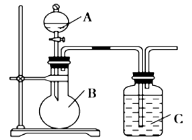
(1)已知硅酸(H2SiO3)是一种难溶于水的弱酸,呈白色。在化学反应中,强酸一般能制取弱酸。现有硝酸溶液、碳酸钙、澄清石灰水、硅酸钠溶液,选择所给试剂,用如上图装置来证明酸性:HNO3>H2CO3>H2SiO3。(不考虑硝酸的挥发性)
A、B、C中盛装的试剂分别为____________、____________、____________。C中实验现象为____________________;
写出C中发生反应的离子方程式:____________________。
(2)已知高锰酸钾在常温下与浓盐酸反应产生氯气,利用上图装置证明氯气氧化性强于碘单质的氧化性。A中盛装浓盐酸,B中装入高锰酸钾粉末,实验时C中溶液变成蓝色,则:C中盛装的试剂为_________________;写出C中离子方程式_____________________。该实验该装置有明显不足,请指出改进方法:__________________________。
(3)如果C中盛装饱和氢硫酸(H2S饱和水溶液),A中装浓盐酸,B中装高锰酸钾溶液,反应开始后观察到现象是C中产生淡黄色沉淀。写出该反应的化学方程式:_____________;如果将SO2气体通入到饱和氢硫酸溶液中,也会产生淡黄色沉淀,该过程体现SO2 (填序号)。
A.漂白性 B.氧化性 C.还原性 D.酸性
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com