
| A、钠:银白色,质软,熔点低,密度比水小 |
| B、钠着火时可以用沙子盖灭,少量的钠可保存在煤油中 |
| C、金属钠在空气中长期放置,最终变为碳酸钠 |
| D、氧化钠和过氧化钠都是白色固体,都是碱性氧化物 |


科目:高中化学 来源: 题型:
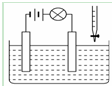 在电解质溶液的导电性装置(如图所示)中,若向某一电解质溶液中逐滴加入另一溶液时,出现灯泡由亮变暗,至熄灭后又逐渐变亮现象的是( )
在电解质溶液的导电性装置(如图所示)中,若向某一电解质溶液中逐滴加入另一溶液时,出现灯泡由亮变暗,至熄灭后又逐渐变亮现象的是( )| A、氢氧化钡溶液中逐滴加入硫酸 |
| B、氢氧化钠溶液中逐滴加入硫酸 |
| C、石灰乳中逐滴加入稀盐酸 |
| D、食盐溶液中逐滴加入盐酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、+4价 | B、+5价 |
| C、+6价 | D、+7价 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、AlCl3溶液中加入足量的氨水:Al3++3OH-═Al(OH)3↓ |
| B、氢氧化钡溶液与稀 H2SO4:Ba2++OH-+SO42-+H+═BaSO4↓+H2O |
| C、向氯化亚铁溶液中通入氯气:2Fe2++Cl2═2Fe3++2Cl- |
| D、过量氯气通入溴化亚铁溶液中2Fe2++2Br-+2Cl2═Fe3++Br2+4Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 物质 | 杂质 | 试剂或方法 | |
| A | NaHCO3溶液 | Na2CO3 | 通入过量的CO2 |
| B | FeCl3溶液 | CuCl2 | Fe |
| C | Fe2O3 | Al2O3 | 盐酸 |
| D | 碘水 | Br2 | 乙醇、萃取 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
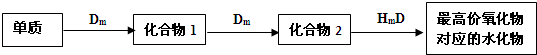
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 有A、B、C、D四种短周期主族元素,其原子序数依次增大.A、B可形成A2B和A2B2两种化合物,B、C同主族且可形成CB2和CB3两种化合物.完成下列问题.
有A、B、C、D四种短周期主族元素,其原子序数依次增大.A、B可形成A2B和A2B2两种化合物,B、C同主族且可形成CB2和CB3两种化合物.完成下列问题.查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com