
【题目】N、P、As等元素的化合物在生产和研究中有许多重要用途.请回答下列问题:
(1)意大利罗马大学的Cacace等人获得了极具理论研究意义的N4分子,该分子的空间构型与P4类似,其中氮原子的轨道杂化方式为______________________,N—N键的键角为______________________;
(2)基态砷原子的价电子排布图为______________________,砷与同周期相邻元素的第一电离能由大到小的顺序为______________________;
(3)配位原子对孤对电子的吸引力越弱,配体越容易与过渡金属形成配合物。PH3与NH3的结构相似,和过渡金属更容易形成配合物的是____________________(填“PH3”或“NH3”)。
(4)SCl3+和PCl3是等电子体,SCl3+的空间构型是____________________;S—Cl键键长 ______P-Cl键键长(填“>”、“=”或“<”),原因是____________________。
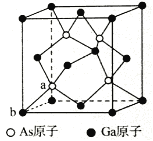
(5)砷化镓为第三代半导体,以其为材料制造的灯泡寿命长,耗能少。已知立方砷化镓晶胞的结构如图所示,砷化镓的化学式为____________________。若该晶体的密度为ρg/cm3,设NA为阿伏加德罗常数的值,则a、b的距离为_________pm(用含ρ和NA的代数式表示)。
【答案】sp3 60° ![]() As>Se>Ge PH3 三角锥形 < S 原子半径小于P原子半径,故S-Cl键要比P-Cl键短 GaAs
As>Se>Ge PH3 三角锥形 < S 原子半径小于P原子半径,故S-Cl键要比P-Cl键短 GaAs ![]()
【解析】
(1)N4分子的空间构型与P4类似,4个N原子形成正四面体构型,每个N原子形成3个N-N键和1对孤对电子;
(2)As元素是第四周期VA族,价电子排布式为4s24p3,根据泡利原理、洪特规则画出价电子排布图;As原子4p轨道为半满稳定状态,能量较低,第一电离能比同周期相邻元素的高;
(3)P元素的电负性比N元素的小,P原子对孤电子对吸引更弱,容易给出孤对电子形成配位键;
(4)PCl3中P原子形成3个P-Cl键,含有1对孤对电子,其空间结构三角锥形,而等电子体的结构相似;
原子半径越小,原子之间形成的共价键越短;
(5)利用均摊法计算晶胞中含有Ga原子、As原子数目,可以确定其化学式;
As原子与周围的4个Ga原子形成正四面体,As原子与晶胞顶点Ga原子连线处于晶胞体对角线上,且Ga原子与As原子之间的距离为晶胞体对角线长度的1/4倍,所以晶胞的体对角线为晶胞棱长的![]() 倍,结合晶胞中含有原子数目,表示出晶胞质量,再根据m=ρV计算晶胞棱长.
倍,结合晶胞中含有原子数目,表示出晶胞质量,再根据m=ρV计算晶胞棱长.
(1)N4分子的空间构型与P4类似,4个N原子形成正四面体构型,每个N原子形成3个N-N键,还含有1对孤对电子,杂化轨道数目为4,故N原子采取sp3杂化,每个面均为正三角形,故N-N键的键角为60°;
(2)As元素处于第四周期VA族,价电子排布式为4s24p3,价电子排布图为:![]() ;As原子4p轨道为半满稳定状态,能量较低,第一电离能高于同周期相邻元素的,故第一电离能:As>Se>Ge;
;As原子4p轨道为半满稳定状态,能量较低,第一电离能高于同周期相邻元素的,故第一电离能:As>Se>Ge;
(3)P元素的电负性比N元素的小,P原子对孤电子对吸引更弱,容易给出孤对电子形成配位键,即为:PH3;
(4)PCl3中P原子形成3个P-Cl键,含有1对孤对电子,其空间结构三角锥形,而等电子体的结构相似,SCl3+的空间构型是三角锥形,S 原子半径小于P原子半径,故 S-Cl 键要比 P-Cl 键短。
(5)晶胞中含有Ga原子数为8×1/8+6×1/2=4,As原子数目为4,化学式为GaAs,As原子与周围的4个Ga原子形成正四面体,As原子与晶胞顶点Ga原子连线处于晶胞体对角线上,Ga原子与As原子之间的距离为晶胞体对角线长度的1/4倍,所以晶胞的体对角线为晶胞棱长的![]() 倍,晶胞质量为4×(70+75)/NAg,则晶胞棱长=
倍,晶胞质量为4×(70+75)/NAg,则晶胞棱长=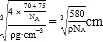 ,故a、b的距离为
,故a、b的距离为![]() 。
。


科目:高中化学 来源: 题型:
【题目】已知反应:2SO2(g)+O2(g)![]() 2SO3(g) ΔH<0。某温度下,将2molSO2和1molO2置于10L密闭容器中,反应达到平衡后,SO2的平衡转化率(α)与体系总压强(p)的关系如图甲所示。则下列说法正确的是( )
2SO3(g) ΔH<0。某温度下,将2molSO2和1molO2置于10L密闭容器中,反应达到平衡后,SO2的平衡转化率(α)与体系总压强(p)的关系如图甲所示。则下列说法正确的是( )

A.由图甲知,A点SO2的平衡浓度为0.08mol·L-1
B.由图甲知,B点SO2、O2、SO3的平衡浓度之比为2∶1∶2
C.达到平衡后,缩小容器容积,则反应速率变化图像可以用图乙表示
D.压强为0.50MPa时不同温度下SO2的转化率与温度关系如丙图,则T2>T1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Pd/A12O3是常见的汽车尾气催化剂。一种从废Pd/A12O3纳米催化剂(主要成分及含量:Pd0.3%,γ-A12O392.8%,其他杂质6.0%)中回收金属Pd的工艺:

已知:γ-Al2O3能与酸反应,α-A12O3不与酸反应。
回答下列问题:
(1)“预处理”时,γ-A12O3经焙烧转化为α-A12O3,该操作的主要目的是_________。
(2)“酸浸”时,Pd转化为PdCl42-,其离子方程式为_________。
(3)“滤液①”和“滤液②”中都含有的主要溶质有_________(填化学式)。
(4)“粗Pd”溶解时,可用稀HNO3替代NaClO3,但缺点是_________。两者相比,_________(填化学式)的氧化效率更高(氧化效率以单位质量得到的电子数表示)。
(5)“沉淀”时,[Pd(NH3)4]2+转化为[Pd(NH3)2]Cl2沉淀,其化学方程式为_________。
(6)酸性条件下,BrO3-能在负载Pd/A12O3纳米催化剂的电极表面快速转化为Br-。
①发生上述转化反应的电极应接电源的_________极(填“正”或“负”);
②研究表明,电流密度越大,电催化效率越高;但当电流密度过大时,该电极会发生副反应生成_________填化学式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碘化钠在光学器件石油探测、安检、环境监测等领域有重要应用。某研究小组开发设计的制备高纯NaI的简化流程如图:
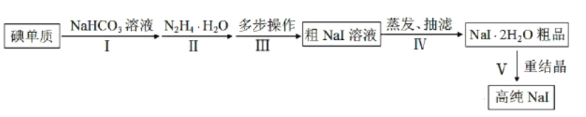
已知:
①I2(s)+I-(aq)![]() I
I![]() (aq)。
(aq)。
②水合肼(N2H4H2O)具有强还原性,可分别将碘的各种酸根和I2还原为I-,本身被氧化为无毒物质。
③NaI易溶于水,也易溶于酒精,在酒精中的溶解度随温度的升高增加不大。
请回答:
(1)步骤Ⅰ,I2与NaHCO3溶液发生歧化反应,生成物中含IO-和IO![]() 离子。
离子。
①I2与NaHCO3溶液反应适宜温度为40~70℃,则采用的加热方式为__。
②实验过程中,加少量NaI固体能使反应速率加快,其原因是__。
(2)步骤Ⅱ,水合肼与IO-反应的离子方程式为__。
(3)步骤Ⅲ,多步操作为:
①将步骤Ⅱ得到的pH为6.5~7的溶液调整pH值至9~10,在100℃下保温8h,得到溶液A;
②将溶液A的pH值调整至3~4,在70~80℃下保温4h,得溶液B;
③将溶液B的pH调整至6.5~7,得溶液C;
④在溶液C中加入活性炭,混合均匀后煮沸,静置10~24h后,过滤除杂得粗NaI溶液。
上述①②③操作中,调整pH值时依次加入的试剂为__。
A.NaOH B.HI C.NH3H2O D.高纯水
(4)步骤Ⅳ,采用改进的方案为用“减压蒸发”代替“常压蒸发”。
①“减压蒸发”需选用的仪器除了圆底烧瓶、蒸馏头、温度计、接收管、接收瓶之外,还有__。
A.直形冷凝管 B.球形冷凝管 C.烧杯 D.抽气泵
②采用“减压蒸发”的优点为__。
(5)将制备的NaI2H2O粗品以95%乙醇为溶剂进行重结晶。请给出合理的操作排序__。
加热95%乙醇→____→___→___→____→纯品(选填序号)。
①减压蒸发结晶 ②NaI2H2O粗品溶解 ③趁热过滤 ④真空干燥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在25°C时,向a mL 0.10mol·L-1的HNO2溶液中逐滴加入0.10mol·L-1的NaOH溶液,滴定过程中,混合溶液的pOH[pOH= -lgc(OH-)]与NaOH溶液的体积V的关系如图所示。已知P点溶液中存在c(OH-)=c(H+)+c(HNO2),下列说法不正确的是( )
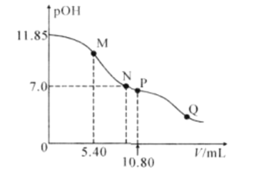
A.25°C时,HNO2电离常数的数量级是10-4
B.M点溶液中存在:3c(H+)+ c(HNO2)=3c(OH-)+ c(NO2-)
C.图上M、N、P、Q四点溶液中所含离子的种类相同
D.a=10.80
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】据《科技日报》报道,我国科学家研制成功一系列石墨烯限域的3d过渡金属中心(Mn、Fe、Co、Ni、Cu)催化剂,在室温条件下以H2O2为氧化剂直接将CH4氧化成C的含氧化合物。请回答下列问题:
(1)在Mn、Fe、Co、Ni、Cu中,某基态原子核外电子排布遵循“洪特规则特例”(指能量相同的原子轨道在全满、半满、全空状态时,体系的能量最低),该原子的外围电子排布式为_____。
(2)在3d过渡金属中,基态原子未成对电子数最多的元素是_____(填元素符号)。
(3)铜的焰色反应呈绿色,在现代化学中,常利用原子光谱上的特征谱线来鉴定元素,称为_____。
(4)石墨烯限域单原子铁能活化CH4分子中的C-H键,导致C与H之间的作用力_____ (“减弱”或“不变”)。铁晶体中粒子之间作用力类型是_____。
(5)常温下,H2O2氧化CH4生成CH3OH、HCHO、HCOOH等。
①它们的沸点分别为64.7℃、-19.5℃、100.8℃,其主要原因是_____;
②CH4和HCHO比较,键角较大的是_____,主要原因是_____。
(6)钴晶胞和白铜(铜镍合金)晶胞分别如图1、2所示。
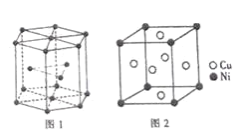
①钴晶胞堆积方式的名称为_____;
②已知白铜晶胞的密度为dg·cm-3,NA代表阿伏加德罗常数的值。图2晶胞中两个面心上铜原子最短核间距为_____ pm(列出计算式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家发现了在细胞层面上对新型冠状病毒(2019-nCOV)有较好抑制作用的药物:雷米迪维或伦地西韦(RemdeSivir,GS-5734)、氯喹 (ChloroqquinE,Sigma-C6628)、利托那韦 (Ritonavir)。其中利托那韦(Ritonavir)的结构如下图,关于利托那韦说法正确的是
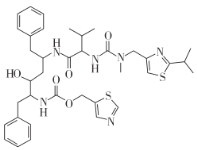
A.能与盐酸或 NaOH溶液反应
B.苯环上一氯取代物有 3种
C.结构中含有 4个甲基
D.1mol该结构可以与13molH2加成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电子工业常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板。
(1)检验溶液中Fe3+存在的常用试剂是___,证明Fe3+存在的现象是____,配制含Fe2+的溶液时,常常向溶液中加入少量___,使被氧气氧化形成的Fe3+还原为Fe2+。
(2)写出FeCl3溶液与金属铜发生反应的化学方程式:___。
(3)某工程师为了从使用过的腐蚀废液中回收铜,并重新获得FeCl3溶液,准备采用下列步骤:
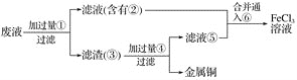
A.请写出上述实验中加入或生成的有关物质的化学式。
①___,②___,③___,④____,⑤____,⑥_____。
B.请写出相关反应的化学方程式。_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式表达不正确的是
A.用SO2水溶液吸收Br2:SO2+Br2+2H2O=4H++SO42-+2Br-
B.酸性高锰酸钾和过氧化氢制取少量氧气:4MnO4-+4H2O2+12H+=4Mn2++7O2↑+10H2O
C.用稀硫酸除去铜绿:4H++Cu2(OH)2CO3=2Cu2++CO2↑+3H2O
D.少量Ba(HCO3)2溶液与NaOH溶液反应:Ba2++2HCO3-+2OH-=BaCO3↓+2H2O+CO32-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com