
����Ŀ��������������ҽҩ�ϳɵ���Ҫ�м��壬ijͬѧ��ʵ�����������������������ȡ��ʵ��������£�
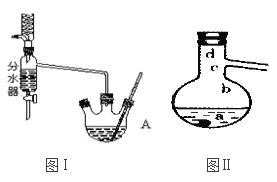
�����Һ��18.5 mL��������13.4 mL���ᣨ��������0.4 mLŨ���ᣩ��������A�в�����������ʯ����ͼI����ʯ������װ�õ���ȥ����Ȼ����Ȼ���Լ20���ӡ�
����Ӧ�����Һ�������´���������ˮϴ�ӣ������Լ�X�������10% Na2CO3��Һϴ�ӡ�
��.�����õ���������������Ʒת��������ƿ�н����������õ�17.1 g������������
����ʵ���������±���ʾ��
������ | ��Է������� | �ܶ�/(g��mL��1) | �е㣯�� | �ܽ��(g)/��100 gˮ�� |
������ | 74 | 0.80 | 118.0 | 9 |
���� | 60 | 1.045 | 118.1 | ���� |
���������� | 1 1 6 | 0.882 | 126.1 | 0.7 |
(1)����A��������_________��ʹ�÷�ˮ����ʵ���пɷ����ˮ����������IJ��ʣ���ԭ����______________________.
(2)������еIJ���˳��Ϊ____________������ţ�����Na2CO3��Һϴ�ӵ�Ŀ����____________���Լ�X����ѡ�����������е�______________������ĸ��ţ���
a����ˮ����þ b��������ʯ�� c����ˮ������
(3)�������װ����ͼ����ʾ����
�������������Ҫʹ��_________�������ܣ����������Ӻú�a������Ӧ����������ͨ����ˮ��b������������ƿ���Ⱥ�˳����___________�������a��b"����b��a����
���¶ȼ�ˮ����������λ�ò�ͬ����Ӱ����������ɣ����¶ȼ�ˮ����ֱ�λ��ͼ���е�________���a����b����c����d������ʱ�ᵼ���ռ����IJ�Ʒ�л��н϶�ĵͷе����ʡ�
(4)��ʵ�������������IJ�����_____________��������������2λ��Ч���֣���
���𰸡� ������ƿ ���Ϸ����ˮ��ʹ������H2OŨ�ȱ�С��������ƽ����������Ӧ�����ƶ� �٢ۢ٢� ��ȥ�����ڲ�Ʒ�е��ᣨ��������˵��Ҳ�ԣ� b ֱ ��a��b a��b 74%
����������1����װ��ͼ��֪����A��������������ƿ����ˮ���������ʹ������ˮ��Ũ�ȼ�С��������������Ӧ���ҽ��У�����ʹ�÷�ˮ����ʵ���пɷ����ˮ����������IJ��ʣ���2��������ˮ��ȥ�ֿ�����ˮ����������ʣ�����Na2CO3��Һ��ȥ�������ᣬ����ˮ��ȥ�����ڲ�Ʒ�е�Na2CO3��Һ��������ˮ�����������ȥ�����Բ�����еIJ���˳��Ϊ�٢ۢ٢ڣ���CaO��ˮ�����ɼ�ᵼ����ˮ�⣬�ʲ�����CaO�������������ѡb����3����ΪʹҺ����Ʒ��ȫ��˳���ؽ���������У�Ӧʹ��ֱ�������ܣ�Ϊȷ���������ȫ��Һ����Ӧ������������ͨ��ȴˮ��Ȼ�������ƿʹ�¶�Ѹ�����µ��е㣬�����Ⱥ�˳������a��b����ͬһ��ƿ�У���ӦҺ���¶ȸ��������¶ȣ������¶ȴ��������¶����ͣ��ʵ��¶ȼƵ�ˮ�������������ƿ��֧�ܿڴ�ʱ�����н϶�е�ϵ͵����ʼ������������У�����λ��ͼ���е�a��b����4��18.5mL��������������18.5 mL��0.8 g/mL=14.8 g���������ϵõ�������������������x����
CH3COOH+CH3CH2CH2CH2OH![]() CH3COOCH2CH2CH2CH3+H2O
CH3COOCH2CH2CH2CH3+H2O
74 g 116 g
14.8 g x
����x=(116 g��14.8 g)��74 g=23.2 g
���������������IJ����ǣ�17.1 g/23.2 g��100%=74%��


 ��һ����ͬ���ɽ�����ϵ�д�
��һ����ͬ���ɽ�����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʵ�������ȷ���ǣ�������
A. ϴ��������ƿ���ԷŽ������к��
B. ��ĥ�ڲ���ƿ����NaOH��Һ
C. �ñ���ȡ��ˮ�е���ʱ����ı���Һ�ӷ�Һ©�����¿ڷų�
D. �ö���̼��ϴ�������Թܱ������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������й�˵����ȷ����
A. �������Ԫ�صĻ�����һ������ǿ������
B. Na2CO3��CaCO3��SiO2���׳Ʒֱ�Ϊ���ʯ��ʯ��ʯӢ
C. �����Ƿ��ж����ЧӦ���ɽ���ɢϵ��Ϊ��Һ���������Һ
D. NH3��SO2��SO3���Ƿǵ���ʣ��Ȼ�����Һ������ͭ��Һ���ǵ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��NM3��D 58���������ٴ�����ε�С���ӿ���ҩ��ṹ���£�

����NM3��D58���������������
A��������NaOH��Һ��Ӧ��ԭ����ȫ��ͬ
B����������ˮ��Ӧ��ԭ����ȫ��ͬ
C�������ܷ�����ȥ��Ӧ��ԭ����ͬ
D����FeCl3��Һ����ɫ��ԭ����ͬ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�о�С�齫һ�����ӷ���������õ���Cu��Al��Fe������Au��Pt�Ƚ����Ļ�������������Ʊ�����ͭ�������ˮ�Ȼ����ķ�����
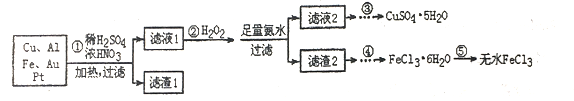
��֪��Cu2++4NH3��H2O=[Cu(NH3)4]2++4H2O
��ش��������⣺
��1�������Cu���ᷴӦ�����ӷ���ʽΪ_________________________��
��2������ڼ�H2O2��������______________������2Ϊ���ѧʽ��__________��
��3������ݲ���ֱ�Ӽ�����ˮ��������________
��4������Һ1��Cu2+��Ũ��Ϊ0.02mol��L-1����������ͭ��ʼ����ʱ��pH=________����֪��Ksp[Cu(OH)2]=2.0x10-20��
��5����֪��2Cu2++4I-=2CuI��+I2 I2+2S2O32-=2I-+S4O62-
ijͬѧΪ�˲ⶨCuSO4��5H2O��Ʒ�����������ɰ����·�����ȡ3.00g��Ʒ����ˮ�ܽ����������KI��Һ����ַ�Ӧ����ˡ�ϴ�ӣ�����Һϡ����250mL��ȡ50mL���������Һ��ָʾ������0.080mol��L-1Na2S2O3����Һ�ζ����ﵽ�ζ��յ��������______________��
�Ĵ�ƽ��ʵ���ȥNa2S2O3����Һ�������£�
ʵ����� | 1 | 2 | 3 | 4 |
����Na2S2O3����Һ��mL�� | 25.00 | 25.02 | 26.20 | 24.98 |
�˲�Ʒ��CuSO4��5H2O����������Ϊ__________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Һ��100 mL 0.5 mol��L-1 NaCl��Һ������Cl-�����ʵ���Ũ����ͬ������ ��
A. 100 mL0.5molL-1 MgCl2��Һ B. 200 mL0.25molL-1 AlCl3��Һ
C. 50mL1molL-1 NaCl��Һ D. 25mL 0.5molL-1 HCl��Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ӵ�������ֵΪNA������˵������ȷ���ǣ� ��
A. ���³�ѹ�£�2 g D2O �к�������ΪNA
B. ����£�22.4L ������̼ԭ����Ϊ6NA
C. 2.4g Mg �ڿ����г��ȼ�գ�ת�Ƶĵ�����Ϊ0.2NA
D. 28g��ϩ�ͱ�ϩ��C3H6���Ļ�����庬�е�̼�����ĿΪ4NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���Ҵ�����Ҫ���л�����ԭ�ϣ�Ҳ�����ʵ�ȼ�ϣ���ҵ�Ͽ�����ϩˮ�Ϸ��ͷ��������ش��������⣺
��1����ϩˮ�Ϸ��ɷ�Ϊ����
��һ������ӦCH2��CH2+ HOSO3H��Ũ���ᣩ��CH3CH2OSO3H���������Ҵף���
�ڶ���������������ˮ�������Ҵ���
�� ��һ�����ڷ�Ӧ____________________���Ӧ���ͣ���
�� �ڶ�����Ӧ�Ļ�ѧ����ʽΪ__________________________________��
�� ��������������Ũ�����������___________________________________��
��2�����ͷ����Ҵ���ֲ��ոѣ���50����ά�أ�Ϊԭ�Ͼ�����ת���Ƶ��Ҵ�
ֲ��ոѡ�ˮ����C6H12O6���ƻ�ø��2CH3CH2OH+2CO2��
![]()
��ά�صĻ�ѧʽΪ_______________����Ҫ��ȡ4.6 ���Ҵ���������Ҫֲ��ո�________�֡�
��3���Ҵ���������90������ͨ������10 ����ȼ���Ҵ����Ͷ��ɡ��Ҵ��������Ҵ��ǿ�������Դ����Դ��_______________�����ϩˮ�Ϸ������ͷ�������
��4�����Ҵ�Ϊԭ�Ͽ��Ʊ�ij�ָ߷���Ϳ�ϣ���ת����ϵ����ͼ��

�� �л���A �Ľṹ��ʽΪ____________��
�� ��Ӧ��Ļ�ѧ����ʽΪ_____________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������Ԫ��X��Y��Z��R��T��ԭ�Ӱ뾶��ԭ��������ϵ��ͼ��ʾ��R��X���γ�X2R��X2R2�����Z�ǵؿ��к������Ľ���Ԫ�أ�Tԭ��������������K���������2���������ƶ���ȷ���ǣ� ��

A. X��Y��ɵĻ������ˮ��Һ����������ƿ�� B. ԭ�Ӱ뾶�����Ӱ뾶�����㣺Y<Z
C. ����������Ӧ��ˮ�������ԣ�Z>T D. ��ZԪ�ص�����Һһ��������
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com