
【题目】研究和开发CO2和CO的创新利用是环境保护和资源利用双赢的课题。
(1)CO可用于合成甲醇。在压强为0.1 MPa条件下,在体积为b L的密闭容器中充入a mol CO和2a mol H2,在催化剂作用下合成甲醇:CO(g)+2H2(g)![]() CH3OH(g)
CH3OH(g)
平衡时CO的转化率与温度、压强的关系如下图:

(ⅰ)该反应属于___________反应(填“吸热”或“放热”)。
(ⅱ)100 ℃时,若一个可逆反应的平衡常数K值很大,对此反应的说法正确的是___________(填序号)。
a.该反应使用催化剂意义不大
b.该反应发生将在很短的时间内完成
c.该反应达到平衡时至少有一种反应物百分含量很小
d.该反应一定是放热反应
(ⅲ)在温度和容积不变的情况下,再向平衡体系中充入a mol CO、2a mol H2,达到平衡时CO的转化率___________(填“增大”、“不变”或“减小”,下同),平衡常数___________。
(ⅳ)在某温度下,向一容积不变的密闭容器中充入2.5 mol CO、7.5 mol H2,反应生成CH3OH(g)达到平衡时,CO的转化率为90%,此时容器内压强为开始时压强的___________倍。
(2)某温度下,若将CO2(g)和H2(g)以体积比1∶4混合,在适当压强和催化剂作用下可制得甲烷,已知:
CH4(g)+2O2(g)===CO2(g)+2H2O(l) ΔH=-890.3 kJ·mol-1
H2(g)+1/2O2(g)===H2O(l) ΔH=-285.8 kJ·mol-1
则CO2(g)和H2(g)反应生成甲烷和液态水的热化学方程式为____________________。
【答案】(1)(ⅰ)放热 ;(ⅱ) c; (ⅲ)增大,不变 ;(ⅳ)0.55;
(2)CO2(g)+4H2(g)===CH4(g)+2H2O(l) ΔH=-252.9 kJ·mol-1。
【解析】
试题分析:(1)(i)根据图像,随着温度的升高,CO的转化率降低,说明反应向逆反应方向进行,根据勒夏特列原理,正反应方向是放热反应;(ii)a、通常状况下,有可能不反应,使用催化剂才能反应,故错误;b、短时间完成,说明反应速率快,化学平衡常数跟化学平衡有关,故错误;c、反应平衡常数很大,说明反应进行程度很大,反应达到平衡,反应物至少有一种反应物百分含量很小,故正确;d、化学平衡常数只受温度影响,100℃时化学平衡常数很大,说明升高温度,平衡向正反应方向移动,即为吸热反应,故错误;(iii)相当于在原来的基础上增大压强,增大压强平衡向正反应方向移动,CO的转化率增大,但平衡常数不变,因为它只受温度的影响;(iv)压强之比等于物质的量之比,消耗1molCO,物质的量减少2mol,减少CO:2.5×90%mol=2.25mol,物质的量减少2×2.25mol=4.5mol,则反应后总物质的量为(10-4.5)mol=5.5mol,反应后的压强是反应压强的0.55倍;(2)①CH4(g)+2O2(g)=CO2(g)+2H2O(l),②H2(g)+1/2O2(g)=H2O(l) ,4×②-①得出△H=(4×-285.8+890.3)kJ·mol-1=-252.9kJ·mol-1,CO2(g)+4H2(g)===CH4(g)+2H2O(l) ΔH=-252.9 kJ·mol-1。


 王后雄学案教材完全解读系列答案
王后雄学案教材完全解读系列答案科目:高中化学 来源: 题型:
【题目】通常用燃烧的方法测定有机物的的分子式,可在燃烧室内将有机物样品与纯氧在电炉加热下充分燃烧,根据产品的质量确定有机物的组成。下图所示的是用燃烧法确定有机物分子式的常用装置。
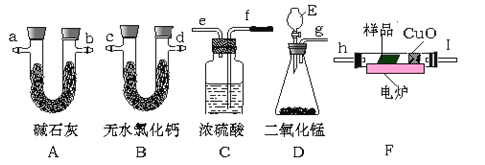
现准确称取1.8g样品(只含C、H、O三种元素中的两种或三种),经燃烧后A管增重1.76g,B管增重0.36g。请回答:
(1)用该方法可测定含有哪些元素和什么状态的有机物_________________;
(2)A、B管内均盛有固态试剂,B管的作用是__________________;
(3)产生的气体由左向右流向,所选用的各导管口连接的顺序是__________________。
(4)E中应盛装什么试剂:______________。
(5)如果把CuO网去掉,A管重量将_______;(填“增大”、“减小”、或“不变”)
(6)该有机物的最简式为__________________;
(7)要确定该有机物的分子式,还必须知道的数据是___________;
A.消耗液体E的质量
B.样品的摩尔质量
C.CuO固体减少的质量
D.C装置增加的质量
E.燃烧消耗O2的物质的量
(8)在整个实验开始之前,需先让D产生的气体通过整套装置一段时间,其目的是_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】环保、安全的铝空气电池的工作原理如图所示,下列有关叙述错误的是( )
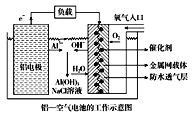
A. NaCl的作用是增强溶液的导电性
B. 正极的电极反应式为O2+4e-+2H2O=4OH-
C. 电池工作过程中,电解质溶液的pH不断增大
D. 用该电池做电源电解KI溶液制取1 mol KIO3,消耗铝电极的质量为54 g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:Ksp(AgCl) = 1.8 × 10-10 ,Ksp(AgI) = 1.5 × 10-16 ,Ksp(Ag2CrO4) =2.0 × 10-12,则在相同温度下,下列难溶盐的饱和溶液中,Ag+浓度大小顺序正确的是
A.AgCl>AgI>Ag2CrO4 B.AgCl>Ag2CrO4>AgI
C.Ag2CrO4>AgCl>AgI D.Ag2CrO4>AgI>AgCl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示为8000C时A、B、C三种气体在密闭容器中反应时浓度的变化只从图上分析不能得出的结论是( )

A.A是反应物
B.前2 min A的分解速率为0.1molL-1min-1
C.达平衡后,若升高温度,平衡向正反应方向移动
D.达平衡后,若增大压强,平衡向逆反应方向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)实验室用Na2CO310H2O晶体配制0.05mol/L的Na2CO3溶液970mL,应选用的容量瓶的规格 ,称取Na2CO310H2O的质量是 g。
(2)2molO3和3molO2的质量之比为 ,分子数之比为 ,同温同压下的密度之比为 ,含氧原子数之比为 。
(3)现有下列九种物质①AgCl ②铜 ③液态醋酸 ④CO2 ⑤H2SO4 ⑥Ba(OH)2固体 ⑦酒精 ⑧稀硝酸 ⑨熔融FeCl3
①上述状态下可导电的是(填序号,下同) ,属于电解质的是 ,属于非电解质的是 。
②上述九种物质中有两种物质之间可发生离子反应H++OH-=H2O,该离子反应对应的化学方程式为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com