
【题目】胶体分散系与其它分散系的本质差别是
A. 是否稳定B. 是否有丁达尔现象
C. 分散质微粒的直径大小D. 分散质粒子是否带电
科目:高中化学 来源: 题型:
【题目】小明同学为研究有机物A和B的结构和性质,分别取7.4gA和6.0gB置于密闭容器中完全燃烧,测得有关数据如下:
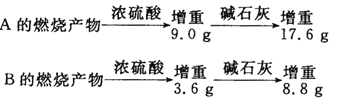
由以上信息可求出:
(1)A物质的分子式为______。已知A和金属Na不反应,则其可能的结构有______种。
(2)B物质的最简式为_______。所有符合该最简式的物质中,相对分子质量最小的物质与酸性高锰酸钾反应的离子方程式为______ 。
(3)相同条件下,相同质量B物质的蒸气所占体积为H2体积的1/30,且B可以发生银镜反应,但不能发生水解反应。写出其结构简式______ 。
(4)若B分子中有3个碳原子,能与NaHCO3反应产生CO2气体,且等效氢的个数比为3:1:1:1,则该物质的系统命名法名称为______ 。
(5)若符合B物质最简式的某物质是生命体中重要的能量物质,在一定条件下可以转化为乙醇,写出该转化反应的化学方程式______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)铝土矿(主要成分为Al2O3,还含有SiO2、Fe2O3)是工业上制备氧化铝的主要原料。工业上提取氧化铝的工艺流程如下:
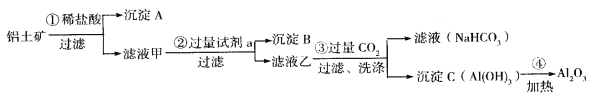
①沉淀A成分是____________;步骤②中的试剂a是_________;(以上均填化学式)。
②简述检验所得滤液甲中存在Fe3+的操作方法:________________________。
(2)用含少量铁的氧化铜制取氯化铜晶体(CuCl2·xH2O)。有如下操作:

已知:在pH为4~5时,Fe3+几乎完全转化为Fe(OH)3沉淀,Cu2+却不反应。
①氧化剂A可选用_________________(填编号,下同)。
A KMnO4 B HNO3 C Cl2 D 浓盐酸
②试剂B可选用____________________。
A NaOH B CuO C FeO D HCl
③试剂B的作用是_______________________________。
A 使Cu2+完全沉淀 B 使Fe3+完全沉淀 C 提高溶液的pH D 除去过量的氧化剂
④从滤液经过结晶得到氯化铜晶体的方法是_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于共价键的说法正确的是 ( )
A.金属原子在化学反应中只能失去电子,因而不能形成共价键
B.由共价键形成的分子可以是单质分子,也可以是化合物分子
C.共价键只能在不同原子之间形成
D.稀有气体分子中只存在共价键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室制取氯气的化学方程式为:MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O。请分别用双线桥法和单线桥法分析该反应中电子转移的方向和数目:
MnCl2+Cl2↑+2H2O。请分别用双线桥法和单线桥法分析该反应中电子转移的方向和数目:
双线桥:MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O。
MnCl2+Cl2↑+2H2O。
__________________________________________
单线桥:MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O。
MnCl2+Cl2↑+2H2O。
___________________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】己知1mol 链烃CxHy可以发生如下系列转化:CxHy![]() Q
Q![]() CxCl12(无机试剂是足量的)下列说法错误的是
CxCl12(无机试剂是足量的)下列说法错误的是
A. x=5、n=11
B. 用酸性高锰酸钾溶液可以区分CxHy和Q
C. 上述转化过程中依次发生了加成反应和取代反应
D. CxCl12可能的结构有三种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢气和氟气反应生成氟化氢的过程中能量变化如图所示。由图可知

A. 生成1 molHF气体放出的热量为270 kJ
B. H2(g)+ F2(g)→ 2HF(l)+ 270 kJ
C. 反应物的总能量大于生成物的总能量
D. 该反应是吸热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】小刚同学探究二氧化硫分别与BaCl2溶液、Ba(OH)2溶液反应的实验。
(1)少量SO2通入到Ba(OH)2溶液中的离子反应方程式为
________________________________________________________________________,
过量的SO2通入到Ba(OH)2溶液中的离子反应方程式为
________________________________________________________________________。
(2)请回答有关问题。小刚同学将SO2通入到BaCl2溶液中,出现了异常现象,看到了明
显的白色沉淀,为探究该白色沉淀的成分,他设计了如下实验流程:
![]()
![]()
![]()
![]()
![]()
则操作①的名称为________,试剂A的化学式为________。
(3)实验表明,小刚加入试剂A后,白色沉淀未见溶解,则该白色沉淀的成分是________(填化学式),产生该白色沉淀的离子方程式是_________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com