
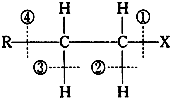
| A、当卤代烃发生水解反应时,被破坏的键是①和④ |
| B、当卤代烃发生水解反应时,被破坏的键是① |
| C、当卤代烃发生消去反应时,被破坏的键是①和③ |
| D、当卤代烃发生消去反应时,被破坏的键是①和② |
 优加精卷系列答案
优加精卷系列答案科目:高中化学 来源: 题型:
| A、1:1:1 |
| B、1:2:1 |
| C、2:3:1 |
| D、2:2:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、含食品添加剂的食品都不属于绿色食品 |
| B、维生素C具有还原性,在人体内起抗氧化作用 |
| C、为防止月饼等富脂食品氧化变质,常在包装袋中放入硫酸亚铁 |
| D、地震后防疫人员在震区周围撒石灰,其作用是进行环境消毒,防止灾后出现疫情 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、c (CH3COO-)<c (Na+) |
| B、c (CH3COOH)+c (CH3COO-)=0.01mol/L |
| C、c (CH3COOH)>c (CH3COO-) |
| D、c (OH-)>c (H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:
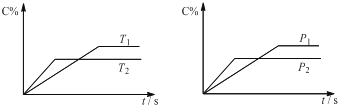
| A、达到平衡后,加入催化剂则C%增大 |
| B、达到平衡后,若升高温度,平衡正向移动 |
| C、a可以为任意的正整数 |
| D、达平衡后,增加A的量,有利于平衡正向移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1:1 | B、2:1 |
| C、1:2 | D、3:1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com