
A.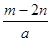 | B. | C. | D. |
 捷径训练检测卷系列答案
捷径训练检测卷系列答案 小夫子全能检测系列答案
小夫子全能检测系列答案科目:高中化学 来源:不详 题型:单选题
| A.3︰2 | B.1︰7 | C.2︰7 | D.1︰14 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.质量为14g | B.分子数为6.02×1024 |
| C.体积为22.4L | D.物质的量为2 mol |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.100mL 0.1mol·L-1的稀硫酸中含有SO42-个数为0.1NA |
| B.1 mol大米中含有NA个大米粒子 |
| C.2.7g金属铝与足量的盐酸反应,铝失去电子数为0.3NA |
| D.常温常压下,11.2L甲烷所含的分子数为0.5NA |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.32g O2中含有的分子数为NA |
| B.标准状况下,22.4 L H2O中含有的分子数为NA |
| C.1 mol Mg与足量O2反应转移的电子数为NA |
| D.1 L 1 mol·L—1 CaCl2溶液中含有的氯离子数为NA |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.一定条件下,2.3g的Na完全与O2反应生成3.6g产物时失去的电子数为0.1NA |
| B.一定条件下用含1mol FeCl3的溶液制备Fe(OH)3胶体,产生NA个Fe(OH)3胶粒 |
| C.标准状况下,22.4L的CCl4中含有的CCl4分子数为NA |
| D.常温常压下,2.24LCO和CO2混合气体中含有的碳原子数目为0.1NA |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| 组别 | I | II | III |
| 盐酸体积/ml | 100 | 100 | 100 |
| A的质量/g | 1.90 | 3.42 | 3.80 |
| 气体的体积/ml | 448 | 716.8 | 672 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.0.1 mol /L | B.1 mol /L | C.4 mol /L | D.0.5 mol /L |
查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com