
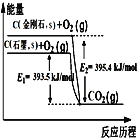
【题目】金刚石和石墨都能燃烧,氧气不足时生成一氧化碳,充分燃烧生成二氧化碳,反应中放出的热量如图所示.下列说法正确的是 ( )
A. 金刚石和石墨互为同素异形体,它们之间的转化属于化学变化
B. 金刚石比石墨稳定
C. 相同物质的量的金刚石比石墨所含有的能量低
D. 由金刚石制取石墨放出1.9 kJ的热量
【答案】A
【解析】
A.金刚石和石墨互为同素异形体,为不同的物质,发生的是化学变化,A正确;
B.由图可知石墨能量低,物质含有的能量越低,稳定性越强,故石墨比金刚石稳定,B错误;
C.图中金刚石的能量高,则相同物质的量的金刚石比石墨所含有的能量高,C错误;
D.①C(s,金刚石)+O2(g)=CO2(g) △H=-395.4 kJ/mol,②C(s,石墨)+O2(g)=CO2(g) △H=-393.5kJ/mol,由盖斯定律可知,①-②得到C(s,金刚石)=C(s,石墨),△H=-395.4 kJ/mol-(-393.5 kJ/mol)=-1.9kJ/mol,由于未指明反应的物质的量,因此不能确定放出热量多少,D正确;
故合理选项是A。


 金博士一点全通系列答案
金博士一点全通系列答案科目:高中化学 来源: 题型:
【题目】POCl3常用作半导体掺杂剂及光导纤维原料,实验室制备POCl3并测定产品含量的实验过程如下:
I.实验室制备POCl3。采用氧气氧化液态PCl3法制取POCl3,实验装置(加热及夹持仪器略)如图:

资料:①Ag++SCN-=AgSCN↓:Ksp(AgCl)>Ksp(Ag SCN);
②PCl3和POCl3的相关信息如下表:
物质 | 熔点/℃ | 沸点/℃ | 相对分子质量 | 其他 |
PCl3 | -112.0 | 76.0 | 137.5 | 两者互溶,均为无色液体,遇水均剧烈反应生成含氧酸和氯化氢 |
POCl3 | 2.0 | 106.0 | 153.5 |
(1) 装置B中的作用是观察氧气的流速和______________、_______________ ,干燥管的作用是_____________
(2)反应温度要控制在60~65℃,原因是:________________________________________________
II.测定POCl3产品的含量。
实验步骤:
①制备POCl3实验结束后,待三颈瓶中的液体冷却至室温,准确称取30.7 g产品(杂质不含氯元素),置于盛有60.00 mL蒸馏水的水解瓶中摇动至完全水解,将水解液配成100.00 mL 溶液。
②取10.00 mL溶液于锥形瓶中,加入10.00 mL 3.2 moI/L AgNO3标准溶液。
③加入少许硝基苯用力摇动,使沉淀表面被有机物覆盖。
④以X为指示剂,用0.2 moI/L KSCN溶液滴定过量的AgNO3溶液,达到滴定终点时共用去10.00 mL KSCN溶液。
(3)实验室用5.0 moI/L AgNO3 配制100 mL 3.2 moI/L AgNO3标准溶液,所使用的仪器除烧杯和玻璃棒外还有_____________________
(4)步骤③若不加入硝基苯的将导致测量结果_____(填偏高、偏低或无影响)
(5)步骤④中X可以选择_____。
(6)反应中POCl3的质量百分含量为_____,通过_____(填操作)可以提高产品的纯度。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CuCl广泛应用于化工和印染等行业。某研究性学习小组拟热分解结晶水合物CuCl·2H2O制备CuCl,并进行相关探究。
【实验探究】该小组用下图所示装置进行实验(夹持仪器略)。

请回答下列问题:
(1)仪器X的名称是 。
(2)实验操作的先后顺序是![]()
![]() (填操作的编号)。
(填操作的编号)。
a.检查装置的气密性后加入药品
b.熄灭酒精灯,冷却
c.在“气体入口”处通入干燥HCl
d.点燃酒精灯,加热
e.停止通入HCl,然后通入N2
(3)在实验过程中,观察到B中物质由白色变为蓝色,C中试纸的颜色变化是 。
(4)装置D中发生的氧化还原反应的离子方程式是 。
【探究反思】
(5)反应结束后,取出CuCl产品进行实验,发现其中含有少量的CuCl2或CuO杂质,根据资料信息分析:
①若杂质是CuCl2,则产生的原因是 。
②若杂质是CuO,则产生的原因是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在下列化学反应中既有离子键、极性键、非极性键断裂,又有离子键、极性键、非极性键形成的是( )
A.Cl2+H2O=HClO+HCl
B.Mg3N2+6H2O=3Mg(OH)2↓+2NH3↑
C.2Na2O2+2H2O=4NaOH+O2↑
D.NH4Cl+NaOH![]() NaCl+NH3↑+H2O
NaCl+NH3↑+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA代表阿伏加德罗常数的值。下列叙述正确的是
A. K37ClO3+6H35Cl(浓)=KCl+3Cl2↑+3H2O反应若有67.2 L氯气生成,电子转移数目为5NA
B. 将1 mol Cl2通入水中,HC1O、Cl-、ClO-粒子数之和为2NA
C. 6.4 g由S2、S4、S8组成的混合物含硫原子数为0.2NA
D. 60g乙酸和葡萄糖混合物充分燃烧消耗NA个O2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图1所示是某些物质的转化关系图(部分小分子产物没有标出)。

已知:
I.A、B、C是三种常见的气态含碳化合物,A、B的相对分子质量均为28,C的相对分子质量略小于A。
II.化合物D的比例模型如图2所示。
III.硫酸氢乙酯水解得E与硫酸。
V.E与F反应,得一种有浓郁香味的油状液体G,E与D反应得无色液体H。
请按要求回答下列问题:
(1)化合物D所含官能团的名称是______,化合物C的结构简式为__________。
(2)化合物A与F在一定条件下也可发生类似①的反应,其化学方程式为___________。
(3)下列说法正确的是___________。
A.反应①的反应类型是加成反应
B.化合物H可进一步聚合成某种高分子化合物
C.在反应②、③中,参与反应的官能团不完全相同
D.从A经硫酸氢乙酯至E的反应中,硫酸实际起到了催化剂的作用
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对可逆反应4NH3(g) + 5O2(g) ![]() 4NO(g) + 6H2O(g),下列叙述正确的是
4NO(g) + 6H2O(g),下列叙述正确的是
A. 化学反应速率关系是:2v正(NH3) = 3v正(H2O)
B. .若单位时间内生成x mol NO的同时,消耗x mol NH3,则反应达到平衡状态
C. 达到化学平衡时,若增加容器体积,则正反应速率减小,逆反应速率增大
D. 达到化学平衡时,4v正(O2) = 5v逆(NO)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com