
【题目】下列离子方程式正确的是()
A.稀盐酸加入大理石中:![]()
B.氢氧化钡溶液中加入稀硫酸![]()
C.硫酸溶液加入![]() 中:
中:![]()
D.稀盐酸加入铁粉中:![]()
【答案】C
【解析】
离子方程式的正误判断,首先看是否符合客观事实,再看化学式拆的是否正确,然后看是否配平,一是原子个数相等,二是两边正负电荷总数要相等,据此进行判断。
A.大理石不溶于水不能拆开,离子方程式为CaCO3+2H+=Ca2++H2O+CO2↑,A错误;
B. 氢氧化钡溶液中加入稀硫酸生成硫酸钡沉淀和水,两个生成物都不能拆开,离子方程式为:Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O,B错误;
C.硫酸溶液加入Cu(OH)2中,离子方程式为2H++Cu(OH)2=Cu2++2H2O,C正确;
D.稀盐酸加入铁粉中反应生成氯化亚铁和氢气,离子方程式为Fe+2H+=Fe2++H2↑,D错误;
答案选C。


 孟建平小学滚动测试系列答案
孟建平小学滚动测试系列答案 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案科目:高中化学 来源: 题型:
【题目】根据下列实验操作与现象得出的结论正确的是
选项 | 实验操作与现象 | 结 论 |
A | 向滴有酚酞的碳酸钠溶液中加入少量氯化钡固体, 红色变浅 | 碳酸钠溶液中存在水解平衡 |
B | 向某溶液中逐渐通入CO2气体,先出现白色胶状沉淀,继续通入CO2气体,白色胶状沉淀不溶解 | 该溶液中一定含有[Al(OH)4]- |
C | 将润湿的淀粉碘化钾试纸置于集满某气体的集气瓶口,试纸变蓝 | 该气体为氯气 |
D | 向10mL 0.5mol·L-1的氯化镁溶液中滴加5mL 2.4mol·L-1氢氧化钠溶液,产生白色沉淀再滴加氯化铜溶液,沉淀变蓝 | Ksp[Cu(OH)2 ]<Ksp[Mg(OH)2 ] |
A. AB. BC. CD. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温时,向20 mL 0.1![]() 的 CH3CH2COOH 溶液中滴加0.1
的 CH3CH2COOH 溶液中滴加0.1![]() 的NaOH溶液,溶液的pH与滴加NaOH溶液体积V的关系如图所示。下列说法正确的是
的NaOH溶液,溶液的pH与滴加NaOH溶液体积V的关系如图所示。下列说法正确的是

A. a 点溶液中 c(CH3CH2COO-) <c(Na+)
B. 图中四点,水的电离程度:c>d>b>a
C. c 点溶液中![]()
D. d 点溶液中c(Na+) +c(OH-) =c(H+) +c(CH3CH2COO-) +c(CH3CH2COOH)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列氧化还原反应中,水作为还原剂的是( )
A.3Fe+4H2O![]() Fe3O4+4H2B.3NO2+H2O = 2HNO3+ NO
Fe3O4+4H2B.3NO2+H2O = 2HNO3+ NO
C.2Na2O2+2H2O = 4NaOH+O2↑D.2F2+2H2O = 4HF+O2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】除去燃煤烟气中的有毒气体,一直是重要的科研课题。某科研小组设计如下装 置模拟工业脱硫脱氮,探究SO2和NO同时氧化的吸收效果。模拟烟气由N2 (90.02%)、SO2(4.99%)、NO(4.99%)混合而成,各气体的流量分别由流量计控制,调节三路气体相应的流量比例,充分混合后进入A。已知:FeSO4+NO![]() [Fe(NO)]SO4(棕色)
[Fe(NO)]SO4(棕色)

(l)仪器A的名称是____,该装置出气管口有两个玻璃球泡,其作用是____。
(2)反应前装置中需要先通入一段时间N2,目的是____,其操作方法是____。
(3)实验中A瓶出现黑色沉淀,写出 A瓶中脱硫反应的离子方程式____。继续实验,现B瓶溶液颜色不变、C瓶溶液出现棕色,这些现象说明____。
(4)关闭活塞e,打开活塞d,在其出气管口,用NO检测仪研究A在不同温度时的脱氮率,实验结果如下图所示,分析图中信息,得出的结论是____。在55℃之前,脱氮率随温度升高而变化的原因可能是____。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高铁电池是一种新型可充电电池,高铁电池的总反应为:3Zn+2K2FeO4+8H2O![]() 3Zn(OH)2+2Fe(OH)3+4KOH,下列叙述不正确的是( )
3Zn(OH)2+2Fe(OH)3+4KOH,下列叙述不正确的是( )
A. 放电时每转移3mol电子,正极有1molK2FeO4被氧化
B. 充电时阳极反应为:Fe(OH)3+5OH-3e-=FeO42-+4H2O
C. 放电时负极反应为:Zn-2e-+2OH-=Zn(OH)2
D. 放电时正极附近溶液的碱性增强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锌-空气燃料电池有比能量高、容量大、使用寿命长等优点,可用作电动车动力电源,电池的电解质溶液为KOH溶液,放电时发生反应:2Zn+O2+4OH-+2H2O=2[Zn(OH)4]2-。下列说法错误的是( )

A.放电时,负极反应为Zn+4OH--2e-=[Zn(OH)4]2-
B.充电时,电解质溶液中c(OH)-逐渐增大
C.放电时,当0.1molZn完全溶解时,流经电解质溶液的电子个数约为1.204×1023
D.采用多孔炭可提高电极与电解质溶液的接触面积,并有利于氧气扩散至电极表面
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H(3一溴-5-甲氧基苯甲酸甲酯)是重要的有机物中间体,可以由A(C7H8)通过下图路线 合成。
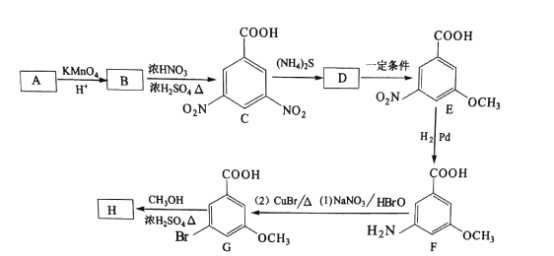
请回答下列问题:
(1)C的化学名称为________,G中所含的官能团有醚键、_______、__________(填名称)。
(2)B的结构简式为________,B生成C的反应类型为___________。
(3)由G生成H的化学方程式为_________。E→F是用“H2/Pd”将硝基转化为氨基,而C→D选用的是(NH4)2S,其可能的原因是________。
(4)化合物F的同分异构体中能同时满足下列条件的共有________种。
①氨基和羟基直接连在苯环上 ②苯环上有三个取代基且能发生水解反应
(5)设计用对硝基乙苯 为起始原料制备化合物
为起始原料制备化合物 的合成路线(其他试剂任选)。_____
的合成路线(其他试剂任选)。_____
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】光气又称碳酰氯,有剧毒,可发生反应: COCl2(g)![]() CO(g)+Cl2(g)H>0。当反应达到平衡时,下列措施不能提高COCl2转化率的是
CO(g)+Cl2(g)H>0。当反应达到平衡时,下列措施不能提高COCl2转化率的是
A. 升温 B. 恒容通入惰性气体 C. 减压 D. 恒压通入惰性气体
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com