
下列排列顺序正确的是:
A、半径:Al3+>Mg2+>Na+>F– B、稳定性:HI<HBr<HCl<HF
C、酸性:HClO4<H2SO4<H3PO4 D、碱性:Al(OH)3>Mg(OH)2>Ca(OH)2
科目:高中化学 来源: 题型:
常温下,已知:4Al(s)+3O2(g)==== 2Al2O3(s)ΔH1 、
4Fe(s)+3O2(g)==== 2Fe2O3(s)ΔH2,关于ΔH1、ΔH2的比较正确的是( )
A.ΔH1>ΔH2 B. ΔH1=ΔH2 C. ΔH1<ΔH2 D.无法计算
查看答案和解析>>
科目:高中化学 来源: 题型:
在下列物质中选择溶于水后可以电离的物质,并写出相应的电离方程式(有几个写几个):
①硝酸铵(NH4NO3) ②葡萄糖[C6H12O6]③氢氧化钡[Ba(OH)2]④硫酸(H2SO4) ⑤四氯化碳(CCl4)
NH4NO3=NH4++NO3﹣
Ba(OH)2=Ba2++2OH﹣
H2SO4=2H++SO42﹣ .
查看答案和解析>>
科目:高中化学 来源: 题型:
下列溶液中微粒浓度关系一定正确的是( )
A.常温下,氨水与氯化铵的pH=7的混合溶液中:c(Cl-)>c(NH4+)
B.常温下,pH=2的一元酸和pH=12的一元强碱等体积混合: c(OH-)=c(H+)
C.0.1 mol·L—1的硫酸铵溶液中:c(NH4+)>c(SO42-)>c(H+)
D.0.1 mol·L—1的硫化钠溶液中:c(OH-)=c(H+)+c(HS-)+c(H2S)
查看答案和解析>>
科目:高中化学 来源: 题型:
某研究小组欲探究SO2的化学性质,设计了如下实验方案。
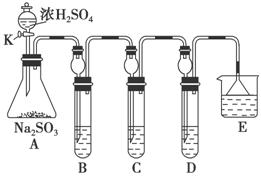
(1)在B中检验SO2的氧化性,则B中所盛试剂可为________。
(2)在C中装FeCl3溶液,检验SO2的还原性,则C中反应的离子方程式为_____________________________________________________。
(3)在D中装新制漂白粉浓溶液。通入SO2一段时间后,D中出现了大量白色沉淀。同学们对白色沉淀成分进行了探究。请回答下列问题:
限选的仪器和试剂:过滤装置、试管、滴管、带导管的单孔塞、蒸馏水、0.5 mol·L-1盐酸、0.5 mol·L-1H2SO4溶液、0.5 mol·L-1BaCl2溶液、品红溶液、新制澄清石灰水。
(ⅰ)假设一:该白色沉淀为CaSO3;
假设二:该白色沉淀为________;
假设三:该白色沉淀为上述两种物质的混合物。
(ⅱ)基于假设一,填写下表:
| 实验操作 | 预期现象和结论 |
| 将D中沉淀过滤,洗涤干净备用 | |
| 用另一干净试管取少量沉淀样品,加入______ __ ______ | __________ _______ ___ ____ |
(ⅲ)若假设二成立,试写出生成该白色沉淀的化学方程式:
__________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
关于化学键的下列叙述中,不正确的是
A、含有共价键的化合物一定是共价化合物
B、共价化合物中一定含有共价键
C、含有离子键的化合物一定是离子化合物
D、双原子单质分子中的共价键一定是非极性键
查看答案和解析>>
科目:高中化学 来源: 题型:
下表是A、B、C、D、E五种有机物的有关信息:
| A | ①能使溴的四氯化碳溶液褪色; ②比例模型为
|
| B | ①由C、H两种元素组成;②球棍模型为 |
| C | ①由C、H、O三种元素组成;②能与Na反应; ③与E反应生成相对分子质量为88的酯 |
| D | ①相对分子质量比C少2;②能由C催化氧化得到 |
| E | ①由C、H、O三种元素组成;②其水溶液能使紫色石蕊试液变红 |
回答下列问题:
A~E中,属于烃的是 (填字母)。
A能使溴的四氯化碳溶液褪色,发生反应的化学方程式为 。
C催化氧化生成D的化学方程式为 。
有机物B具有的性质是 (填序号)。
①无色无味的液体;②有毒;③不溶于水;④密度比水大;
⑤能使酸性KMnO4溶液和溴水褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
在一固定体积的密闭容器中,可逆反应,nA(g)+mB (g)  pC(g)已经达到平衡状态。已知n+m>p,正反应为放热反应。下列分析结论中正确的是
pC(g)已经达到平衡状态。已知n+m>p,正反应为放热反应。下列分析结论中正确的是
①升温,c(B)/c(C)的值变小;②降温,平衡体系内混合气体的平均相对分子质量变小;
③增加B的物质的量,A的转化率增大;④使用催化剂,气体总的物质的量不变;
⑤加压使密闭容器的容积变小,A或B的浓度则变大;
⑥若A的反应速率为v(A),则v(B)= n /m [v(A)]
A.①② B.②③④ C.③④⑤ D.③④⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)常温下,将20.0 g 14%的NaCl溶液跟30.0 g 24%的NaCl溶液混合,混合后得到密度为1.17 g·cm-3的溶液。请计算:
①混合后的溶液中NaCl的质量分数是多少?
②混合后的溶液的物质的量浓度为多少?
(2)在标准状况下,1 L水溶解了一定体积的NH3,所得溶液的密度为ρ g·cm-3,物质的量浓度为a mol·L-,则所溶解的NH3的体积为多少?
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com