
【题目】某混合溶液中可能含有HCl、MgCl2、AlCl3、NH4Cl、Na2CO3、KCl中的几种物质,往该溶液中逐滴加入NaOH溶液,产生沉淀的物质的量(n)与加入的NaOH溶液体积(V)的关系如图所示。下列说法正确的是

A.溶液中一定不含有的溶质是MgCl2、NH4Cl
B.溶液中可能含有的溶质是KCl、Na2CO3
C.溶液中一定含有的溶质是HCl、AlCl3、NH4Cl
D.AB段发生反应的离子方程式为Mg2++2OH-=Mg(OH)2↓
【答案】C
【解析】
根据图象可知,OA段无沉淀,说明有HCl,则无Na2CO3;AB段有沉淀,CD段沉淀完全消失,说明沉淀为Al(OH)3,说明溶液中只有AlCl3,无MgCl2,BC段沉淀不变,说明溶液中含有NH4Cl,此段铵根离子与氢氧根离子反应,根据分析可知,溶液中一定含有HCl、AlCl3、NH4Cl,一定不含MgCl2、Na2CO3,可能含有KCl,以此解答该题。
A. 根据分析,溶液中一定不含有的溶质是MgCl2、Na2CO3,故A错误;
B. 根据分析,溶液中可能含有的溶质是KCl,故B错误;
C. 根据分析,溶液中一定含有的溶质是HCl、AlCl3、NH4Cl,故C正确;
D. AB段发生反应的离子方程式为Al3++3OH-=Al (OH)3↓,故D错误;
答案选C。


科目:高中化学 来源: 题型:
【题目】纳米Fe3O4晶体材料可以作为核磁共振造影增强剂,用于疾病的诊断和治疗,其制备过程如图所示,下列叙述不合理的是( )

A.在反应②中,![]() 的作用可能是促进氯化铁水解
的作用可能是促进氯化铁水解
B.直接加热FeCl3溶液也可以得到四氧化三铁
C.反应③的化学反应方程式是6FeOOH+CO=2Fe3O4+3H2O+CO2
D.纳米四氧化三铁在水中形成的分散系,有可能产生丁达尔现象
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向一定量的FeO,Fe,Fe3O4的混合物中加入100mL 1mol/L的盐酸,恰好使混合物完全溶解,放出224mL(标准状况)的气体,在所得溶液中加入KSCN溶液无血红色出现. 若用足量的CO在高温下还原相同质量的此混合物,能得到铁的质量是()
A.11.2 gB.5.6 gC.2.8 gD.1.4g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】第三周期的三种元素甲、乙、丙,原子序数依次增大,且原子核外都有1个未成对电子,下列说法错误的是
A.金属性:甲>乙>丙B.三种元素的单质都能与水反应
C.离子半径:甲>乙>丙D.最高价氧化物对应水化物可两两相互反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】体积相同的盐酸和醋酸溶液,c(Cl-) = c(CH3COO-)= 0.01 mol/L,下列说法正确的是
A.pH:醋酸>盐酸
B.完全反应消耗NaOH的量:醋酸>盐酸
C.与相同的Na2CO3粉末反应的起始速率:醋酸<盐酸
D.分别用水稀释相同倍数后,所得溶液中:c (Cl-) = c (CH3COO-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】W、X、Y、Z是同周期主族元素,Y的最外层电子数是X次外层电子数的3倍,四种元素与锂组成的盐是一种新型的锂离子电池的电解质(结构如图,箭头表示配位键)。下列说法不正确的是( )
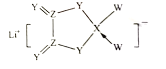
A.W的非金属性比Y的强
B.该物质中X原子满足8电子稳定结构
C.该物质中含离子键和共价键
D.Z的氧化物都易溶于水中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】![]() (连二亚硫酸钠)是易溶于水,不溶于甲醇的白色固体,在空气中极易被氧化,是一种还原性漂白剂。制取
(连二亚硫酸钠)是易溶于水,不溶于甲醇的白色固体,在空气中极易被氧化,是一种还原性漂白剂。制取![]() 的方法很多,
的方法很多,
(1)在碱性溶液中用![]() 还原
还原![]() 法制备
法制备![]() 的反应原理为:
的反应原理为:![]() (未配平)反应装置如图所示:
(未配平)反应装置如图所示:
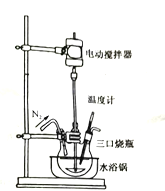
①实验开始及整个过程中均需通入![]() ,其目的是__________________________________。
,其目的是__________________________________。
②制备过程中温度需控制在10~45℃,采用水浴加热的主要优点是______________________。
③为使![]() 尽可能完全被还原,加入三口烧瓶中的反应液,应控制
尽可能完全被还原,加入三口烧瓶中的反应液,应控制![]() ______________。
______________。
(2)用![]() 还原
还原![]() 制备
制备![]() 的装置(夹持加热仪器略)如下:
的装置(夹持加热仪器略)如下:
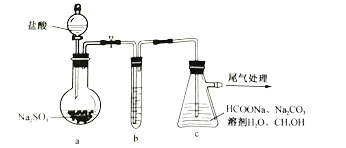
①装置a烧瓶中发生反应的化学方程式为_________________________________。
②装置b用于净化![]() ,适宜的试剂是______________________________。
,适宜的试剂是______________________________。
③装置c在70~83℃生成![]() 并析出,同时逸出
并析出,同时逸出![]() ,该反应的化学方程式为________________________,加入
,该反应的化学方程式为________________________,加入![]() 的目的是________________________;利用反应后的浊液分离提纯
的目的是________________________;利用反应后的浊液分离提纯![]() 需经过的操作为_____________________________________________________。
需经过的操作为_____________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】.某盐是一种重要的化工原料,在印染、制革、木材和农业等领域有重要用途,其溶液可能含有NH4+、Al3+、SO42-、Fe2+、Cl-等若干种离子,某同学设计并完成了如下实验:
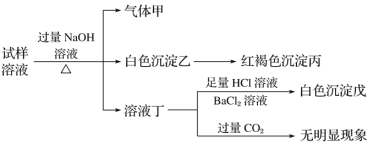
根据以上的实验操作与现象,该同学得出的结论不正确的是( )
A.试样中肯定有NH4+、SO42-和Fe2+
B.试样中一定没有Al3+
C.若气体甲在标准状况下体积为0.448 L,沉淀丙和沉淀戊分别为1.07 g和4.66 g,则可判断溶液中还有Cl-
D.该盐工业上可以用作净水剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学设计了如下实验方法分离KNO3和Ba(NO3)2两种固体混合物并测定其含量:
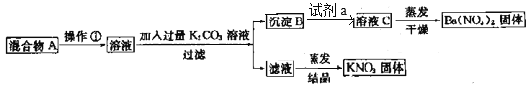
(1)操作①的名称是____________,试剂a是____________(填化学式)。
(2)加入K2CO3溶液所发生反应的离子方程式是__________。
(3)按此实验方案分离得到的KNO3,经分析含有杂质K2CO3,除去K2CO3的操作为___________
(4)过滤后洗涤沉淀B的实验操作为________________。
(5)实验前称量混合物A的质量为m g,称量经洗涤干燥后的沉淀B的质量为w g,则混合物中Ba(NO3)2质量分数为______________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com