
【题目】体积相同的盐酸和醋酸溶液,c(Cl-) = c(CH3COO-)= 0.01 mol/L,下列说法正确的是
A.pH:醋酸>盐酸
B.完全反应消耗NaOH的量:醋酸>盐酸
C.与相同的Na2CO3粉末反应的起始速率:醋酸<盐酸
D.分别用水稀释相同倍数后,所得溶液中:c (Cl-) = c (CH3COO-)
【答案】B
【解析】
A. 盐酸、醋酸的电离方程式分别为HCl=H++Cl-、CH3COOH![]() H++ CH3COO-,c(Cl-) = c(CH3COO-),则二者c(H+)相等,pH:醋酸=盐酸,A项错误;
H++ CH3COO-,c(Cl-) = c(CH3COO-),则二者c(H+)相等,pH:醋酸=盐酸,A项错误;
B.盐酸完全电离,醋酸微弱电离,当c(Cl-) = c(CH3COO-)时,c(HCl) c(CH3COOH) ,故等体积完全反应消耗NaOH的量:醋酸>盐酸,B项正确;
C. 盐酸和醋酸与相同的Na2CO3粉末反应,本质都是与氢离子的反应,初始二者的氢离子浓度相同,故起始速率:醋酸=盐酸,C项错误;
D. 分别用水稀释相同倍数后,稀释过程促进醋酸的电离,故所得溶液中:c (Cl-) < c (CH3COO-),D项错误;
答案选B。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】下列对化学用语的理解正确的是( )
A.键线式H-C1-O可以表示次氯酸分子的结构
B.电子式![]() 可以表示氢氧根离子,也可以表示羟基
可以表示氢氧根离子,也可以表示羟基
C.结构示意图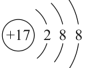 可以可以表示35Cl-,也可以表示37Cl-
可以可以表示35Cl-,也可以表示37Cl-
D.比例模型![]() 可以表示甲烷分子,也可以表示四氯化碳分子
可以表示甲烷分子,也可以表示四氯化碳分子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国科学家提出用CO2置换可燃冰(mCH4·nH2O) 中CH4的设想,置换过程如图所示,下列说法正确的是
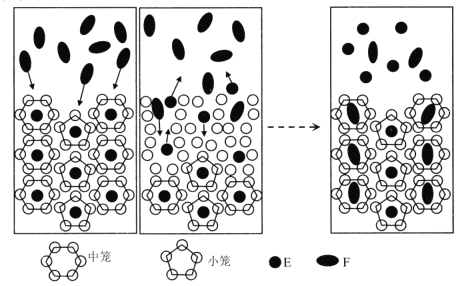
A.E代表CO2, F代表CH4
B.笼状结构中水分子间主要靠氢键结合
C.CO2置换出CH4的过程是化学变化
D.CO2可置换可燃冰中所有的CH4分子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲酸香叶酯是一种食品香料,可以由香叶醇与甲酸发生酯化反应制得。
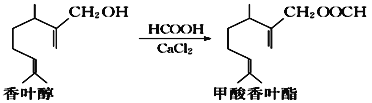
下列说法中正确的是( )
A.香叶醇的分子式为C11H18O
B.香叶醇、甲酸香叶酯均可与钠发生置换反应生成H2
C.1 mol甲酸香叶酯可以与2 mol H2发生加成反应
D.甲酸香叶酯可使溴的四氯化碳溶液和酸性KMnO4溶液褪色,褪色原理相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA 为阿伏加德罗常数的值,下列叙述正确的是
A.标准状况下,22.4L CCl4含有的分子数目为NA
B.7.8g Na2O2与水完全反应转移的电子数为0.1 NA
C.常温常压下,16 g O2和O3的混合气体中含氧原子2NA
D.常温常压下,1L0.l mol/LNaHSO4溶液中HSO4-数目为 0.1NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某混合溶液中可能含有HCl、MgCl2、AlCl3、NH4Cl、Na2CO3、KCl中的几种物质,往该溶液中逐滴加入NaOH溶液,产生沉淀的物质的量(n)与加入的NaOH溶液体积(V)的关系如图所示。下列说法正确的是

A.溶液中一定不含有的溶质是MgCl2、NH4Cl
B.溶液中可能含有的溶质是KCl、Na2CO3
C.溶液中一定含有的溶质是HCl、AlCl3、NH4Cl
D.AB段发生反应的离子方程式为Mg2++2OH-=Mg(OH)2↓
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列流程回答:
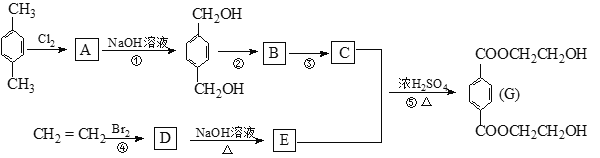
(1) 写出结构简式 C______ E_________。
(2)指出反应类型: ① ___________ ③ _____________ ⑤ ____________
(3)写出化学方程式 C + E ![]() G____________
G____________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定质量的镁和铝的混合物投入100ml盐酸中,固体全部溶解后,向所得溶液中加入NaOH溶液,生成沉淀的物质的量与加入NaOH溶液的体积关系如图所示.
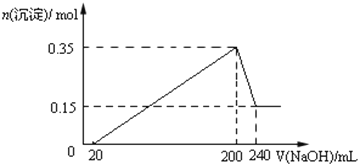
(1)原混合物中镁和铝的质量比为_______
(2)NaOH溶液的物质的量浓度为_______ molL﹣1
(3)生成的气体在标准状况下的体积为_______ L.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Li4Ti5O12和LiFePO4都是锂离子电池的电极材料,可利用钛铁矿(主要成分为FeTiO3,还含有少量MgO、SiO2等杂质)来制备,工艺流程如下:
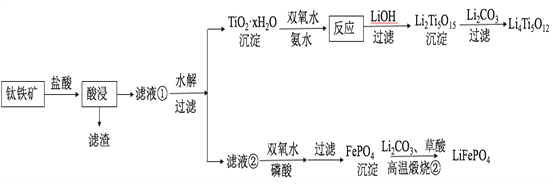
回答下列问题:
(1)“酸浸”实验中,铁的浸出率结果如下图所示。由图可知,当铁的净出率为70%时,所采用的实验条件为___________________。
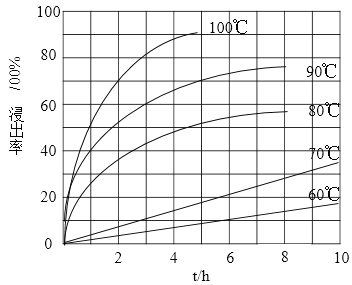
(2)“酸浸”后,钛主要以TiOCl42-形式存在,写出相应反应的离子方程式__________________。
(3)TiO2·xH2O沉淀与双氧水、氨水反应40 min所得实验结果如下表所示:
温度/℃ | 30 | 35 | 40 | 45 | 50 |
TiO2·xH2O转化率% | 92 | 95 | 97 | 93 | 88 |
分析40℃时TiO2·xH2O转化率最高的原因__________________。
(4)Li2Ti5O15中Ti的化合价为+4,其中过氧键的数目为__________________。
(5)若“滤液②”中c(Mg2+)=0.02 mol/L,加入双氧水和磷酸(设溶液体积增加1倍),使Fe3+恰好沉淀完全即溶液中c(Fe3+)=1×10-5 mol/L,此时是否有Mg3(PO4)2沉淀生成?___________(列式计算)。
FePO4、Mg3(PO4)2的Ksp分别为1.3×10-22、1.0×10-24。
(6)写出“高温煅烧②”中由FePO4制备LiFePO4的化学方程式______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com