
| A. | 置换反应 | B. | 分解反应 | C. | 复分解反应 | D. | 氧化还原反应 |
分析 热还原法:冶炼较不活泼的金属Zn、Fe、Sn、Pb、Cu,常用还原剂有(C、CO、H2等),
A.由一种单质跟一种化合物起反应,生成另一种单质和另一种化合物的反应叫做置换反应;
B.由一种反应物生成两种或两种以上其他物质的反应叫分解反应;
C.两种化合物相互交换成分生成另两种化合物的反应叫复分解反应;
D.元素的化合价发生变化的反应,属于氧化还原反应,据此解答.
解答 解:A.一氧化碳还原氧化铁Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2,不是置换反应,故A错误;
B.Hg、Ag等用加热分解氧化物的方法制得,热还原法冶炼金属一定不属于分解反应,因需加还原剂,反应物一定不止一种,故B错误;
C.热还原法冶炼金属,一定属于氧化还原反应,所以一定不属于复分解反应,故C错误;
D.金属化合物中金属表现为正价,金属单质元素表现为0价,所以从金属化合物中还原出金属一定属于氧化还原反应,故D正确;
故选:D.
点评 本题考查了金属的冶炼,侧重考查反应类型判断,熟悉热还原法原理,明确相关概念是解题关键,题目难度不大.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
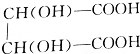 +2NaOH=
+2NaOH=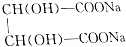 +2H2O.
+2H2O.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 只有②④⑤ | B. | 只有⑤⑦ | C. | 只有①③⑦ | D. | 只有①② |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
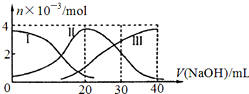
| A. | H2 A在水中的电离方程式是:H2A=H ++HA -;HA -═H++A2- | |
| B. | 当V(NaOH)=20mL时,则有:c(Na + )>c(HA- )>c(H + )>c(A 2- )>c(OH- ) | |
| C. | 当V(NaOH)=30mL时,则有:2c(H + )+c(HA- )+2c(H2A)=c(A 2- )+2 c(OH- ) | |
| D. | 当V(NaOH)=40mL时,其溶液中水的电离受到抑制 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 、
、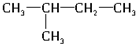 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com