
| A、向NaHCO3溶液中加入少量的澄清石灰水:2HCO3-+Ca2++2OH-=CaCO3↓+CO32-+2H2O |
| B、FeCl3溶液与Cu的反应:Cu+Fe3+═Cu2++Fe2+ |
| C、醋酸溶液与水垢中的CaCO3反应:CaCO3+2 H+═Ca2++H2O+CO2↑ |
| D、氯化铝溶液中加入过量氨水:Al3++4 NH3?H2O═AlO2-+4NH4++2 H2O |


科目:高中化学 来源: 题型:
| A、电化学腐蚀是造成金属腐蚀的主要原冈 |
| B、将可见光通过胶体出现“光路”是因为发生了光的折射 |
| C、酿酒过程中,葡萄糖可通过水解反应生成酒精 |
| D、铜片放入浓硫酸中无明显变化,说明铜在冷的浓硫酸中发生钝化 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 ,试回答:
,试回答:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、原子半径:W>Z>Y>X |
| B、氢化物稳定性:Y>Z |
| C、X与Z只能形成l0电子分子 |
| D、WY3既有离子键又有共价键 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、此元素有3种不同的同位素 | ||||
| B、其中一种同位素质量数为80 | ||||
C、同位素
| ||||
| D、X2平均相对分子质量为160 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 (1)甲醇是一种可再生能源,具有开发和应用的广阔前景,工业上一般可采用如下反应来合成甲醇:CO(g)+2H2(g)?CH3OH(g).分析该反应并回答下列问题:下列各项中,不能够说明该反应已达到平衡的是
(1)甲醇是一种可再生能源,具有开发和应用的广阔前景,工业上一般可采用如下反应来合成甲醇:CO(g)+2H2(g)?CH3OH(g).分析该反应并回答下列问题:下列各项中,不能够说明该反应已达到平衡的是查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
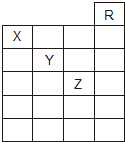 如图是元素周期表前六周期的一部分,关于元素X、Y、Z的叙述正确的是( )
如图是元素周期表前六周期的一部分,关于元素X、Y、Z的叙述正确的是( )| A、只有③ | B、只有①④ |
| C、只有①②③④ | D、①②③④⑤ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com