
【题目】铝热反应有广泛的用途,实验装置如下图1所示。下列说法正确的是

A. 铝热反应的能量变化可用图2表示
B. 工业上可用铝热反应的方法提取镁
C. 在铝热反应过程中没有涉及到的化学反应类型是化合反应
D. 该铝热反应的化学方程式是8Al+3Fe3O4![]() 4Al2O3+9Fe
4Al2O3+9Fe
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】在25℃时,密闭容器中X、Y、Z三种气体的初始浓度和平衡浓度如表:下列说法错误的是( )
物质 | X | Y | Z |
初始浓度/molL﹣1 | 0.1 | 0.2 | 0 |
平衡浓度/molL﹣1 | 0.05 | 0.05 | 0.1 |
A.反应达到平衡时,X的转化率为50%
B.反应可表示为X+3Y2Z
C.改变温度可以改变此反应的平衡常数
D.增大压强使平衡向生成Z的方向移动,平衡常数增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】唑啉草酯H是用于麦田的具有新颖结构的苯基吡唑啉除草剂。一种合成路线如下:
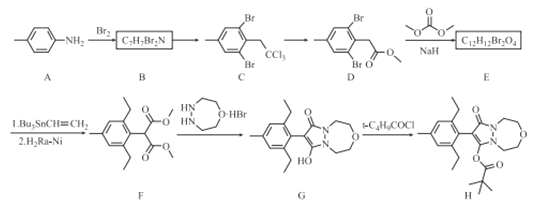
回答下列问题:
(1)A的化学名称为__________
(2)B的结构简式为__________
(3)G![]() H的反应类型为__,下列关于G、H的说法正确的是______(填选项字母)。
H的反应类型为__,下列关于G、H的说法正确的是______(填选项字母)。
A.G不含手性碳原子,H含有一个手性碳原子
B.二者均能使酸性KMnO4溶液褪色
C.二者均含有3种含氧官能团
D.二者各1mol时,最多消耗H2的物质的量不相等
(4)写出D![]() E的化学反应方程式:__________.
E的化学反应方程式:__________.
(5)同时满足下列条件的F的同分异构体Ⅰ的结构有__种(不考虑立体异构),写出一种核磁共振氢谱显示有3种不同化学环境的氢,且峰面积之比为9:1:1的Ⅰ的结构简式:_________________
①苯环上连有2个相同的叔丁基[-C(CH3)3]
②苯环上只有2个H
③1molⅠ能与2molNaHCO3反应产生无色气体
(6)结合题给信息,写出以2-甲基-1-丙烯和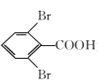 为原料(其他试剂任选)制备化合物
为原料(其他试剂任选)制备化合物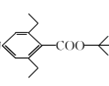 的合成路线:____________。
的合成路线:____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA代表阿伏加德罗常数的值,下列叙述正确的是
A. 标准状况下,1.12 L CCl4含有质子数的数目为3.7NA
B. 常温常压下,3.0 g含葡萄糖的冰醋酸中含有的原子总数为0.4NA
C. 常温时,56g Fe与足量浓硝酸反应,转移的电子数目为3NA
D. 晶体B的结构单元如右图 ,则11g晶体B含有0.6NA个三角形(相邻原子构成)
,则11g晶体B含有0.6NA个三角形(相邻原子构成)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关图示的说法正确的是

A. 图甲表示CH4 (g)+2O2 (g)=CO2 (g)+2H2O(1)的能量变化
B. 图乙表示压强对2A(g)+2B(g)![]() 3C(g)+D(g)的影响,且压强:P甲>P乙
3C(g)+D(g)的影响,且压强:P甲>P乙
C. 图丙表示温度对N2 (g)+3H2(g)![]() NH3 (g) △H<0的影响
NH3 (g) △H<0的影响
D. 图丁表示N2 (g)+3H2(g)![]() 2NH3 (g)平衡时NH3体积分数随起始n(N2)/n(H2)的变化,则转化率:αA(H2)=αB(H2)
2NH3 (g)平衡时NH3体积分数随起始n(N2)/n(H2)的变化,则转化率:αA(H2)=αB(H2)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有机物的结构简式中,书写正确的是( )
A. CH2CH2 B. C2H5OOCCH3 C. CH3—CH—CH3 D. CH3C—OOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对炼锌厂的铜镉废渣中各元素进行分离,能减少环境污染,同时制得食品锌强化剂的原料ZnSO4·7H2O实现资源的再利用。其流程图如下。

[相关资料]
①铜镉废渣中含有铜、锌、镉、铁、砷等元素,其含量依次减少。
②FeAsO4难溶于水;ZnSO4·7H2O易溶于水,难溶于酒精。
③Zn(OH)2属于两性氢氧化物。
④滤液I中有Fe2+、Zn2+、Cu2+、Cd2+和少量的AsO![]() 。
。
⑤有关离子沉淀完全的pH
金属离子 | Fe3+ | Zn2+ | Mn2+ | Cu2+ | Cd2+ |
沉淀完全pH | 3.2 | 8.0 | 9.8 | 6.4 | 9.4 |
请回答下列问题:
(1)提高铜镉废渣浸出率可以采用的方法是(写出其中一点即可)____;
(2)向滤液I中逐滴滴人酸性KMnO4溶液可与AsO![]() 发生反应生成FeAsO4,写出该反应的离子方程式____;加入酸性KMnO4溶液不能过量,判断该滴定终点的现象是____;滤渣Ⅱ中除了FeAsO4外,还有____;
发生反应生成FeAsO4,写出该反应的离子方程式____;加入酸性KMnO4溶液不能过量,判断该滴定终点的现象是____;滤渣Ⅱ中除了FeAsO4外,还有____;
(3)制得的ZnSO4·7H2O需洗涤,洗涤晶体时应选用试剂为____;
(4)上述流程除了实现对这些元素进行提取分离能减少环境污染,同时制得ZnSO4·7H2O实现资源的再利用,还可以得到副产物___
(5)回收所得的Cd可用于制造镍镉碱性二次电池,电池的工作时,正极NiO(OH)转化为Ni(OH)2,则充电时电池的正极反应式为____;
(6)若a克铜镉废渣含有b molFe元素,加入了c mol KMnO4,则铜镉废渣中As元素的质量分数为____。(不考虑镉元素与KMnO4的反应)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于元素周期律和周期表的描述,正确的是( )
A. 在元素周期表的右上方可以寻找制取半导体的元素
B. 元素的性质随着原子序数的增加而呈周期性变化
C. 俄国化学家门捷列夫是通过实验的方法建立元素周期表的
D. 同一主族元素的原子从上到下,原子半径减小,金属性增强
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com