
【题目】A、B、C、D、E是原子序数依次增大的五种短周期元素。A原子的电子层数与它的核外电子总数相同,A与C、B与D分别为同主族,B和C的最外层电子数之和与E的最外层电子数相同。A与E形成的化合物化学式为AE,其分子中含18个电子。请回答下列问题:
(1)A元素单质的化学式为__________________。
(2)由A、B、C三种元素形成的化合物的电子式为___________,这种化合物形成的晶体中所含的化学键类型有______________。
(3)A、B、D三种元素形成的一种化合物和A、B形成的一种化合物能发生氧化还原反应,反应的化学方程式为_____________________________________________。
(4)B、C、E三种元素形成一种盐,此盐中三种原子个数比为1∶1∶1,在25℃时,将该盐溶于水,测得溶液pH>7,理由是___________________________(用离子方程式表示)。
【答案】H2 ![]() 离子键、共价键 H2SO3 +H2O2=H2SO4 +H2O ClO-+H2O =HClO+OH-
离子键、共价键 H2SO3 +H2O2=H2SO4 +H2O ClO-+H2O =HClO+OH-
【解析】
A、B、C、D、E是原子序数依次增大的五种短周期元素.A原子的电子层数与它的核外电子总数相同,则A为H元素;因A与C、B与D分别为同主族,则C为Na元素;AE是18e-的化合物,则E为Cl元素;又因为B与C的最外层电子数之和与E的最外层电子数相同,则B最外层电子数=7-1=6,则B为O元素,D为S元素,据此解答。
A、B、C、D、E是原子序数依次增大的五种短周期元素.A原子的电子层数与它的核外电子总数相同,则A为H元素;因A与C、B与D分别为同主族,则C为Na元素;AE是18e-的化合物,则E为Cl元素;又因为B与C的最外层电子数之和与E的最外层电子数相同,则B最外层电子数=7-1=6,则B为O元素,D为S元素,
(1)A元素单质的化学式为H2;
(2)由H、O、Na三种元素形成的化合物为NaOH,其电子式为![]() ,晶体中所含的化学键有:离子键、共价键;
,晶体中所含的化学键有:离子键、共价键;
(3)H、O、S三种元素形成的一种化合物和H、O形成的一种化合物能发生氧化还原反应,应是亚硫酸与过氧化氢反应生成硫酸、水,反应的化学方程式为:H2SO3+H2O2═H2SO4+H2O;
(4)O、Na、Cl三种元素形成一种盐,此盐中三种原子个数比为1:1:1,则该盐为NaClO,在25℃时,将该盐溶于水,溶液中ClO-水解:ClO-+H2OHClO+OH-,破坏水的电离平衡,溶液呈碱性,即溶液的pH>7。


 口算能手系列答案
口算能手系列答案科目:高中化学 来源: 题型:
【题目】如图是用实验室制得的乙烯(C2H5OH![]() CH2=CH2↑+H2O)与溴水作用制取1,2﹣二溴乙烷的部分装置图,根据图示判断下列说法正确的是
CH2=CH2↑+H2O)与溴水作用制取1,2﹣二溴乙烷的部分装置图,根据图示判断下列说法正确的是

A. 装置①和装置③中都盛有水,其作用相同
B. 装置②和装置④中都盛有NaOH溶液,其吸收的杂质相同
C. 产物可用分液的方法进行分离,1,2﹣二溴乙烷应从分液漏斗的上口倒出
D. 制备乙烯和生成1,2﹣二溴乙烷的反应类型分别是消去反应和加成反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三氧化二铟(In2O3)是一种透明的导电材料,可运用于接触屏、液晶显示器等高科技领域;铟产业被称为“信息时代的朝阳产业”。利用水铟矿[主要成分In(OH)3,常温下Ksp[In(OH)3]=l.41×10-33]制备In2O3的工艺流程如下:
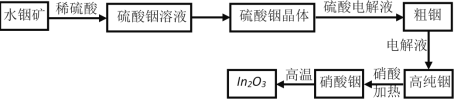
(1)写出水铟矿被硫酸酸浸的离子方程式___________________。
(2)从硫酸铟溶液中制备硫酸铟晶体的实验步骤:____、_____、过滤、洗涤、干燥。
(3)某研究机构用硫酸提取铟时,酸度(每升溶液中含硫酸的质量)与浸出率关系如图
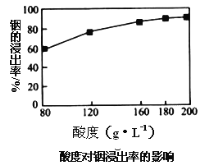
①当酸度为196时,硫酸物质的量浓度为___________。
②请选择适宜的酸度值:_______,并说明选择的理由______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】绿矾别名青矾、皂荚矾等,是我国古代常用的药材,以硫铁矿[主要成分为二硫化亚铁(FeS2)]为原料制备绿矾晶体,工艺流程如下:
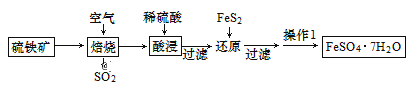
下列说法正确的是( )
A.焙烧过程中每生成1molSO2转移电子数为5NA
B.还原后所得滤液可用高锰酸钾检验Fe3+是否反应完全
C.为中和还原后滤液中过量的酸,可加入一定量FeCO3
D.操作1为蒸发结晶
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学利用家中废旧材料制作可使扬声器发出声音的电池,装置如下图所示。下列说法不正确的是
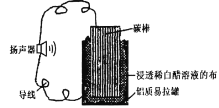
A.扬声器发声,说明该装置将电能转化为化学能
B.铝质易拉罐逐渐被腐蚀,说明铝失去电子
C.在碳棒上有气体生成,该气体可能为氢气
D.电子由铝制易拉罐经导线流向碳棒
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了研究化学反应A+B=C+D的能量变化情况,某同学设计了如图所示装置。当向盛有A的试管中滴加试剂B时,看到U形管中甲处液面下降乙处液面上升。
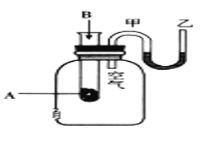
试回答下列问题:
(1)该反应为_______反应(填“放热”或“吸热”)。
(2)A和B的总能量比C和D的总能量_______(填“高”或“低”)。
(3)反应物化学键断裂吸收的能量_______(填“高”或“低”)于生成物化学键形成放出的能量。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】![]() 、
、![]() 为核电荷数小于18的两种元素,元素
为核电荷数小于18的两种元素,元素![]() 的原子的最外层电子数是次外层电子数的一半,元素
的原子的最外层电子数是次外层电子数的一半,元素![]() 的原子的最外层电子数与最内层电子数之和等于次外层电子数。下列有关叙述正确的是
的原子的最外层电子数与最内层电子数之和等于次外层电子数。下列有关叙述正确的是
A.![]() 、
、![]() 一定是非金属元素B.
一定是非金属元素B.![]() 的最外层电子数比
的最外层电子数比![]() 的少
的少
C.![]() 的单质在化学反应中只能作还原剂D.
的单质在化学反应中只能作还原剂D.![]() 与
与![]() 的最外层电子数相等
的最外层电子数相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】观察下列A、B、C、D、E五种粒子(原子或离子)的结构示意图,回答有关问题:
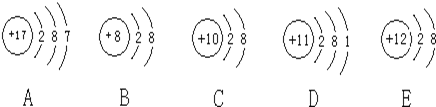
(1)属于离子结构示意图的是______、______(填编号)。
(2)性质最稳定的原子是(填写编号,在本小题中下同)______,最容易失去电子的原子是______,最容易得到电子的原子是______。
(3)A、D两种元素形成的化合物在水溶液中的电离方程式______。
(4)在核电荷数1-18的元素内,列举两个与B核外电子层排布相同的离子,写出离子的符号______、______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某烃A的相对分子质量为84。回答下列问题:
(1)该烃的分子式为________,下列物质与A以任意比例混合,若总物质的量一定,充分燃烧消耗氧气的量不变的是________(填序号)。
a.C6H14 b.C7H12O2 c.C6H14O d.C7H14O2
(2)若烃A为链烃,与HBr加成后只能得到一种产物,且该烃的一氯代物只有一种。
①A的结构简式为________。
②链烃A与溴的CCl4溶液反应生成B;B与NaOH的醇溶液共热可得到D,D分子中无溴原子。请写出由B制备D的化学方程式:________。
(3)若核磁共振氢谱显示链烃A有三组不同的峰,峰面积比为3∶2∶1,则A的可能的结构有几种________(不考虑顺反异构)。
(4)若A不能使溴水褪色,且其一氯代物只有一种,则A的结构简式为________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com