
����Ŀ��ijС��ͬѧ�����ƣ����岽�����£�
![]()
��ʱ����õ�ʵ������ͼ���£�
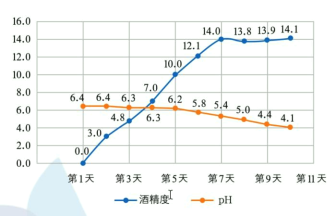
����˵������ȷ����
A.Ŵ���е����ھ������ǻ�ø������ˮ��Ϊ�����ǣ��������ھƻ�ø������ת��Ϊ�Ҵ�
B.����������� pH ���½�����������Ϊ�����Ҵ�����������Ϊ����
C.�ӵ� 7 �쿪ʼ�Ƶľƾ��Ƚ������䣬˵����Һ�е��������Ѿ���ȫ��Ӧ
D.��С������������ƾƾ��Ȳ��ߣ��ɲ���������߾ƾ���
���𰸡�B
��������
A. Ŵ���е����ھ������ǻ�ø������ˮ��Ϊ�����ǣ��������ھƻ�ø������ת��Ϊ�Ҵ�����A��ȷ��
B. ����������� pH ���½�����������Ϊ���������黯ø�������²��������ᣬ�Ӷ�ʹ��pH���ͣ���B����
C. �ӵ� 7 �쿪ʼ�Ƶľƾ��Ƚ������䣬˵����Һ�оƾ��������ɣ��������Ѿ���ȫ��Ӧת��Ϊ�ƾ�����C��ȷ��
D. ��С������������ƾƾ��Ȳ��ߣ�Ϊ����߾ƾ��ȿɲ�������������D��ȷ��
������������ΪB��


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NAΪ�����ӵ�������ֵ������˵����ȷ����
A.100g46%����(HCOOH)ˮ��Һ��������ԭ����Ϊ5NA
B.14gFe����������ʴ����Fe2O3��xH2O���缫��Ӧת�Ƶĵ�����Ϊ0.75NA
C.8.8 g���������к����õ��ӶԵ���ĿΪ1.3NA
D.��״���£�22.4LCS2�������ķ�����ĿΪ NA��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��25��ʱ��������ĵ���ƽ�ⳣ�����£�
��ѧʽ | CH3COOH | H2CO3 | HClO |
����ƽ�ⳣ�� | 1.8��10��5 | K1��4.3��10��7 K2��5.6��10��11 | 3.0��10��8 |
�ش��������⣺
��1��һ������£����¶�����ʱ��Ka________(����������������С������������)��
��2�������������ӽ��H+�����ɴ�С��˳����______________________(����ĸ)��
a.CO32�� b.ClO�� c.CH3COO�� d.HCO3��
��3�����з�Ӧ���ܷ�������________(����ĸ)��
a. CO32����2CH3COOH��2CH3COO����CO2����H2O
b. ClO����CH3COOH��CH3COO����HClO
c. CO32����2HClO��CO2����H2O��2ClO��
d. 2ClO����CO2��H2O��CO32����2HClO
��4��������ˮϡ�ʹ��ᣬ���и�ʽ��ʾ����ֵ��ˮ�������Ӷ��������______(����ĸ)��
a.c(CH3COOH)/c(H+) b. c(CH3COO-)/c(CH3COOH) c. c(H+)/Ka d.c(H+)/c(OH-)
��5�������Ϊ10 mL��pH��Ϊ2�Ĵ�����Һ��HX��Һ�ֱ��ˮϡ����1000 mL��ϡ������pH�仯����ͼ��ʾ��
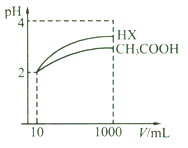
��HX�ĵ���ƽ�ⳣ��________(����>������=������<������ͬ)����ĵ���ƽ�ⳣ����ϡ�ͺ�HX��Һ��ˮ���������c(H+)_____������Һ��ˮ���������c(H+)����ͬŨ�ȵ�NaOH��Һ�ֱ��к�������������Һ��ǡ���к�ʱ����NaOH��Һ�����������____HX��
��6��25��ʱ�����CH3COOH��CH3COONa�Ļ����ҺpH��6������Һ��c(CH3COO��)-c(Na+)��________mol��L-1(�ȷ��ֵ)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����20 mL 0.40 mol/L H2O2��Һ�м�������KI��Һ������H2O2+I-=H2O+IO��������H2O2+IO��= H2O+O2��+ I����H2O2�ֽⷴӦ�����������仯�Ͳ�ͬʱ�̲������O2�����(�������״��)���¡�
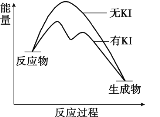
t/min | 0 | 5 | 10 | 15 | 20 |
V(O2)/mL | 0.0 | 12.6 | 20.16 | 28.0 | 32.7 |
�����ж�����ȷ����
A. ��ͼ�п��Կ�����KI������H2O2�ķֽ�����
B. ��Ӧ���Ƿ��ȷ�Ӧ����Ӧ�������ȷ�Ӧ
C. 0~10 min��ƽ����Ӧ���ʣ�v(H2O2)��9.0��10-3 mol/(L��min)
D. H2O2�ڷ�Ӧ�����м������������ԣ��������˻�ԭ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ʵ����ʵ���������������Ӧ������ȷ���ǣ� ��
ѡ�� | ʵ����ʵ����� | ���� |
A | ����������ͬ�� | ��������������ʱ������Ӧ��Ũ�Ȼ�ѧ��Ӧ���ʼӿ� |
B | �ڻ�ѧ��Ӧǰ�����������ͻ�ѧ���ʶ�û�з����ı� | ����һ�������뻯ѧ��Ӧ |
C | ���ʵ���Ũ����ͬ������ʹ���ֱ������������״��ͬ��п����Ӧ | ��ʼʱ�ķ�Ӧ������ͬ |
D | ���ݻ��ɱ���ܱ������з�����Ӧ | ����Ӧ���ʼӿ죬�淴Ӧ���ʲ��� |
A. AB. BC. CD. D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���� N��ϩ��������ͪ��NVP���ͼ���ϩ�� �����һ���HEMA���ϳ�ˮ�������ϸ߾���A ���нϸߵĺ�ˮ������·������ͼ��ʾ��
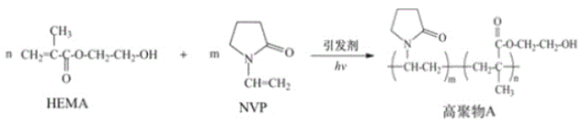
����˵������ȷ����
A.HEMA ��ˮ�������������ۺϷ�Ӧ�ĵ���
B.�߾���A ���ж����OH ���������õ���ˮ��
C.HEMA �� NVP ͨ�����۷�Ӧ���ɸ߾��� A
D.�����߾���A ������HOOC(CH2)4COOH ��Ӧ������ͨ���γ��µ����������������γ���״�ṹ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����mgþ�����Ļ�����м���������ϡ���ᣬǡ����ȫ��Ӧ���ɱ�״���µ�����bL����Ӧ�����Һ�м���cmol/L����������ҺVmL��ʹ�������Ӹպó�����ȫ���õ��ij�������Ϊng���ٽ��õ��ij����������������ٸı�Ϊֹ���õ�����pg�������й�ϵ����ȷ����
A. ![]() B.
B. ![]() C. n=m+17Vc D.
C. n=m+17Vc D. ![]() m��p��
m��p��![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ش��������⣺
��1��25��ʱ��pH��3����������ˮ�������c(H��)Ϊ_______��
��2��99��ʱ����pH��6������ˮ�м���NaHSO4���壬�����¶Ȳ��䣬�����Һ��pH��2����ʱˮ�����ӻ�Kw��_____����Һ��c(OH-)Ϊ_____��
��3��25��ʱ��a mol��L��1CH3COOH��Һ��pH��b���ú�a��b�Ĵ���ʽ��ʾCH3COOH�ĵ���ƽ�ⳣ��Ka��________��
��4��25��ʱ��pH��3�Ĵ����pH��11��NaOH��Һ�������Ϻ���Һ��___(������������������������)�ԡ�
��5��25��ʱ��Ka(CH3COOH)��1.8��10��5��Ka(HSCN)��0.13�����¶��½�20mL 0.1mol��L��1CH3COOH��Һ��20mL 0.1mol��L��1HSCN��Һ�ֱ���20mL 0.1mol��L��1NaHCO3��Һ��ϣ�ʵ���ò������������(V)��ʱ��(t)�仯��ʾ��ͼ��ͼ��ʾ����Ӧ��ʼ�Σ�������Һ����CO2��������ʴ������Բ����ԭ����_____________________________________________��

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��һ��ʵ������ȡ������������Ϊԭ�Ͻ����ض���Ӧ��װ�ã�B���е��ܺ�һ����ͨ���ij���©������

��1��A����������װ�ã����з�Ӧ�Ļ�ѧ����ʽΪ__________________________��
��2��ʵ�鿪ʼʱ���ȵ�ȼA���ľƾ��ƣ�������K����Cl2��������װ�ã��ٵ�ȼD���ƾ��ƣ�Cl2ͨ��Cƿ���ٽ���D��Dװ�õ�Ӳ�ʲ�������ʢ��̿�ۣ�����������ԭ��Ӧ�������ΪCO2��HCl����д��D�з�Ӧ�Ļ�ѧ����ʽ��___________________��װ��C��������_________________ ��
��3����E������ɫʯ����Һ����ɫ����ɫ��Ϊ��ɫ���ٱ�Ϊ��ɫ����ԭ����__��
��4������E���ձ�����Һ��Ϊ����ʯ��ˮ����Ӧ����������Ϊ___����ѡ���ţ�
��A���а�ɫ�������ɣ�B�������Ա仯��C�������ɰ�ɫ�����������ɫ������ʧ
��5��D����Ӧ��Ϻر�����K����ȥ�ƾ��ƣ����������ȵ����ã�A������Cl2��������ʱB�е�������__��B��������___________________________________��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com