
对于0.1mol•L-1 Na2SO3溶液,正确的是
A、升高温度,溶液的pH降低
B、c(Na+)=2c(SO32―)+ c(HSO3―)+ c(H2SO3)
C、c(Na+)+c(H+)=2 c(SO32―)+ 2c(HSO3―)+ c(O H―)
H―)
D、加入少量NaOH固体,c(SO32―)与c(Na+)均增大
科目:高中化学 来源: 题型:
一定温度下,某密闭容器中的反应为:aX(g)+bY(g))  cZ(g)+dW(g),经5min达到平衡,X减少n mol/L,Y减少n/3mol/L,Z增加2n/3mol/L。若将体系压强增大,W的百分含量不发生变化,则
cZ(g)+dW(g),经5min达到平衡,X减少n mol/L,Y减少n/3mol/L,Z增加2n/3mol/L。若将体系压强增大,W的百分含量不发生变化,则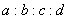 为
为
A.3:1:2:1 B.1:3:2:2 C.1:3:1:2 D.3:1:2:2
查看答案和解析>>
科目:高中化学 来源: 题型:
Na2O2、HCl、Al2O3三种物质在水中完全反应后,溶液中只含有Na+、H+、Cl-、OH-且溶液呈中性,则Na2O2、HCl、Al2O3的物质的量之比可能为
A.3∶2∶1 B.2∶4∶1 C.2∶3∶1 D.4∶2∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组离子在指定溶液中能大量共存的是 ( )
①无色溶液中:K+、Na+、MnO4-、SO42-
②pH=11的溶液中:CO32-、Na+、AlO2-、NO3-
 ③加入Al能放出H2的溶液中:Cl-、HCO3-、SO42-、NH4+
③加入Al能放出H2的溶液中:Cl-、HCO3-、SO42-、NH4+
④由水电离出的c(OH-)=10-13mol·L-1的溶液中:Na+、Ba2+、Cl-、Br-
⑤有较多Fe3+的溶液中: Na+、NH4+、SCN-、HCO3-
⑥酸性溶液中:Fe2+、Al3+、NO3-、I-、Cl-
A.①② B.③⑥ C.②④ D.③⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
将标准状况下的2.24L CO2通入150mL1mol/LNaOH溶液中,下列说法正确的是
A.c(HCO3-)略大于c(CO32-) B.c(HCO3-)等于c(CO32-)
C.c(Na+)等于c(CO32-)与c(HCO3-)之和 D.c(HCO3-)略小于c(CO32-)
查看答案和解析>>
科目:高中化学 来源: 题型:
现有浓度为0.1 mol/L的五种电解质溶液
①Na2CO3 ②NaHCO3 ③NaAlO2 ④CH3COONa ⑤NaOH
已知:CO2+3H2O+2AlO2-===2Al(OH)3↓+CO32-
(1)这五种溶液的pH由小到大的顺序是________________(填编号)。
(2)将五种溶液稀释相同的倍数时,其pH变化最大的是________(填编号)。
(3)在上述五种溶液中分别加入AlCl3溶液,能产生大量无色无味气体的是_______ _________(填编号)。
(4)将上述①、②、③、④四种溶液两两混合时,有一对溶液相互间能发生反应,则该反应的离子方程式是__________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列对熵的理解不正确的是
A.同种物质气态时熵值最大,固态时熵值最小
B.体系越有序,熵值越小;越混乱,熵值越大
C.与外界隔离的体系,自发过程将导致体系的熵减小
D.25 ℃、1.01×105 Pa时,2N2O5(g) 4NO2(g)+O2(g)是熵增的反应
4NO2(g)+O2(g)是熵增的反应
查看答案和解析>>
科目:高中化学 来源: 题型:
一答案 (1)0.1 mol·L-1·min-1 0.166 7 < (2)升高温度 (3)71.88%
定条件下,体积为1 L的密闭容器中发生如下反应:
SiF4(g)+2H2O(g)  SiO2(s)+4HF(g) ΔH=+148.9 kJ·mol-1
SiO2(s)+4HF(g) ΔH=+148.9 kJ·mol-1
(1)下列各项中能说明该反应已达化学平衡状态的是________(填字母序号)。
a.v消耗(SiF4)=4v生成(HF) b.容器内气体压强不再变化
c.容器内气体的总质量不再变化 d.HF的体积分数不再变化
(2)反应过程中测定的部分数据如下表(表中t2>t1)所示。
| 反应时间/min | n(SiF4)/mol | n(H2O)/mo |
| 0 | 1.20 | 2.40 |
| t1 | 0.80 | a |
| t2 | b | 1.60 |
通过a或b的值及化学平衡原理说明t1时反应是否达到化学平衡状态:_________________________________________________________________________。
(3)若只改变一个条件使上述反应的化学平衡常数变大,该反应________(填序号)。
a.一定向正反应方向移动 b.一定向逆反应方向移动
c.一定是减小压强造成的 d.一定是升高温度造成的 e.SiF4的平衡转化率一定增大
查看答案和解析>>
科目:高中化学 来源: 题型:
下列对进行焰色反应的实验操作注意事项的说明,正确的是( )
①钾的火焰颜色要透过蓝色钴玻璃观察
②先灼烧铂丝到火焰呈原色时,再蘸被检验物质
③每次实验后都要将铂丝蘸稀硫酸后灼烧至火焰呈无色为止
④没有铂丝可用无锈铁丝代替
A.仅③不正确 B.仅④不正确 C.③④不正确 D.②③④不正确
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com