
T ℃时,在1 L的密闭容器中充入2 mol CO2和6 mol H2,一定条件下发生反应:CO2(g)+3H2(g) CH3OH(g)+H2O(g) ΔH=-49.0 kJ·mol-1,测得H2和CH3OH(g)的浓度随时间变化如下表所示。下列说法不正确的是( )
CH3OH(g)+H2O(g) ΔH=-49.0 kJ·mol-1,测得H2和CH3OH(g)的浓度随时间变化如下表所示。下列说法不正确的是( )
| 时间/min | c(H2)/mol·L-1 | c(CH3OH)/mol·L-1 | v(正)和v(逆)比较 |
| t0 | 6 | 0 | ? |
| t1 | 3 | 1 | v(正)=v(逆) |
 励耘书业暑假衔接宁波出版社系列答案
励耘书业暑假衔接宁波出版社系列答案科目:高中化学 来源: 题型:单选题
某工业反应为:X2(g)+3Y2(g) 2XY3(g)。图Ⅰ表示在一定温度下此反应过程中的能量变化;图Ⅱ表示在2 L的密闭容器中反应时X2的物质的量随时间的变化曲线;图Ⅲ表示在其他条件不变的情况下,改变起始物Y2的物质的量对此反应平衡的影响。
2XY3(g)。图Ⅰ表示在一定温度下此反应过程中的能量变化;图Ⅱ表示在2 L的密闭容器中反应时X2的物质的量随时间的变化曲线;图Ⅲ表示在其他条件不变的情况下,改变起始物Y2的物质的量对此反应平衡的影响。
下列说法正确的是( )
| A.由图Ⅰ可知,加入适当的催化剂,E和ΔH都减小 |
| B.图Ⅱ中0~10 min内该反应的平均速率v(Y2)="0.045" mol·L-1·min-1,从11 min起其他条件不变,压缩容器的体积为1 L,则n(X2)的变化曲线为d |
| C.图Ⅲ中a、b、c三点所处的平衡状态中,反应物X2的转化率最高的是b点 |
| D.图Ⅲ中T1和T2表示温度,对应温度下的平衡常数为K1、K2,则T1<T2,K1<K2 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
T ℃时在2 L的密闭容器中X(g)与Y(g)发生反应生成Z(g)。反应过程中X、Y、Z的浓度变化如图(1)所示;若保持其他条件不变,反应温度分别为T1和T2时,Y的体积分数与时间的关系如图(2)所示。
则下列结论正确的是 ( )。
| A.反应进行的前3 min内,用X表示的反应速率v(X)=0.3 mol·(L·min)-1 |
B.容器中发生的反应可表示为3X(g)+Y(g) 2Z(g) 2Z(g) |
| C.保持其他条件不变,升高温度,反应的化学平衡常数K减小 |
| D.若改变反应条件,使反应进程如图(3)所示,则改变的条件是增大压强 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
温度为T ℃时,向2.0 L恒容密闭容器中充入2.0 mol NO2,反应2NO2(g)??N2O4(g)经一段时间后达到平衡。反应过程中测定的部分数据见下表:
| t/s | 0 | 50 | 150 | 250 | 350 |
| n(N2O4)/mol | 0 | 0.12 | 0.18 | 0.20 | 0.20 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
恒温、恒压下,a mol A和b mol B在一个容积可变的容器中发生如下反应:A(g)+2B(g) 2C(g),一段时间后达到平衡,生成n mol C。则下列说法中正确的是( )
2C(g),一段时间后达到平衡,生成n mol C。则下列说法中正确的是( )
A.物质A、B的转化率之比为a∶b
B.当v正(A)=2v逆(B)时,可确定反应到达平衡状态
C.起始时刻和达平衡后容器中的压强比为(a+b)∶(a+b— )
)
D.若起始时放入2a mol A和2b mol B,则达平衡时生成2n mol C
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
对于可逆反应N2(g)+3H2(g) 2NH3(g) ΔH<0,下列研究目的和示意图相符的是( )。
2NH3(g) ΔH<0,下列研究目的和示意图相符的是( )。
| | A | B |
| 研究 目的 | 压强对反应的影 响(p2>p1) | 温度对反应的影响 |
| 图示 | 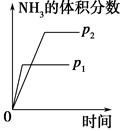 | 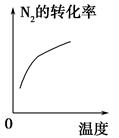 |
| 研究 目的 | 平衡体系增加N2 对反应的影响 | 催化剂对反应的影响 |
| 图示 |  | 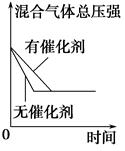 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
无水氯化铝是一种重要的催化剂,工业上由Al2O3制备无水氯化铝的反应为2Al2O3(s)+6Cl2(g) 4AlCl3(g)+3O2(g) ΔH>0。下列分析错误的是( )
4AlCl3(g)+3O2(g) ΔH>0。下列分析错误的是( )
| A.增大反应体系的压强,反应速率加快 |
| B.加入碳粉,平衡向右移动,原因是碳与O2反应,降低了生成物的浓度且放出热量 |
| C.电解熔融的Al2O3和AlCl3均能得到单质铝 |
| D.将AlCl3·6H2O在氯化氢气流中加热,也可制得无水氯化铝 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
在恒容条件下化学反应:2SO2(g)+O2(g) 2SO3(g) ΔH="-Q" kJ·mol-1。在上述条件下分别充入的气体和反应放出的热量(Q)如表所列:
2SO3(g) ΔH="-Q" kJ·mol-1。在上述条件下分别充入的气体和反应放出的热量(Q)如表所列: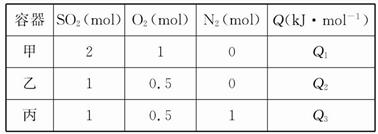
根据以上数据,下列叙述正确的是( )
| A.在上述条件下反应生成1 mol SO3固体放热Q/2 kJ | B.2Q3<2Q2=Q1<Q |
| C.Q1=2Q2=2Q3=Q | D.2Q2=2Q3<Q1<Q |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com