
【题目】二氯化二硫(S2Cl2)是一种重要的化工原料,常用作橡胶硫化剂,改变生橡胶受热发粘、遇冷变硬的性质。查阅资料可知S2Cl2具有下列性质:
(1)制取少量S2Cl2
物理性质 | 毒性 | 色态 | 挥发性 | 熔点 | 沸点 |
剧毒 | 金黄色液体 | 易挥发 | -76℃ | 138℃ | |
化学性质 | ①300℃以上完全分解; ②S2Cl2+Cl2 ③遇高热或与明火接触,有引起燃烧的危险; ④受热或遇水分解放热,放出腐蚀性烟气; | ||||
实验室可利用硫与少量氯气在110~140℃反应制得S2Cl2粗品。
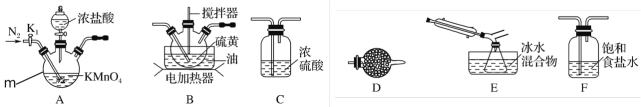
①仪器m的名称为___________,装置F中试剂的作用是__________。
②装置连接顺序:A→_______________→E→D。
③实验前打开K1,通入一段时间的氮气排尽装置内空气。实验结束停止加热后,再通入一段时间的氮气,其目的是_____________。
④为了提高S2Cl2的纯度,实验的关键是控制好温度和_____________。
(2)S2Cl2遇水强烈反应产生烟雾,该反应的化学方程式2S2Cl2+2H2O=SO2↑+3S↓+4HCl↑甲同学为了验证两种气体产物,将水解生成的气体依次通过硝酸银与稀硝酸的混合溶液、品红溶液、NaOH溶液,该方案_________(填“可行”或“不可行”),原因是___________。
(3)某同学为了测定S2Cl2与水反应后生成的气体X在混合气体中的体积分数,设计了如下实验方案:

①W溶液可以是____________(填标号)。
aH2O2溶液 bKMnO4溶液(硫酸酸化) c氯水
②该混合气体中气体X的体积分数为_____________(用含V、m的式子表示)。
【答案】三颈烧瓶 除去Cl2中混有的HCl杂质 FCB 将装置内的氯气排入D内吸收以免污染空气,并将B中残留的S2Cl2排入E中收集 滴入浓盐酸的速率(或B中通入氯气的量) 不可行 二氧化硫被硝酸氧化成硫酸根,既难于检验二氧化硫又干扰氯化氢检验 ac ![]() ×100%
×100%
【解析】
(1)根据实验目的及实验装置分析解答;(2)根据物质的性质及常见的物质检验方法分析解答;(3)根据分析氧化剂的氧化性强弱分析解答,根据元素守恒及题给数据计算体积体积分数。
(1)①根据仪器构造分析知,仪器m的名称为三颈烧瓶;实验室可利用硫与少量氯气在110~140℃反应制得S2Cl2粗品,氯气过量则会生成SCl2,利用装置A制备氯气,氯气中含氯化氢气体和水蒸气,通过装置F除去氯化氢,通过装置C除去水蒸气,通过装置B和硫磺反应在110~140℃反应制得S2Cl2粗品,通过装置E冷凝得到二氯化二硫(S2Cl2),连接装置D是防止空气中水蒸气进入,故答案为:三颈烧瓶;除去Cl2中混有的HCl杂质;
②利用装置A制备氯气,氯气中含氯化氢气体和水蒸气,通过装置F除去氯化氢,通过装置C除去水蒸气,通过装置B和硫磺反应在110~140℃反应制得S2Cl2粗品,通过装置E冷凝得到二氯化二硫(S2Cl2),连接装置D是防止空气中水蒸气进入,依据上述分析可知装置连接顺序为:A→F→C→B→E→D,故答案为:FCB;
③实验前打开K1,通入一段时间的氮气排尽装置内空气。实验结束停止加热后,再通入一段时间的氮气,其目的是:将装置内的氯气排入D内吸收以免污染空气,并将B中残留的S2Cl2排入E中收集,故答案为:将装置内的氯气排入D内吸收以免污染空气,并将B中残留的S2Cl2排入E中收集;
④反应生成S2Cl2的氯气过量则会生成SCl2,温度过高S2Cl2会分解,为了提高S2Cl2的纯度,实验的关键是控制好温度和滴入浓盐酸的速率或B中通人氯气的量,故答案为:滴入浓盐酸的速率或B中通人氯气的量;
(2)二氧化硫具有还原性,能被硝酸氧化生成硫酸根,无法使品红褪色。硫酸根结合银离子生成硫酸银沉淀,干扰氯离子的检验,故答案为:不可行;二氧化硫被硝酸氧化成硫酸根,既难于检验二氧化硫又干扰氯化氢检验;
(3)①W溶液是吸收氧化二氧化硫的溶液,可以是a.H2O2溶液,c.氯水,但不能是b.KMnO4溶液(硫酸酸化),因为高锰酸钾溶液能氧化氯化氢生成氯气,故答案为:ac;
②过程分析可知生成沉淀为硫酸钡沉淀,硫元素守恒得到二氧化硫物质的量n(SO2)=n(BaSO4)=![]() ,该混合气体中二氧化硫的体积分数为气体物质的量分数,则二氧化硫体积分数=
,该混合气体中二氧化硫的体积分数为气体物质的量分数,则二氧化硫体积分数= ,故答案为:
,故答案为:![]() 。
。


科目:高中化学 来源: 题型:
【题目】生物质能是一种洁净、可再生的能源。生物质气(主要成分为CO、CO2、H2等)与H2混合,催化合成甲醇是生物质能利用的方法之一。
(1)上述反应的催化剂含有Cu、Zn、Al等元素。写出基态Zn原子的核外电子排布式________。
(2)根据等电子原理,写出CO分子的结构式______。
(3)甲醇催化氧化可得到甲醛,甲醛与新制Cu(OH)2的碱性溶液反应生成Cu2O沉淀。
①甲醇的沸点比甲醛的高,其主要原因是______________;甲醛分子中碳原子轨道的杂化类型为________。
②甲醛分子的空间构型是________;1 mol甲醛分子中σ键的数目为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是2004年批量生产的笔记本电脑所用甲醇燃料电池的结构示意图。甲醇在催化剂作用下提供质子(H+)和电子,电子经外电路、质子经内电路到达另一极与氧气反应,电池总反应为2CH30H+302=2C02+4H20。下列说法正确的是

A. 左电极为电池的正极,a处通入的物质是甲醇
B. 右电极为电池的负极,b处通入的物质是空气
C. 负极反应式为:CH30H+H20-6e-=CO2+6H+
D. 正极反应式为:02+2H20+4e-=40H—
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】回答下列问题:
(1)铅蓄电池的总反应为:Pb + PbO2 + 2H2SO4 ![]() 2PbSO4 + 2H2O,放电时,负极反应式为___________,充电时,阳极反应式为___________。
2PbSO4 + 2H2O,放电时,负极反应式为___________,充电时,阳极反应式为___________。
(2)利用如图装置,可以模拟铁的电化学防护。
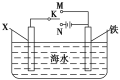
①若X为石墨,为减缓铁的腐蚀,将开关K置于N处,该电化学防护法称为___________。
②若X为锌,开关K置于M处,该电化学防护法称为__________。
(3)我国的科技人员为了消除SO2的污染,利用原电池原理,设计如图2装置用SO2和O2制备硫酸,电极A、B为多孔的材料。
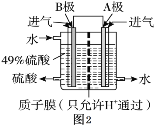
① A极的电极反应式是________。
② B极的电极反应式是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A、B、C、D、E、F是元素周期表中前36号元素,它们的原子序数依次增大。A的质子数、电子层数、最外层电子数均相等,B元素基态原子中电子占据三种能量不同的原子轨道且每种轨道中的电子总数相同,D的基态原子核外成对电子数是成单电子数的3倍,E4+与氩原子的核外电子排布相同。F是第四周期d区原子序数最大的元素。请回答下列问题:
(1)写出E的价层电子排布式 。
(2)A、B、C、D电负性由大到小的顺序为 (填元素符号)。
(3)F(BD)4为无色挥发性剧毒液体,熔点-25℃ ,沸点43℃。不溶于水,易溶于乙醇、乙醚、苯等有机溶剂,呈四面体构型,该晶体的类型为 ,F与BD之间的作用力为 。
(4)开发新型储氢材料是氢能利用的重要研究方向。
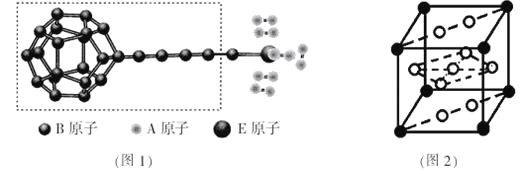
①由A、B、E三种元素构成的某种新型储氢材料的理论结构模型如图1所示,图中虚线框内B原子的杂化轨道类型有 种;
②分子X可以通过氢键形成“笼状结构”而成为潜在的储氢材料。X一定不是 (填标号);
A.H2O B.CH4C.HF D.CO(NH2)2
③F元素与镧( La)元素的合金可做储氢材料,该晶体的晶胞如图2所示,晶胞中心有一个F原子,其他F原子都在晶胞面上,则该晶体的化学式为_______________;已知其摩尔质量为M g.mol-1,晶胞参数为a pm,用NA表示阿伏伽德罗常数,则该晶胞的密度为 g.cm-3。
查看答案和解析>>
科目:高中化学 来源: 题型:
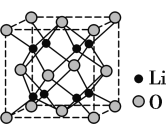
【题目】(1)Li2O具有反萤石结构,晶胞如图所示。已知晶胞参数为0.466 5 nm,阿伏加德罗常数的值为NA,则Li2O的密度为__________ g·cm-3(列出计算式)。
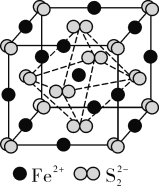
(2)FeS2晶体的晶胞如图所示。晶胞边长为a nm、FeS2相对式量为M、阿伏加德罗常数的值为NA,其晶体密度的计算表达式为________g·cm-3;晶胞中Fe2+位于S![]() 所形成的正八面体的体心,该正八面体的边长为____nm。
所形成的正八面体的体心,该正八面体的边长为____nm。
(3)我国科学家最近成功合成了世界上首个五氮阴离子盐(N5)6(H3O)3(NH4)4Cl(用R代表)。R的晶体密度为d g·cm-3,其立方晶胞参数为a nm,晶胞中含有y个[(N5)6(H3O)3(NH4)4Cl]单元,该单元的相对质量为M,则y的计算表达式为______________。
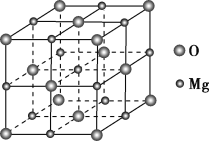
(4)MgO具有NaCl型结构(如图),其中阴离子采用面心立方最密堆积方式,X射线衍射实验测得MgO的晶胞参数为a=0.420 nm,则r(O2-)为________nm。MnO也属于NaCl型结构,晶胞参数为a′=0.448 nm,则r(Mn2+)为____________nm。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质属于分子晶体的是( )
A. 熔点是10.31℃,液态不导电,水溶液能导电
B. 熔点是1070℃,固态不导电,熔融状态能导电,易溶于水
C. 熔点3550℃,不溶于水,不导电
D. 熔点是97.80℃,质软,固态可导电,密度是0.97g·cm﹣3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳酸亚铁在空气中灼烧得到铁的氧化物A和一种气体。某学习小组为了探究该氧化物A的组成设计了两种实验方案:
方案Ⅰ
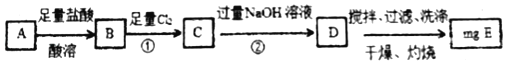
(1)若该方案中①通入Cl2不足量,小组成员认为可以通过在空气中充分搅拌D而最终实现准确测定,他的依据是_____(用化学方程式表示)
(2)若氧化物A的质量是7.8400g,E的质量为8.0000g根据数据计算化合物A的化学式为_____。
方案Ⅱ
①称取ag氧化物A样品溶于足量稀硫酸,并配成100mL溶液。
②取20.00 mL该溶液于锥形瓶中,滴加几滴KSCN溶液,溶液变红色;再滴加双氧水至红色刚好褪去,同时产生少量气泡(资料显示SCN-可被H2O2氧化,产物为N2、CO2、SO42﹣)
③待气泡消失后,用 b mol/LKI标准溶液滴定锥形瓶中的Fe3+,滴定终点时消耗cmL KI标准溶液。
(3)该方案用到的定量仪器有量筒、分析天平、酸式滴定管、_____。
(4)步骤②中滴加KSCN溶液的目的是_____。
(5)补充完整该实验步骤③用到的酸式滴定管的润洗操作:关闭滴定管旋塞,从上口注入3﹣5mL待装液,_____,重复2﹣3次。
(6)步骤③能否选用淀粉作指示剂_____。(填“能”或“否”)
(7)有的同学通过查阅相关资料对该小组的实验设计进行了评价,以下说法合理的是_____
A.资料显示:HSCN有剧毒,易挥发。因此该方案步骤②可能因产生HSCN而不符合实验安全性的要求。
B.步骤②若加入H2O2过量,后续步骤不加以处理也不会对实验结果造成任何影响。
C.资料显示:Fe3+和I﹣之间的反应是明显的可逆反应,这样步骤③就会造成滴定测定不准确
(8)有的同学对碳酸亚铁的获得产生了兴趣。通过查阅资料发现碳酸亚铁可通过碳酸氢钠和硫酸亚铁发生Fe2++2HCO3﹣FeCO3↓+H2CO3制得,请计算该反应的平衡常数K=_____(mol/L)﹣2可能用到的缴据如下:Ksp(FeCO3)=3.20×10﹣11,H2CO3的Ka1=4.30×10﹣7,Ka2=5.61×10﹣11。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁、钴、镍等金属及其化合物在科学研究和工业生产中应用十分广泛。回答下列问题:
(1)铁、钴、镍的基态原子核外未成对电子数最多的是_________。
(2)酞菁钴分子的结构简式如图所示,中心离子为钴离子,酞钴分子中与钴离子通过配位键结合的氮原子的编号是_______(填1、2、3、4),三种非金属原子的电负性由大到小的顺序为_______(用相应的元素符号表示);氮原子的杂化轨道类型为________。

(3)Fe(CO)x常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂,据此可判断Fe(CO)x,晶体属于_______(填晶体类型),若配合物Fe(CO)x的中心原子价电子数与配体提供电子数之和为18,则x=________。
(4)NiO、FeO的晶体结构类型与氯化钠的相同,Ni2+和Fe2+的离子半径分别为69pm和78pm,则熔点NiO______FeO(填“>”“<”或“=”),原因是_________。
(5)NiAs的晶胞结构如图所示:①镍离子的配位数为_________。
②若阿伏加德罗常数的值为NA,晶体密度为pg·cm-3,则该晶胞中最近的Ni2+之间的距离为________cm。(写出计算表达式)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com